备考2020年中考 化学一轮基础复习:专题二十三 酸碱中和反应
试卷更新日期:2020-03-17 类型:一轮复习
一、单选题
-
1. 下列表述正确的是( )A、稀盐酸和稀硫酸化学性质相似的原因是溶液中都含有H+ B、用pH试纸测定某未知溶液的pH为5.5 C、生成盐和水的反应一定是中和反应 D、使酚酞试液变红色的一定是碱2. 下列实际应用中,利用中和反应原理的是( )
①用氢氧化钠溶液洗涤石油中残余硫酸;②用氢氧化铝治疗胃酸;
③用熟石灰改良酸性土壤;④将稀氨水(含有NH4+、OHˉ)涂抹在蚊虫叮咬处(分泌岀蚁酸)止痒。
A、①②③④ B、仅①②③ C、仅②③④ D、仅①③④3. 在A+B →C+D的反应中,下列叙述错误的是( )
A、若C和D为盐和水,该反应不一定是中和反应 B、若A是氧化铜、C为铜,该反应不一定是置换反应 C、若将20gA和30gB混合,则生成C和D的总质量一定为50g D、此反应可能是复分解反应4. 下列图象不能正确反映其对应变化关系的是()A、电解水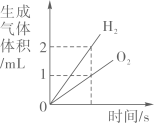 B、向硫酸钠与盐酸的混合溶液中逐滴滴入氢氧化钡溶液
B、向硫酸钠与盐酸的混合溶液中逐滴滴入氢氧化钡溶液 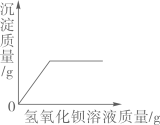 C、向氢氧化钠溶液中逐滴滴入稀硫酸溶液
C、向氢氧化钠溶液中逐滴滴入稀硫酸溶液 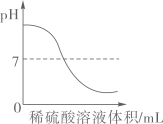 D、向一定量的氯化亚铁和氯化铜混合溶液中加入镁粉
D、向一定量的氯化亚铁和氯化铜混合溶液中加入镁粉 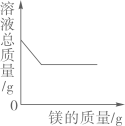
二、填空题
-
5. 化学与我们的生产、生活息息相关(1)、向酸性土壤里撒(填俗称);(2)、84消毒液是一种有刺激性气味的高效液体消毒剂,广泛用于宾馆、医院、家庭等,主要成分为次氯酸钠(NaClO),次氯酸钠自身没有消毒作用,有消毒作用的是次氯酸钠与空气中二氧化碳反应得到的次氯酸(HClO),发生的反应为2 NaClO+CO2+X=Na2CO3+2HClO,则X是(填化学式),写出次氯酸钠(NaClO)的化学式并标出氯元素的化合价为。84消毒液是含氯消毒剂,氯气是种挥发性有毒气体,因此84消毒液必须保存。6. 化学与生活密切相关,请按要求填空。(1)、用来检验无水酒精中是否含有水的物质是化学式为;(2)、引起酸雨的主要物质是;(3)、自来水生产过程中加液氯的目的是;(4)、丙烷(C3H8)是液化石油气的主要成分,C3H8的摩尔质量是 , 其中碳元素的质量分数是(用分数表示),0.25molC3H8中约含有个H原子。7. 宏观和微观相联系是化学独特的思维方式,微观探析化学反应的规律是化学科学的核心任务。根据下列微观示意图回答问题。
 (1)、从微观的角度说明图示反应的实质是;(2)、该反应的化学方程式是。(3)、若反应中NaOH稍过量,则反应后,溶液中存在的微观粒子有。
(1)、从微观的角度说明图示反应的实质是;(2)、该反应的化学方程式是。(3)、若反应中NaOH稍过量,则反应后,溶液中存在的微观粒子有。三、实验探究题
-
8. 兴趣小组的同学探究盐酸与氢氧化钠溶液能发生中和反应,以及反应后溶液的成分,进行了如右下图所示的实验,并绘制了反应过程中烧杯内溶液的pH随加入溶液体积的变化曲线图。请你参与学习并填写空格:
 (1)、烧杯中盛放的是溶液;(2)、曲线上b点坐标为(18,7),该点所表示的意义是。(3)、同学们对反应后溶液的成分进行探究如下:
(1)、烧杯中盛放的是溶液;(2)、曲线上b点坐标为(18,7),该点所表示的意义是。(3)、同学们对反应后溶液的成分进行探究如下:【提出问题】反应后溶液中的微粒有什么?
【假设猜想】依据曲线上的点和已学
知识分析,提出了以下四种猜想:
猜想一:只有Na+、Cl-、H2O;
猜想二:有Na+、Cl-、H2O、H+;
猜想三:有Na+、Cl-、H2O、OH-
猜想四:有Na+、Cl-、H2O、H+、OH-。
小红同学认为猜想是不合理的,理由是 。
(4)、【实验探究】①小芳同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,说明猜想 不成立;
②小君同学取烧杯中的溶液少量于试管中,滴加几滴酚酞溶液,无明显变化,认为猜想一成立。小明同学认为小君同学的判断不科学,理由是 。
③小兰同学取烧杯中的溶液少量于试管中,滴加几滴碳酸钠溶液,观察到有气泡产生,由此断定猜想二成立。该实验中发生反应的化学方程式是。
【实验拓展】
请你用与①、②、③不同类别的试剂,设计另一种方案验证猜想二成立。
实验操作
实验现象
实验结论
猜想二成立
9. A、B、C是金属活动性顺序表中的三种金属。取形状大小相同的A、B、C三种金属,分别向其加入同体积同溶质质量分数的稀盐酸,实验现象如下表所示,请回答:实验

现象
速率快,产生大量气泡
速率缓慢,产生气泡较少
无现象
(1)、A,B,C三种金属的活动性由强到弱的顺序是(填字母)。(2)、将金属C放入硝酸银溶液中,其表面有银析出,写出该反应的化学方程式。(3)、向金属A反应后的溶液中滴入几滴紫色石蕊试剂,溶液变红色。则此溶液的pH(填“>”“<”或“=”)7。再向该溶液中滴加NaOH溶液,溶液由红色变为紫色,发生的化学反应方程式为。10. 某化学兴趣小组用实验室常用药品(或溶液)对“NaOH溶液与稀盐酸是否恰好完全反应”进行探究。(知识卡片):氯化钠溶液显中性。氯化铜易溶于水。
(实验探究):
(1)、方案Ⅰ:某同学先向试管中加入约2mLNaOH溶液,再滴入几滴酚酞溶液,溶液变红。然后慢慢滴入稀盐酸,边滴边振荡,直至溶液恰好变为无色。①实验结论。
②从微观的角度分析,该反应的实质是。
③在滴入稀盐酸的过程中,若观察到有少量气泡出现,请分析产生气泡的可能原因(用化学方程式表示)。
(2)、方案Ⅱ:实验步骤
实验现象
结论
取2mLNaOH溶液于试管中,滴入一定量的稀盐酸,振荡后加入镁条
若
稀盐酸过量
若没有明显现象
NaOH溶液与稀盐酸恰好完全反应
(3)、(实验反思):另有同学提出方案Ⅱ不能证明NaOH溶液与稀盐酸恰好完全反应,其原因是。
(4)、除以上方案外,下列哪些物质单独使用,也能证明“NaOH 溶液与稀盐酸是否恰好完全反应” (填序号)。A 铜片 B pH试纸 C 氧化铜 D 紫色石蕊试液
四、综合题
-
11. 在用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示:
 (1)、该实验操作是将滴加到另一种溶液中。(2)、当加入溶液的质量为a g时,所得溶液中的溶质为(写化学式)。(3)、当加入溶液的质量为bg时,向所得溶液中滴加酚酞溶液,溶液呈色(4)、氢氧化钠溶液与稀盐酸发生中和反应时观察不到明显现象,为了确定其反应是否发生,某班同学设计了不同的实验方案进行探究
(1)、该实验操作是将滴加到另一种溶液中。(2)、当加入溶液的质量为a g时,所得溶液中的溶质为(写化学式)。(3)、当加入溶液的质量为bg时,向所得溶液中滴加酚酞溶液,溶液呈色(4)、氢氧化钠溶液与稀盐酸发生中和反应时观察不到明显现象,为了确定其反应是否发生,某班同学设计了不同的实验方案进行探究方案一:向装有一定量氢氧化钠溶液的烧杯中滴几滴酚酞试液,不断滴入稀盐酸,并用玻璃棒搅拌。如果实验现象是就可以证明氢氧化钠溶液与稀盐酸发生了化学反应;
方案二:向装有一定量稀盐酸的试试管中滴加氢氧化钠溶液,振荡后再向其中滴加碳酸钠溶液,如果有气泡产生,则说明氢氧化钠溶液与稀盐酸没有发生化学反应。 你认为方案二的结论正确吗?(填“正确”或“错误”),理由是:。