备考2020年中考 化学一轮基础复习:专题十一 化学方程式的相关计算
试卷更新日期:2020-03-17 类型:一轮复习
一、单选题
-
1. 下列图像能正确反映其对应关系的是( )A、电解水
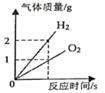 B、加热一定质量的氯酸钾和二氧化锰的混合物
B、加热一定质量的氯酸钾和二氧化锰的混合物 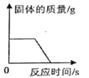 C、发生的反应为2KNO3 2KNO2+O2↑
C、发生的反应为2KNO3 2KNO2+O2↑  D、等质量的碳酸钙分别与足量等体积等浓度的稀盐酸反应
D、等质量的碳酸钙分别与足量等体积等浓度的稀盐酸反应  2. 在一定条件下,一个密闭容器内发生某反应,测得反应过程中各物质的质量部分数据如下表所示。下列说法正确的是()
2. 在一定条件下,一个密闭容器内发生某反应,测得反应过程中各物质的质量部分数据如下表所示。下列说法正确的是() A、a等于10 B、该化学反应为分解反应 C、丙一定为催化剂 D、b等于123. 密闭容器中加入甲、乙、丙、丁四种物质,使之充分反应,反应前后测得有关数据如表
A、a等于10 B、该化学反应为分解反应 C、丙一定为催化剂 D、b等于123. 密闭容器中加入甲、乙、丙、丁四种物质,使之充分反应,反应前后测得有关数据如表物质
甲
乙
丙
丁
反应前质量/g
18
1
2
32
反应后质量/g
X
26
2
12
下列说法中,不正确的是()
A、反应后物质甲的质量为13g B、物质丙可能是该反应的催化剂 C、反应中乙、丁的质量比为5:4 D、乙是反应物4. 在反应2A+B=3C+D中,A和B的相对分子质量之比为5:1,已知20gA与一定量B恰好完全反应,生成5gD,则在此反应中B和C的质量比为()A、4:19 B、3:5 C、1:3 D、2:17二、计算题
-
5. 化学兴趣小组为测定某铜锌合金中成分金属的含量,称取10g样品放入烧杯中,向其中加入100g稀硫酸,样品中的锌恰好完全反应,此时测得烧杯内物质的总质量为109.8g。
请完成下列分析及计算:
(1)、硫酸(H2SO4)中硫元素的质量分数为(计算结果精确到0.1%)。(2)、反应中共生成气体g。(3)、计算样品中铜的质量分数。6. 为了测定大理石样品中钙的质量分数(杂质不含钙元素,不溶于水,也不与其他物质发生反应),进行了如下实验。请回答下列问题。 (1)、上述实验过程中发生反应的化学方程式为。(2)、根据已知条件列出求解第一次所加的稀盐酸中溶质的质量(X)的比例式。(3)、此大理石样品中钙元素的质量分数 。(4)、用36.5%的浓盐酸配制200g上述稀盐酸,所需盐酸的质量为。(5)、若将反应后的滤液蒸发11.2g水,无晶体析出,所得溶液中溶质的质量分数为。(6)、现有上述大理石样品500t,可以制得含杂质的生石灰的质量为。7. 长久使用的热水壶底部有一层水垢,主要成分是碳酸钙(CaCO3),某化学兴趣小组为了测定水垢中碳酸钙的质量分数,取25g水垢放入过量的稀盐酸的烧杯中,立即将烧杯放在天平上,称其质量。在以后的5min内,每一分钟读一次数。结果如下表,试回答下列问题:
(1)、上述实验过程中发生反应的化学方程式为。(2)、根据已知条件列出求解第一次所加的稀盐酸中溶质的质量(X)的比例式。(3)、此大理石样品中钙元素的质量分数 。(4)、用36.5%的浓盐酸配制200g上述稀盐酸,所需盐酸的质量为。(5)、若将反应后的滤液蒸发11.2g水,无晶体析出,所得溶液中溶质的质量分数为。(6)、现有上述大理石样品500t,可以制得含杂质的生石灰的质量为。7. 长久使用的热水壶底部有一层水垢,主要成分是碳酸钙(CaCO3),某化学兴趣小组为了测定水垢中碳酸钙的质量分数,取25g水垢放入过量的稀盐酸的烧杯中,立即将烧杯放在天平上,称其质量。在以后的5min内,每一分钟读一次数。结果如下表,试回答下列问题:时间/min
1
2
3
4
5
质量/g
100g
95g
92g
91.2g
91.2g
(1)、反应生成的二氧化碳的质量为多少?(2)、该水垢中CaCO3的质量分数为多少?8. 某化学兴趣小组同学为回收一块铜锌合金中的铜,按照图进行实验恰好完全反应),计算: (1)、4.0g铜锌合金中锌的质量是g。(2)、所用稀硫酸的溶质的质量分数。9. 25g大理石和100g稀盐酸溶液恰好完全反应(杂质不与酸反应),反应结束后,称得烧杯内物质的质量为116.2g,求:(1)、反应中生成CO2的质量;(2)、该大理石中CaCO3的质量分数。
(1)、4.0g铜锌合金中锌的质量是g。(2)、所用稀硫酸的溶质的质量分数。9. 25g大理石和100g稀盐酸溶液恰好完全反应(杂质不与酸反应),反应结束后,称得烧杯内物质的质量为116.2g,求:(1)、反应中生成CO2的质量;(2)、该大理石中CaCO3的质量分数。三、综合题
-
10. 我国科学家研究发现由CO2高效转化为甲醇(CH3OH)的新技术,该反应的微观过程如图所示:

请推断出物质丁并回答下列问题
(1)、上述甲→丁四种物质中属于氧化物的有(填化学式)。(2)、写出该反应的化学方程式。(3)、类比乙醇的燃烧,写出甲醇在空气中完全燃烧的化学方程式。(4)、若22g CO2全部转化为CH3OH,且反应中其它物质均不含碳元系,可生成CH3OH的质量为g。11. 为了测定混有少量杂质的高锰酸钾固体样品中高锰酸钾的质量分数,取20g样品加热(杂质不反应、不含氧元素),剩余固体的质量与加热时间的关系如下表所示:加热时间/min
t0
t1
t2
t3
t4
t5
t6
剩余固体质量/g
20
20
19.6
18.8
18.6
18.4
18.4
(1)、t0至t1时间段,固体质量不变的原因是。(2)、反应中产生氧气的质量是 。(3)、求样品中高锰酸钾的质量是多少?(写出计算过程)(4)、该高锰酸钾固体样品中高锰酸钾的质量分数为。(5)、请分析题中数据,绘制20g高锰酸钾样品中氧元素的质量随着时间的变化图,并标注折点数据。