湖南省邵阳市武冈三中2016-2017学年中考模拟化学考试试卷
试卷更新日期:2017-08-21 类型:中考模拟
一、选择题
-
1. 以下古代诗词中涉及到化学变化的是( )A、粉身碎骨浑不怕,要留清白在人间 B、欲渡黄河冰塞川,将登太行雪满山 C、气蒸云梦泽,波撼岳阳城 D、忽如一夜春风来,千树万树梨花开2. 青少年正处于生长发育期,需要摄取较多的蛋白质.下面几种来自邵阳的美食中,主要成分富含蛋白质的是( )A、邵阳米粉 B、新宁脐橙 C、宝庆腊肉 D、邵阳茶油3. 下列物质中,能用作氮肥的是( )A、K2SO4 B、NH4HCO3 C、K2CO3 D、Ca(HPO4)24. 干燥多风季节的夜晚,在荒野里,人们有时看到“鬼火”现象,其实它是一种类似于氨气组成的气体(pH3)在空气中的自燃现象,pH3中P元素的化合价是( )A、﹣3 B、+3 C、+1 D、+55. 材料与人类生活密切相关,下列物品与所用材料的对应关系不正确的是( )A、尼龙绳﹣﹣合成纤维 B、医用剪刀﹣﹣合金 C、羊绒围巾﹣﹣天然纤维 D、汽车轮胎﹣﹣塑料6. 下列实验操作正确的是( )A、
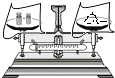 称量药品质量
B、
称量药品质量
B、 检测溶液pH
C、
检测溶液pH
C、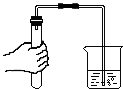 检查装置气密性
D、
检查装置气密性
D、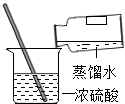 浓硫酸稀释
7. 下列化学用语与正确的是( )A、2个氢原子:2H B、氧分子:O C、铜离子:Cu2+ D、硫酸钠:NaSO48. 关于分子和原子两种微粒的叙述正确的是( )A、物质只能由分子构成 B、相同原子可能构成不同的分子 C、分子在不断运动,原子静止不动 D、化学变化中分子数目一定发生变化9. 科学家计划用质子数为20的钙原子,轰击核电荷数为98的锎元素靶,使两元素的原子核合并在一起,合成核电荷数为118的新元素.对此理解正确的是( )A、新元素的原子核外电子数为116 B、新元素的原子序数为118 C、新元素的相对原子质量为118 D、变化过程中元素种类没有发生改变10. 图是表示气体分子的示意图,图中“●”和“○”分别表示质子数不同的两种原子,其中表示化合物的是( )A、
浓硫酸稀释
7. 下列化学用语与正确的是( )A、2个氢原子:2H B、氧分子:O C、铜离子:Cu2+ D、硫酸钠:NaSO48. 关于分子和原子两种微粒的叙述正确的是( )A、物质只能由分子构成 B、相同原子可能构成不同的分子 C、分子在不断运动,原子静止不动 D、化学变化中分子数目一定发生变化9. 科学家计划用质子数为20的钙原子,轰击核电荷数为98的锎元素靶,使两元素的原子核合并在一起,合成核电荷数为118的新元素.对此理解正确的是( )A、新元素的原子核外电子数为116 B、新元素的原子序数为118 C、新元素的相对原子质量为118 D、变化过程中元素种类没有发生改变10. 图是表示气体分子的示意图,图中“●”和“○”分别表示质子数不同的两种原子,其中表示化合物的是( )A、 B、
B、 C、
C、 D、
D、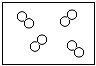 11. 资阳市2011年5月20日空气质量报告:老城区空气污染指数为64,空气质量级别为Ⅱ级,空气质量状况为良,空气首要污染物为可吸入颗粒物.下列有关空气各成分的说法正确的是( )A、氧气的化学性质比较活泼,属于可燃物 B、氮气的化学性质不活泼,可用于食品防腐 C、空气质量报告中所列的空气质量级别越大,空气质量越好 D、二氧化碳在空气中含量增多会引起温室效应,属于空气污染物12. 下列事实与对应解释不相符合的是( )A、氧化汞分解成汞和氧气﹣﹣分子可以再分 B、甘蔗甜,苦瓜苦﹣﹣不同分子性质不同 C、切洋葱时可闻到刺激性气味﹣﹣分子在不停运动 D、结冰的水不能流动(0℃以下)﹣﹣水分子不再运动13. 某原子的最外层上的电子数为1,则此元素( )A、一定是非金属元素 B、一定是金属元素 C、一定是稀有气体元素 D、无法确定14. 如图是电解水的简易装置,下列有关叙述不正确的是( )
11. 资阳市2011年5月20日空气质量报告:老城区空气污染指数为64,空气质量级别为Ⅱ级,空气质量状况为良,空气首要污染物为可吸入颗粒物.下列有关空气各成分的说法正确的是( )A、氧气的化学性质比较活泼,属于可燃物 B、氮气的化学性质不活泼,可用于食品防腐 C、空气质量报告中所列的空气质量级别越大,空气质量越好 D、二氧化碳在空气中含量增多会引起温室效应,属于空气污染物12. 下列事实与对应解释不相符合的是( )A、氧化汞分解成汞和氧气﹣﹣分子可以再分 B、甘蔗甜,苦瓜苦﹣﹣不同分子性质不同 C、切洋葱时可闻到刺激性气味﹣﹣分子在不停运动 D、结冰的水不能流动(0℃以下)﹣﹣水分子不再运动13. 某原子的最外层上的电子数为1,则此元素( )A、一定是非金属元素 B、一定是金属元素 C、一定是稀有气体元素 D、无法确定14. 如图是电解水的简易装置,下列有关叙述不正确的是( ) A、与甲试管中的电极相连的是电池的负极 B、产生气体时,水槽中的液面会逐渐上升 C、乙试管内的气体能使带火星木条复燃 D、若将试管换成量筒,则能直接计算出生成气体的质量比15. 在细菌作用下,可以用氨气处理含有甲醇(CH3OH)的工业废水,有关反应的化学方程式为5CH3OH+12O2+6NH3═3N2+5X+19H2O,则X的化学式为( )A、NO B、CO2 C、H2 D、CO16. 下列有关碳及其化合物的叙述不正确的是( )A、二氧化碳、一氧化碳均能使紫色石蕊溶液变红 B、一定温度下C和CO均可将氧化铜还原成铜 C、金刚石、石墨完全燃烧均生成二氧化碳 D、石灰石、大理石都可与稀盐酸反应17. 下列化学方程式对应的反应类型均不正确的是( )A、4P+O2═2P2O5 化合反应 B、H2O H2↑+O2↑ 分解反应 C、C+CuO Cu+CO2 置换反应 D、HCl+NaOH═NaCl+H2O 复分解反应18. 下列关于溶液的叙述正确的是( )A、汽油洗衣服上的油污是利用了乳化作用 B、硝酸铵固体溶于水时仅发生扩散吸热的过程 C、某物质的不饱和溶液变为饱和溶液后溶质质量分数可能不变 D、“波尔多液”是无色、透明、均一稳定的混合物19. “关爱生命,拥抱健康”是永恒的主题.下列做法不会损害人体健康的是( )A、用含小苏打的发酵粉焙制糕点 B、用三聚氰胺提高牛奶中蛋白质的含量 C、用NaNO2腌制肉制品 D、“瘦肉精”提高猪的瘦肉率20. 化学时刻影响着我们的生活,它在工农业生产和日常生活中起到了非常重要的作用.下列说法中正确的是( )A、微量元素在人体内的需求量很小,不需要从外界摄取 B、纤维素无法被人体吸收,所以食物中的纤维素对人体毫无意义 C、硫酸铜可用于配制农药波尔多液,但不能用铁桶盛放 D、木炭燃烧的剧烈程度由它的着火点决定,而与氧气的浓度无关21. 液化石油气是一种常用的家庭燃料,泄漏时如果处理不当,常常会酿成悲剧.为了安全起见,最好在厨房安装报警器,如果报警器显示有液化气泄漏,应立即采取的措施是( )
A、与甲试管中的电极相连的是电池的负极 B、产生气体时,水槽中的液面会逐渐上升 C、乙试管内的气体能使带火星木条复燃 D、若将试管换成量筒,则能直接计算出生成气体的质量比15. 在细菌作用下,可以用氨气处理含有甲醇(CH3OH)的工业废水,有关反应的化学方程式为5CH3OH+12O2+6NH3═3N2+5X+19H2O,则X的化学式为( )A、NO B、CO2 C、H2 D、CO16. 下列有关碳及其化合物的叙述不正确的是( )A、二氧化碳、一氧化碳均能使紫色石蕊溶液变红 B、一定温度下C和CO均可将氧化铜还原成铜 C、金刚石、石墨完全燃烧均生成二氧化碳 D、石灰石、大理石都可与稀盐酸反应17. 下列化学方程式对应的反应类型均不正确的是( )A、4P+O2═2P2O5 化合反应 B、H2O H2↑+O2↑ 分解反应 C、C+CuO Cu+CO2 置换反应 D、HCl+NaOH═NaCl+H2O 复分解反应18. 下列关于溶液的叙述正确的是( )A、汽油洗衣服上的油污是利用了乳化作用 B、硝酸铵固体溶于水时仅发生扩散吸热的过程 C、某物质的不饱和溶液变为饱和溶液后溶质质量分数可能不变 D、“波尔多液”是无色、透明、均一稳定的混合物19. “关爱生命,拥抱健康”是永恒的主题.下列做法不会损害人体健康的是( )A、用含小苏打的发酵粉焙制糕点 B、用三聚氰胺提高牛奶中蛋白质的含量 C、用NaNO2腌制肉制品 D、“瘦肉精”提高猪的瘦肉率20. 化学时刻影响着我们的生活,它在工农业生产和日常生活中起到了非常重要的作用.下列说法中正确的是( )A、微量元素在人体内的需求量很小,不需要从外界摄取 B、纤维素无法被人体吸收,所以食物中的纤维素对人体毫无意义 C、硫酸铜可用于配制农药波尔多液,但不能用铁桶盛放 D、木炭燃烧的剧烈程度由它的着火点决定,而与氧气的浓度无关21. 液化石油气是一种常用的家庭燃料,泄漏时如果处理不当,常常会酿成悲剧.为了安全起见,最好在厨房安装报警器,如果报警器显示有液化气泄漏,应立即采取的措施是( )
A、赶紧打开厨房中的电灯,找出漏气部位 B、关闭气源阀门,并打开门窗通风 C、迅速跳窗,逃离现场 D、在厨房内及时用手机拨打火警电话22. 苏州的“碧螺春”享誉全国.“碧螺春”茶叶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46 . 下列说法错误的是( )A、单宁酸由碳、氢、氧三种元素组成 B、一个单宁酸分子是由76个碳原子、52个氢原子和46个氧原子构成 C、单宁酸中碳、氧元素的质量比为57:23 D、单宁酸中氢元素的质量分数最小23. 下列有关环保问题的叙述中,错误的是( )A、“绿色化学”是指对环境无负面影响的化学 B、“白色污染”是指白色粉尘等对环境造成的影响 C、“温室气体”主要是指二氧化碳气体 D、“酸雨”是由大气中含硫和氮的污染物导致的24. 有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Y表面有银析出,而Z没有变化.根据以上实验事实,判断这三种金属的活动性由强到弱的顺序是( )A、Z、Y、X B、X、Y、Z C、Y、X、Z D、X、Z、Y25. 除去下列物质中的少量杂质,所选用试剂或方法不正确的是( )选项
物 质
杂 质
试剂或方法
A
KNO3溶液
Ba(NO3)2
Na2SO4溶液
B
CaO固体
CaCO3
高温煅烧
C
KCl固体
MnO2
溶解、过滤、蒸发
D
FeSO4溶液
CuSO4
铁粉、过滤
A、A B、B C、C D、D二、填空题
-
26. 用适当的数字和符号表示:(1)、地壳中含量最多的金属元素与最多的非金属元素组成的化合物 .(2)、3个二氧化氮分子 .(3)、2个铵银离子 .27. 2015年6月5日是世界环境日,我国的主题是“践行绿色生活”,爱护水资源、节约用水是其中重要内容之一.(1)、淡水资源有限,我们需要节约用水.如图中表示节水标志的是(填字母)
 (2)、长期饮用酸碱度过大或硬度过大的水都不利于人体健康,在实验室里可用来测定水的酸碱度;生活中常讲的“烧开水”是指利用的方法,获得可以饮用的水,这样既可以降低水的硬度又可以除去水中的细菌.(3)、下列与自来水的净化过程无关的是 (填序号)A、沉降 B、过滤 C、消毒 D、电解.28. 如图是A、B、C、D四种粒子的结构示意图.据图回答下列问题:
(2)、长期饮用酸碱度过大或硬度过大的水都不利于人体健康,在实验室里可用来测定水的酸碱度;生活中常讲的“烧开水”是指利用的方法,获得可以饮用的水,这样既可以降低水的硬度又可以除去水中的细菌.(3)、下列与自来水的净化过程无关的是 (填序号)A、沉降 B、过滤 C、消毒 D、电解.28. 如图是A、B、C、D四种粒子的结构示意图.据图回答下列问题: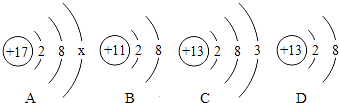 (1)、B粒子属于(填“原子”“阴离子”或“阳离子”),其离子符号为(2)、D与(填序号)属于同种元素(3)、若A为阴离子,则X= .29. 如图为某化学反应的微观过程,其中“
(1)、B粒子属于(填“原子”“阴离子”或“阳离子”),其离子符号为(2)、D与(填序号)属于同种元素(3)、若A为阴离子,则X= .29. 如图为某化学反应的微观过程,其中“ ”和“
”和“  ”表示两种不同的原子.
”表示两种不同的原子.  (1)、该反应中反应物(填“可能”或“不可能”)是氧化物.(2)、图中虚线框内应填的微观图示是(选填A、B、C、D),你推断的依据是
(1)、该反应中反应物(填“可能”或“不可能”)是氧化物.(2)、图中虚线框内应填的微观图示是(选填A、B、C、D),你推断的依据是A.
 B.
B.  C.
C.  D.
D.  30. 铁、铜、银、锌是生活中常见的金属,请根据所学知识回答下列问题.(1)、铜能制成导线,是利用了铜的性.(2)、若要验证Cu、Ag、Fe的活动性强弱,可选择的试剂组是 (填序号)A、Fe、Cu、Ag、稀硫酸 B、Cu、Ag、FeSO4溶液 C、Fe、Ag、CuSO4溶液(3)、将等质量的锌粉和铁粉分别与溶质质量分数相同等质量的稀硫酸充分反应,产生H2的质量与时间的关系如图所示.请回答下列问题:
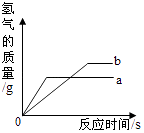
30. 铁、铜、银、锌是生活中常见的金属,请根据所学知识回答下列问题.(1)、铜能制成导线,是利用了铜的性.(2)、若要验证Cu、Ag、Fe的活动性强弱,可选择的试剂组是 (填序号)A、Fe、Cu、Ag、稀硫酸 B、Cu、Ag、FeSO4溶液 C、Fe、Ag、CuSO4溶液(3)、将等质量的锌粉和铁粉分别与溶质质量分数相同等质量的稀硫酸充分反应,产生H2的质量与时间的关系如图所示.请回答下列问题:①表示锌粉与稀硫酸反应的曲线是(填“a”或“b”).
②对于曲线a表示的反应,(填化学式)有剩余.
③若有一种金属有剩余,则剩余的金属一定是填化学式.
 31. 20℃时,分别向盛有10g水的A、B两试管中加入等质量的甲、乙两种固体,充分溶解后,观察到如图1所示现象,图2表示的是甲、乙两种物质的溶解度曲线.
31. 20℃时,分别向盛有10g水的A、B两试管中加入等质量的甲、乙两种固体,充分溶解后,观察到如图1所示现象,图2表示的是甲、乙两种物质的溶解度曲线.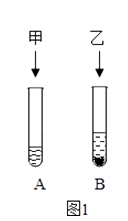 (1)、20℃时,(填“A”或“B”)试管中的溶液一定是饱和溶液;(2)、图2中(填“M”或“N”),表示甲物质的溶解度曲线
(1)、20℃时,(填“A”或“B”)试管中的溶液一定是饱和溶液;(2)、图2中(填“M”或“N”),表示甲物质的溶解度曲线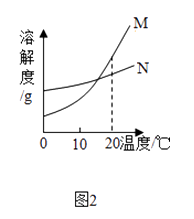 (3)、要使B试管中剩余的固体继续溶解,可采用的方法是(答一种方法即可).(4)、将20℃时M的饱和溶液降温到10℃(假设水不蒸发),其溶质质量分数(填“增大”、“减小”或“不变”).32. 归纳是学习的重要方法,在学习酸、碱、盐后,绘制出如图所示的物质之间的反应关系(图中短线连接的物质表示能相互反应),请填写下列空白:
(3)、要使B试管中剩余的固体继续溶解,可采用的方法是(答一种方法即可).(4)、将20℃时M的饱和溶液降温到10℃(假设水不蒸发),其溶质质量分数(填“增大”、“减小”或“不变”).32. 归纳是学习的重要方法,在学习酸、碱、盐后,绘制出如图所示的物质之间的反应关系(图中短线连接的物质表示能相互反应),请填写下列空白: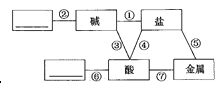 (1)、在图中空白方框中可填写指示剂或(填物质类别).(2)、反应⑦要能发生要求金属必须排在金属活动性顺序表中的前面.(3)、写出一个符合反应④的化学方程式 .(4)、验证反应①,可以选择下列 (填两种物质序号)进行反应.A、Na2SO4 B、KNO3 C、Ba(OH)2 D、NaOH.
(1)、在图中空白方框中可填写指示剂或(填物质类别).(2)、反应⑦要能发生要求金属必须排在金属活动性顺序表中的前面.(3)、写出一个符合反应④的化学方程式 .(4)、验证反应①,可以选择下列 (填两种物质序号)进行反应.A、Na2SO4 B、KNO3 C、Ba(OH)2 D、NaOH.三、实验探究题
-
33. 某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50g 5%的氯化钠溶液.
实验一:如图1是同学们做粗盐提纯实验的操作示意图.

请回答下列问题:
(1)、操作③中用玻璃棒搅拌的作用是 . 操作⑥中的错误是 . 如果⑥中的滤液仍然浑浊,就应该 .(2)、粗盐提纯实验的操作顺序为(填操作序号)、称量精盐并计算产率.(3)、操作④中,当观察到时,停止加热.此操作中玻璃棒的作用是 .(4)、该同学将配好的溶液装入试剂瓶中,请你帮助他在如图2所示的标签内写好标签的内容.(5)、实验二:用提纯得到的精盐配制了50g 5%的氯化钠溶液.经检测,溶质质量分数偏小,其原因可能有(填序号).①氯化钠固体仍然不纯②称量时砝码端忘垫质量相同的纸片.
③量取水时,仰视读数④装瓶时,有少量溶液洒出.
 34. 研究性学习在实验室进行了化学实验,向一盛有镁和铜混合物的烧杯中加入一定量的稀盐酸,充分反应后,观察到烧杯中有固体剩余,对反应后所得溶液中溶质的成分进行探究.(1)、写出上述烧杯中发生反应的化学方程式 .(2)、对反应后所得溶液中溶质的成分进行猜想,请你再补充一种猜想.
34. 研究性学习在实验室进行了化学实验,向一盛有镁和铜混合物的烧杯中加入一定量的稀盐酸,充分反应后,观察到烧杯中有固体剩余,对反应后所得溶液中溶质的成分进行探究.(1)、写出上述烧杯中发生反应的化学方程式 .(2)、对反应后所得溶液中溶质的成分进行猜想,请你再补充一种猜想.【猜想】小光猜想:溶质为氯化镁;
小红猜想:溶质为氯化铜和氯化镁;
你的猜想:溶质为 .
(3)、【讨论】你认为的猜想不合理,理由是 .(4)、【实验】若你的猜想正确,设计一种实验方案证明你的猜想并完成下表:实验步骤
实验现象
实验结论
取少量反应后溶液:
你的猜想正确
(5)、【应用】如果你的猜想正确,把该废液倒入铁质下水管道可能造成的一条危害 .四、计算题
-
35. 根据右图浓盐酸的商标,回答下列问题
 (1)、某研究小组的同学欲用该盐酸配制100g 10%的稀盐酸,需该盐酸g(保留一位小数),配置时应选用(填“10mL”或“50mL”)量筒量取.(2)、小组同学用所配稀盐酸来测量水垢[主要成分为CaCO3和Mg(OH)2]中CaCO3的质量分数:
(1)、某研究小组的同学欲用该盐酸配制100g 10%的稀盐酸,需该盐酸g(保留一位小数),配置时应选用(填“10mL”或“50mL”)量筒量取.(2)、小组同学用所配稀盐酸来测量水垢[主要成分为CaCO3和Mg(OH)2]中CaCO3的质量分数:取10.0g水垢,加入所配100g 10%的稀盐酸中,测得各时间段内生成气体的质量如下表:
时间/min
1
2
3
4
5
气体质量/g
1.5
2.5
3.0
3.3
3.3
通过实验,计算该水垢中CaCO3的质量分数.