2016-2017学年江西省萍乡市高二下学期期末化学试卷
试卷更新日期:2017-08-20 类型:期末考试
一、选择题
-
1. 下列化学用语正确的是( )A、氟化氢的电子式:
 B、氯原子的结构示意图:
B、氯原子的结构示意图:  C、氯化钠的电离方程式:NaCl=Na++Cl﹣
D、乙醇的结构式:C2H6O
2. 糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质.以下叙述中,不正确的是( )A、植物油能使溴的四氯化碳溶液褪色 B、淀粉水解的最终产物是葡萄糖 C、葡萄糖能发生水解反应 D、蛋白质遇硫酸铜溶液后会变性3. 下列物质中最简式相同,但既不是同系物,也不是同分异构体,又不含相同官能团的是( )A、
C、氯化钠的电离方程式:NaCl=Na++Cl﹣
D、乙醇的结构式:C2H6O
2. 糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质.以下叙述中,不正确的是( )A、植物油能使溴的四氯化碳溶液褪色 B、淀粉水解的最终产物是葡萄糖 C、葡萄糖能发生水解反应 D、蛋白质遇硫酸铜溶液后会变性3. 下列物质中最简式相同,但既不是同系物,也不是同分异构体,又不含相同官能团的是( )A、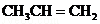 和
和 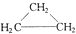 B、乙炔和苯
C、
B、乙炔和苯
C、 和
和 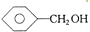 D、甲醛和甲酸甲酯
4. 下列说法中,正确的是( )A、只有醛类物质才能发生银镜反应 B、甲醛、乙醛、丙醛都没有同分异构体 C、将2%的稀氨水逐滴加入2%的AgNO3溶液中,至沉淀恰好溶解为止,可制得银氨溶液 D、将2%的NaOH溶液4~6滴,滴入2mL 10%的CuSO4溶液中制得Cu(OH)2悬浊液,用作检验醛基的试剂5. 美国天文学家在亚利桑那州一天文观察台探测到了银河系中心2.6万光年处一巨大气云中的特殊电磁波,这种电磁波表明那里可能有乙醇醛糖分子存在.下列有关乙醇醛糖(HOCH2CHO)的有关说法正确的( )A、乙醇醛糖是一种有机物,不易溶于水 B、乙醇醛糖能发生取代反应、加成反应、氧化反应以及还原反应 C、乙醇醛糖与甲酸乙酯互为同分异构体 D、1 mol 乙醇醛糖与足量的银氨溶液作用,可析出1 molAg6. 具有显著抗癌活性的10﹣羟基喜树碱的结构如图所示.下列关于10﹣羟基喜树碱的说法正确的是( )
D、甲醛和甲酸甲酯
4. 下列说法中,正确的是( )A、只有醛类物质才能发生银镜反应 B、甲醛、乙醛、丙醛都没有同分异构体 C、将2%的稀氨水逐滴加入2%的AgNO3溶液中,至沉淀恰好溶解为止,可制得银氨溶液 D、将2%的NaOH溶液4~6滴,滴入2mL 10%的CuSO4溶液中制得Cu(OH)2悬浊液,用作检验醛基的试剂5. 美国天文学家在亚利桑那州一天文观察台探测到了银河系中心2.6万光年处一巨大气云中的特殊电磁波,这种电磁波表明那里可能有乙醇醛糖分子存在.下列有关乙醇醛糖(HOCH2CHO)的有关说法正确的( )A、乙醇醛糖是一种有机物,不易溶于水 B、乙醇醛糖能发生取代反应、加成反应、氧化反应以及还原反应 C、乙醇醛糖与甲酸乙酯互为同分异构体 D、1 mol 乙醇醛糖与足量的银氨溶液作用,可析出1 molAg6. 具有显著抗癌活性的10﹣羟基喜树碱的结构如图所示.下列关于10﹣羟基喜树碱的说法正确的是( ) A、分子式为C20H16N2O5 B、不能与FeCl3溶液发生显色反应 C、不能发生酯化反应 D、一定条件下,1mol该物质最多可与1mol NaOH反应7. 苯中可能混有少量的苯酚,下列实验能证明苯中是否混有少量苯酚的是( )
A、分子式为C20H16N2O5 B、不能与FeCl3溶液发生显色反应 C、不能发生酯化反应 D、一定条件下,1mol该物质最多可与1mol NaOH反应7. 苯中可能混有少量的苯酚,下列实验能证明苯中是否混有少量苯酚的是( )①取样品,加入少量高锰酸钾酸性溶液,振荡,看酸性高锰酸钾溶液是否褪色,褪色则有苯酚,不褪色则无苯酚.
②取样品,加入氢氧化钠溶液,振荡,观察样品是否减少.
③取样品,加入过量的浓溴水,观察是否产生白色沉淀,若产生白色沉淀则有苯酚,没有白色沉淀则无苯酚.
④取样品,滴加少量的FeCl3溶液,观察溶液是否显紫色,若显紫色则有苯酚,若不显紫色则无苯酚.
A、③④ B、①③④ C、①④ D、全部8. 已知某有机物C6H12O2能发生水解反应生成A和B,B能氧化成C.若A、C都能发生银镜反应,则C6H12O2符合条件的结构简式有(不考虑立体异构)( )A、3种 B、4种 C、5种 D、6种9. 下列说法正确的是( )A、室温下,在水中的溶解度:丙三醇>苯酚>1﹣氯丁烷 B、用核磁共振氢谱不能区分HCOOCH3和HCOOCH2CH3 C、用Na2CO3溶液不能区分CH3COOH和CH3COOCH2CH3 D、油脂在酸性或碱性条件下均可发生水解反应,且产物相同10. 电解尿素的碱性溶掖可以制取氢气,其装置如图所示(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极).下列有关说法中不正确的是( ) A、电解过穆中b极附近溶液碱性明显增强 B、溶液中的OH﹣逐渐向a极区附近移动 C、若在b极产生标准状况下224mL氢气,则消耗尿素2g D、a极反应式为CO(NH2)2+8OH﹣﹣6e﹣═CO32﹣+N2↑+6H2O11. 有机物A和B只由C、H、O中的两种或三种元素组成,等物质的量的A和B完全燃烧时,消耗相等物质的量的氧气,则A和B的相对分子质量的差值(其中n为正整数)不可能为( )A、0 B、14n C、18n D、44n12. 下列说法正确的是( )A、按系统命名法,化合物
A、电解过穆中b极附近溶液碱性明显增强 B、溶液中的OH﹣逐渐向a极区附近移动 C、若在b极产生标准状况下224mL氢气,则消耗尿素2g D、a极反应式为CO(NH2)2+8OH﹣﹣6e﹣═CO32﹣+N2↑+6H2O11. 有机物A和B只由C、H、O中的两种或三种元素组成,等物质的量的A和B完全燃烧时,消耗相等物质的量的氧气,则A和B的相对分子质量的差值(其中n为正整数)不可能为( )A、0 B、14n C、18n D、44n12. 下列说法正确的是( )A、按系统命名法,化合物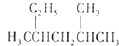 的名称为2﹣甲基﹣4﹣乙基戊烷
B、等质量的甲烷、乙烯、1,3﹣丁二烯分别充分燃烧,所耗用氧气的量依次减少
C、苯酚、水杨酸
的名称为2﹣甲基﹣4﹣乙基戊烷
B、等质量的甲烷、乙烯、1,3﹣丁二烯分别充分燃烧,所耗用氧气的量依次减少
C、苯酚、水杨酸 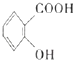 和苯甲酸都是同系物
D、三硝基甲苯的分子式为C7H3N3O6
13. 根据下列实验操作和现象所得结论不正确的是( )
和苯甲酸都是同系物
D、三硝基甲苯的分子式为C7H3N3O6
13. 根据下列实验操作和现象所得结论不正确的是( )选项
实验操作与现象
结论
A
用玻璃棒蘸取某溶液进行焰色反应实验,火焰呈黄色
溶液中含有Na+
B
向浓度均为0.1mol•L﹣1的FeCl3和AlCl3混合溶液中滴加NaOH溶液,出现红褐色沉淀.
Ksp[Fe(OH)3]<Ksp[Al(OH)3]
C
室温下,用pH试纸测得:0.1mol•L﹣1Na2CO3溶液的pH约为11;0.1mol•L﹣1NaHCO3溶液的pH约为8.
HCO3﹣结合H+的能力比CO32﹣的强
D
用Fe3+浓度相同的FeCl3溶液和Fe2(SO4)3溶液,分别清洗做完银镜反应的试管,FeCl3溶液清洗的干净
存在可逆过程:Fe3++Ag⇌Fe2++Ag+ , 且溶解度AgCl<Ag2SO4
A、A B、B C、C D、D14. 酯类物质广泛存在于香蕉、梨等水果中.某实验小组先从梨中分离出一种酯,然后将分离出的酯水解,得到了乙酸和另一种化学式为C6H13OH的物质.对于此过程,以下分析中不正确的是( )A、C6H13OH分子含有羟基 B、C6H13OH可与金属钠发生反应 C、实验小组分离出的酯可表示为CH3COOC6H13 D、不需要催化剂,这种酯在水中加热即可大量水解15. 下列关于苯的叙述正确的是( ) A、反应①为取代反应,有机产物与水混合浮在上层 B、反应②为氧化反应,反应现象是火焰明亮并带有浓烟 C、反应③为取代反应,有机产物是一种烃 D、反应④中1 mol苯最多与3 mol H2发生加成反应,是因为苯分子含有三个碳碳双键16. 常温下,HNO2的电离平衡常数为K=4.6×10﹣4(已知 =2.14),向20mL0.01mol•L﹣1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )
A、反应①为取代反应,有机产物与水混合浮在上层 B、反应②为氧化反应,反应现象是火焰明亮并带有浓烟 C、反应③为取代反应,有机产物是一种烃 D、反应④中1 mol苯最多与3 mol H2发生加成反应,是因为苯分子含有三个碳碳双键16. 常温下,HNO2的电离平衡常数为K=4.6×10﹣4(已知 =2.14),向20mL0.01mol•L﹣1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )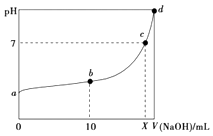 A、HNO2的电离方程式为HNO2=NO2﹣+H+ B、a点H2O电离出的c(H+)=2.14×10﹣3mol•L﹣1 C、b点溶液中离子浓度大小关系为c(NO2﹣)>c(Na+)>c(H+)>c(OH﹣) D、X值等于20
A、HNO2的电离方程式为HNO2=NO2﹣+H+ B、a点H2O电离出的c(H+)=2.14×10﹣3mol•L﹣1 C、b点溶液中离子浓度大小关系为c(NO2﹣)>c(Na+)>c(H+)>c(OH﹣) D、X值等于20二、填空题
-
17. 有机物A常用于食品行业.已知9.0g A在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2 .(1)、A分子的质谱图如图所示,从图中可知其相对分子质量是90,则A的分子式是 .
 (2)、A能与NaHCO3溶液发生反应,A一定含有的官能团名称是 .(3)、A分子的核磁共振氢谱有4个峰,峰面积之比是1:1:1:3,则A的结构简式是 .(4)、0.1mol A与足量Na反应,在标准状况下产生H2的体积是L.(5)、A在一定条件下可聚合得到一种聚酯,用于制造手术缝合线,其反应的化学方程式是 .18. 联苄(
(2)、A能与NaHCO3溶液发生反应,A一定含有的官能团名称是 .(3)、A分子的核磁共振氢谱有4个峰,峰面积之比是1:1:1:3,则A的结构简式是 .(4)、0.1mol A与足量Na反应,在标准状况下产生H2的体积是L.(5)、A在一定条件下可聚合得到一种聚酯,用于制造手术缝合线,其反应的化学方程式是 .18. 联苄( )是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为: (1)、催化剂的制备:图1是实验室制取少量无水AlCl3的相关实验装置的仪器和药品:
)是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为: (1)、催化剂的制备:图1是实验室制取少量无水AlCl3的相关实验装置的仪器和药品:
①将上述仪器连接成一套制备并保存无水AlCl3的装置,各管口标号连接顺序为:d接e,接 , 接 , 接 .
②有人建议将上述装置中D去掉,其余装置和试剂不变,也能制备无水AlCl3 . 你认为这样做是否可行(填“可行”或“不可行”),你的理由是 .
③装置A中隐藏着一种安全隐患,请提出一种改进方案: .
(2)、联苄的制备联苄的制取原理为:

反应最佳条件为n(苯):n(1,2﹣二氯乙烷)=10:1,反应温度在60﹣65℃之间.实验室制取联苄的装置如图2所示(加热和加持仪器略去):

实验步骤:
在三口烧瓶中加入120.0mL苯和适量无水AlCl3 , 由滴液漏斗滴加10.7mL1,2﹣二氯乙烷,控制反应温度在60﹣65℃,反应约60min.将反应后的混合物依次用稀盐酸、2%Na2CO3溶液和H2O洗涤分离,在所得产物中加入少量无水MgSO4固体,静止、过滤,先常压蒸馏,再减压蒸馏收集170~172℃的馏分,得联苄18.2g.
相关物理常数和物理性质如下表
名称
相对分子质量
密度/(g•cm﹣3)
熔点/℃
沸点/℃
溶解性
苯
78
0.88
5.5
80.1
难溶水,易溶乙醇
1,2一二氯乙烷
99
1.27
﹣35.3
83.5
难溶水,可溶苯
无水氯化铝
133.5
2.44
190
178(升华)
遇水水解,微溶苯
联苄
182
0.98
52
284
难溶水,易溶苯
④仪器a的名称为 , 和普通分液漏斗相比,使用滴液漏斗的优点是 .
⑤洗涤操作中,水洗的目的是;无水硫酸镁的作用是 .
⑥常压蒸馏时,最低控制温度是 .
⑦该实验的产率约为 . (小数点后保留两位有效数字)
19. 聚戊二酸丙二醇(PPG)是一种可降解的聚脂类高分子材料,在材料的生物相容性方面有限好的应用前景.PPG的一种合成路线如下: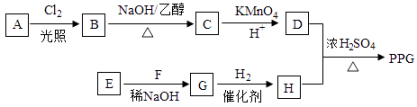
已知;
①烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢
②化合物B为单氯代烃;化合物C的分子式为C5H8
③E、F为相对分子质量差14的同系物,F是福尔马琳的溶质
④R1CHO+R2CH2CHO
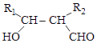
回答下列问题:
(1)、A的结构简式为 .(2)、由B生成C的化学方程式为 .(3)、由E和F生成G的反应类型为 , E的化学名称为 .(4)、由D和H生成PPG的化学方程式为;(5)、D的同分异构体能同时满足下列条件的共有种(不含立体异构);①能与饱和NaHCO3溶液反应产生液体
②既能发生银镜反应,又能发生水解反应,其中核磁共振请谱显示为3组峰,且峰面积比为6:1:1的是有(写结构简式)
20. 火力发电厂释放出的大量NONOx、SO2、CO2会对环境造成污染.对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现节能减排、废物利用等目的.(1)、脱硝:利用甲烷催化还原NOx;CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=﹣574kJ•mol﹣1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=﹣1160kJ•mol﹣1
甲烷直接将NO2还原为N2的热化学方程式为 .
(2)、脱硫:①某种脱硫工艺将废气处理后可获得硫酸铵和硝酸铵,物质的量浓度相等的硫酸铵溶液和硝酸铵溶液,前者的c(NH4+)与后者的c(NH4+)的关系是 .A.大于2倍 B.等于2倍 C.介于2倍与2倍之间 D.小于1倍
②25℃时pH均为4的硝酸铵溶液和稀硝酸中由水电离出的氢离子浓度分别为c1、c2 , 则c1与c2的比值等于 .
(3)、脱碳:废气中的CO2转化为甲醇(CH3OH)可用于制作甲醇燃料电池(结构如图),质子交换膜左右两侧的溶液均为1L2mol•L﹣1H2SO4溶液.电极c上发生的电极反应式为 , 当电池中有1mole﹣发生转移时左右两侧溶液的质量之差为g (假设反应物a、b耗尽,忽略气体的溶解).