2016-2017学年江西省南昌市三校联考高二下学期期末化学试卷
试卷更新日期:2017-08-20 类型:期末考试
一、选择题
-
1. 15g A物质和10.5g B物质完全反应,生成7.2g C物质,1.8g D物质和0.3mol E物质,则E物质的摩尔质量是( )A、100g/mol B、100g C、55g/mol D、55g2. 下列数量的各物质所含原子个数由大到小顺序排列的是( )
①0.5mol氨气 ②4g氦气 ③4℃时9mL水 ④0.2mol磷酸钠.
A、④③②① B、①④③② C、②③④① D、①④②③3. 试分析有机物下列性质中该有机物不具有的是:( )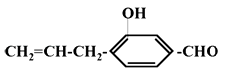 ;(1)加聚反应(2)加成反应 (3)使酸性高锰酸钾溶液褪色(4)与NaHCO3溶液反应放出CO2气体 (5)与KOH溶液反应.A、(1)(3) B、(2)(4) C、(4) D、(4)(5)4. 烯烃被酸性高锰酸钾溶液氧化的规律是,双键两端的基团=CH2变成CO2 , =CHR变成RCOOH,
;(1)加聚反应(2)加成反应 (3)使酸性高锰酸钾溶液褪色(4)与NaHCO3溶液反应放出CO2气体 (5)与KOH溶液反应.A、(1)(3) B、(2)(4) C、(4) D、(4)(5)4. 烯烃被酸性高锰酸钾溶液氧化的规律是,双键两端的基团=CH2变成CO2 , =CHR变成RCOOH,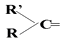 变成
变成 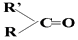 ,现有某溴代烷A,分子式为C4H9Br,在NaOH醇溶液中加热得到有机物B,B被酸性高锰酸钾溶液氧化后不可能得到的产物是( ) A、只有CH3COOH B、CO2和 CH3COCH3 C、CO2和CH3CH2COOH D、HCOOH和CH3CH2COOH5. 同温同压下,x g甲气体和y g乙气体占有相同的体积,根据阿伏加德罗定律判断,x:y的值可以表示( )A、甲与乙的物质的量之比 B、等质量的甲与乙的分子个数之比 C、同温同压下,甲与乙的密度之比 D、同温同体积下,等质量的甲与乙的压强之比6. 可以用来鉴别己烯、甲苯、乙酸乙酯、苯酚溶液的一组试剂是( )A、氯化铁溶液 溴水 B、碳酸钠溶液 溴水 C、酸性高锰酸钾溶液 溴水 D、酸性高锰酸钾溶液 氯化铁溶液7. 中草药秦皮中含有的七叶树内酯 (环上氢原子未标出,每个折点表示一个碳原子),具有抗菌作用.若1mol七叶树内酯分别跟浓溴水和NaOH溶液完全反应,则消耗的溴和NaOH的物质的量分别为( )
,现有某溴代烷A,分子式为C4H9Br,在NaOH醇溶液中加热得到有机物B,B被酸性高锰酸钾溶液氧化后不可能得到的产物是( ) A、只有CH3COOH B、CO2和 CH3COCH3 C、CO2和CH3CH2COOH D、HCOOH和CH3CH2COOH5. 同温同压下,x g甲气体和y g乙气体占有相同的体积,根据阿伏加德罗定律判断,x:y的值可以表示( )A、甲与乙的物质的量之比 B、等质量的甲与乙的分子个数之比 C、同温同压下,甲与乙的密度之比 D、同温同体积下,等质量的甲与乙的压强之比6. 可以用来鉴别己烯、甲苯、乙酸乙酯、苯酚溶液的一组试剂是( )A、氯化铁溶液 溴水 B、碳酸钠溶液 溴水 C、酸性高锰酸钾溶液 溴水 D、酸性高锰酸钾溶液 氯化铁溶液7. 中草药秦皮中含有的七叶树内酯 (环上氢原子未标出,每个折点表示一个碳原子),具有抗菌作用.若1mol七叶树内酯分别跟浓溴水和NaOH溶液完全反应,则消耗的溴和NaOH的物质的量分别为( ) A、3mol,2mol B、3mol,4mol C、2mol,3mol D、4mol,4mol8. 下列条件下,两瓶气体所含原子数一定相等的是( )A、同质量、不同密度的N2和CO B、同温度、同体积的N2和H2 C、同体积、同密度的C2H4和CH4 D、同压强、同体积的N2O和CO29. 设NA为阿伏加德罗常数的值,标准状况下某O2和N2的混合气体mg含有b个分子,则ng该混合气体在相同状况下所占的体积应是( )A、 L B、 C、 D、 L10. 等质量的下列各烃完全燃烧时,消耗氧气最多的是( )A、CH4 B、C2H6 C、C3H6 D、C6H611. 下列各有机物的名称肯定错误的是( )A、3﹣甲基﹣2﹣戊烯 B、3﹣甲基﹣2﹣丁烯 C、2,2﹣二甲基丙烷 D、3﹣甲基﹣1﹣丁烯12. 与100mL0.1mol/L AlCl3溶液中Cl﹣的物质的量浓度相等的是( )A、50mL0.1mol/L NaCl溶液 B、50mL0.15mol/L MgCl2溶液 C、10mL1.0mol/L FeCl3溶液 D、100mL0.3mol/L KClO3溶液13. 以下物质:(1)甲烷(2)苯(3)聚乙烯(4)聚乙炔(5)2丁炔(6)环己烷(7)邻二甲苯(8)苯乙烯.既能使KMnO4酸性溶液褪色,又能使溴水因发生化学反应而褪色的是( )A、(3)(4)(5)(8) B、(4)(5)(7)(8) C、(4)(5)(8) D、(3)(4)(5)(7)(8)14. 下列说法不正确的是( )A、麦芽糖及其水解产物均能发生银镜反应 B、在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH C、用溴水即可鉴别苯酚溶液、2,4﹣已二烯和甲苯 D、用甘氨酸(H2N﹣CH2﹣COOH)和丙氨酸(
A、3mol,2mol B、3mol,4mol C、2mol,3mol D、4mol,4mol8. 下列条件下,两瓶气体所含原子数一定相等的是( )A、同质量、不同密度的N2和CO B、同温度、同体积的N2和H2 C、同体积、同密度的C2H4和CH4 D、同压强、同体积的N2O和CO29. 设NA为阿伏加德罗常数的值,标准状况下某O2和N2的混合气体mg含有b个分子,则ng该混合气体在相同状况下所占的体积应是( )A、 L B、 C、 D、 L10. 等质量的下列各烃完全燃烧时,消耗氧气最多的是( )A、CH4 B、C2H6 C、C3H6 D、C6H611. 下列各有机物的名称肯定错误的是( )A、3﹣甲基﹣2﹣戊烯 B、3﹣甲基﹣2﹣丁烯 C、2,2﹣二甲基丙烷 D、3﹣甲基﹣1﹣丁烯12. 与100mL0.1mol/L AlCl3溶液中Cl﹣的物质的量浓度相等的是( )A、50mL0.1mol/L NaCl溶液 B、50mL0.15mol/L MgCl2溶液 C、10mL1.0mol/L FeCl3溶液 D、100mL0.3mol/L KClO3溶液13. 以下物质:(1)甲烷(2)苯(3)聚乙烯(4)聚乙炔(5)2丁炔(6)环己烷(7)邻二甲苯(8)苯乙烯.既能使KMnO4酸性溶液褪色,又能使溴水因发生化学反应而褪色的是( )A、(3)(4)(5)(8) B、(4)(5)(7)(8) C、(4)(5)(8) D、(3)(4)(5)(7)(8)14. 下列说法不正确的是( )A、麦芽糖及其水解产物均能发生银镜反应 B、在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH C、用溴水即可鉴别苯酚溶液、2,4﹣已二烯和甲苯 D、用甘氨酸(H2N﹣CH2﹣COOH)和丙氨酸( )缩合最多可形成4种二肽
15. 乙烯雌酚是一种激素类药物,结构如图,下列有关叙述不正确的是( )
)缩合最多可形成4种二肽
15. 乙烯雌酚是一种激素类药物,结构如图,下列有关叙述不正确的是( )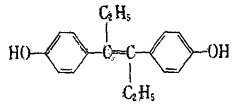 A、它易溶于有机溶剂 B、1mol该有机物最多消耗NaOH和Na2CO3的物质的量均为2mol C、1mol该有机物可以与5mol Br2发生反应 D、该有机物分子中,最多有14个碳原子共平面16. V mL硫酸铝溶液中,含Al3+m g,取V/4mL该溶液稀释到4VmL,则稀释后溶液中SO42﹣的物质的量浓度为( )A、125m/9V mol/L B、125m/18 V mol/L C、125 m/36V mol/L D、125 m/54V mol/L
A、它易溶于有机溶剂 B、1mol该有机物最多消耗NaOH和Na2CO3的物质的量均为2mol C、1mol该有机物可以与5mol Br2发生反应 D、该有机物分子中,最多有14个碳原子共平面16. V mL硫酸铝溶液中,含Al3+m g,取V/4mL该溶液稀释到4VmL,则稀释后溶液中SO42﹣的物质的量浓度为( )A、125m/9V mol/L B、125m/18 V mol/L C、125 m/36V mol/L D、125 m/54V mol/L二、填空题
-
17. 请给下列有机物用系统命名法命名
 18. 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
18. 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
(1)、该浓盐酸的物质的量浓度为mol/L.(2)、取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是 .A、溶液中HCl的物质的量 B、溶液的浓度 C、溶液中Cl﹣的数目 D、溶液的密度(3)、某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.3mol/L稀盐酸.①该学生需要量取 mL上述浓盐酸进行配制.
②配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次);
A.用30mL水洗涤烧杯2﹣3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量水(约30mL)的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1﹣2cm处
③在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏高”或“偏低”或“无影响”).
I、用量筒量取浓盐酸时俯视观察凹液面
II、用量筒量取浓盐酸后,洗涤量筒2~3次,洗涤液也转移到容量瓶
III、溶液注入容量瓶前没有恢复到室温就进行定容
(4)、若在标准状况下,将V LHCl气体溶于1L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为 mol/L.(填字母)A、 B、 C、 D、(5)、现将100mL 0.5mol/L的盐酸与200mL 0.1mol/LCuCl2溶液混合,体积变化忽略不计,所得溶液中Cl﹣的物质的量浓度是 .
19. 以乙烯为初始反应物可制得正丁醇(CH3CH2CH2CH2OH)已知两个醛分子在一定条件下可以自身加成.下式中反应的中间产物(Ⅲ)可看成是由(Ⅰ)中的碳氧双键打开,分别跟(Ⅱ)中的2﹣位碳原子和2﹣位氢原子相连而得.(Ⅲ)是一种3﹣羟基醛,此醛不稳定,受热即脱水而生成不饱和醛(烯醛):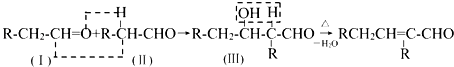
请运用已学过的知识和上述给出的信息写出由乙烯制正丁醇各步反应的化学方程式(不必写出反应条件).
三、计算题
-
20. 液态化合物在一定量的氧气中恰好完全燃烧,反应方程式为:XY2(l)+3O2(g)=XO2(g)+2YO2(g)冷却后,在标准状况下测得生成物的体积是672mL,密度是2.56g/L.(1)、反应前O2的体积为 .(2)、化合物XY2的摩尔质量是 .(3)、在XY2分子中,X、Y两元素的质量之比为3:16,则X、Y两元素分别为和(写元素名称).21. 0.2mol有机物和0.4mol O2在密闭容器中燃烧后的产物为CO2、CO和H2O(g).产物经过浓硫酸后,浓硫酸的质量增加10.8g;再通过灼热CuO充分反应后,固体质量减轻3.2g;最后气体再通过碱石灰被完全吸收,碱石灰质量增加17.6g.(1)、通过计算推断该有机物的化学式.(2)、若0.2mol该有机物恰好与4.6g金属钠完全反应,试确定该有机物的结构简式.