2017年上海市宝山区高考化学二模试卷
试卷更新日期:2017-08-16 类型:高考模拟
一、选择题
-
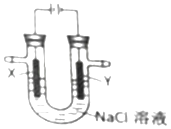
1. 甲状腺大的病人需要多吃海带,这是因为海带中含有较多的( )A、氯元素 B、钠元素 C、碘元素 D、铁元素2. 酸雨的pH值是( )A、<7 B、<6.5 C、<6 D、<5.63. 属于工业固氮的是( )A、N2与O2反应生成NO B、由NH3转变成 NH4HCO3 C、N2与H2在一定条件下反应生成NH3 D、豆科植物的根瘤吸收氮4. 有关HF和HCl判断正确的是( )A、键长:HF>HCl B、键能:HF>HCl C、稳定性:HCl>HF D、共用电子对偏移程度:HCl>HF5. 不能用来鉴别乙醛、乙酸的试剂是( )A、水 B、石蕊试液 C、银氨溶液 D、新制的氢氧化铜溶液6. 将两种互不相溶的液体分离的方法是( )A、分液 B、结晶 C、纸层析 D、过滤7. 按照有机物的命名规则,下列命名正确的是( )A、1,2﹣二甲基戊烷 B、2﹣乙基丁烷 C、3﹣乙基己烷 D、3,4﹣二甲基戊烷8. 下列试剂中,可以鉴别二氧化碳和二氧化硫的是( )A、澄清石灰水 B、品红溶液 C、湿润的蓝色石蕊试纸 D、硝酸银溶液9. 某老师批阅学生实验报告,下列哪些学生是以科学的态度记录实验数据的( )A、甲学生用电子天平称取NaOH固体1.220g B、乙学生用广泛pH试纸测定溶液的酸碱性:pH=14.5 C、丙学生用碱式滴定管取25.0mL0.1mol/L的盐酸 D、丁学生用50mL 量筒量取46.70mL浓盐酸10. 下列事实与盐类水解无关的是( )A、氯化铝溶液蒸干后灼烧得不到无水氯化铝 B、氯化铁溶液常用作制印刷电路板的腐蚀剂 C、常用热的纯碱溶液除去油污 D、长期施用硫酸铵易使土壤酸化11. 下列物质的工业生产原理不涉及氧化还原反应的是( )A、氨气 B、纯碱 C、硫酸 D、烧碱12. 用如图所示装置电解氯化钠溶液(X、Y 是碳棒).下列判断正确的是( )
 A、X电极为阴极 B、Y电极为负极 C、X电极表面发生氧化反应 D、Y电极表面有氯气生成13. 在密闭容器中,反应2SO2(g)+O2(g)=2SO3(g) 达到平衡后,若将容器体积缩小一半,对反应产生的影响是( )A、V(正)减小,V(逆)增大 B、V(正)增大,V(逆)减小 C、V(正)、V(逆)都减小 D、V(正)、V(逆)都增大14. 布洛芬片常用来减轻感冒症状,其结构简式如图,下列有关说法错误的是( )
A、X电极为阴极 B、Y电极为负极 C、X电极表面发生氧化反应 D、Y电极表面有氯气生成13. 在密闭容器中,反应2SO2(g)+O2(g)=2SO3(g) 达到平衡后,若将容器体积缩小一半,对反应产生的影响是( )A、V(正)减小,V(逆)增大 B、V(正)增大,V(逆)减小 C、V(正)、V(逆)都减小 D、V(正)、V(逆)都增大14. 布洛芬片常用来减轻感冒症状,其结构简式如图,下列有关说法错误的是( ) A、布洛芬的分子式为C13H18O2 B、布洛芬与苯乙酸是同系物 C、1mol 布洛芬最多能与3mol 氢气发生加成反应 D、布洛芬在苯环上发生取代反应,其一氯代物有4种15. 配制一定物质的量浓度的Na2CO3溶液时,下下列因素会导致溶液浓度偏高的是( )A、溶解时有少量液体溅出 B、洗涤液未全部转移到容量瓶中 C、容量瓶使用前未干燥 D、定容时液面未到刻度线16. 下列溶液中氢离子浓度最小的是( )A、10L0.10mol/LCH3COOH 溶液 B、2L 0.05mol/L H2SO4溶液 C、1L0.10mol/LHNO3溶液 D、2L0.1mol/LHCl溶液17. 等量的铁粉分别与足量的盐酸、水蒸气在一定的条件下充分反应,则在相同的条件下,产生氢气的物质的量之比是( )A、1:1 B、3:4 C、2:3 D、4:318. 25℃时,将10mL质量分数为50%(密度1.4g/mL)的硫酸稀释成100mL,下列说法正确的是( )A、纯硫酸的摩尔质量为98 B、上述100mL稀硫酸中含溶质14g C、上述稀释过程所需要的蒸馏水为90mL D、质量分数为50%的硫酸物质的量浓度为7.14mol/L19. 溶质都为1mol的NaHCO3溶液和Ba(OH)2溶液混合,能完整表示该反应的离子方程式是( )A、CO32﹣+Ba2+=BaCO3 B、HCO3﹣+OH﹣→H2O+CO32﹣ C、HCO3﹣+Ba2++OH﹣→H2O+BaCO3 D、2HCO3﹣+Ba2++OH﹣=BaCO3+2H2O+CO32﹣20. 工业上常用NaHSO3处理含Cr2O72﹣的废液,反应的离子方程式为:5H++Cr2O72﹣+3HSO3﹣→2Cr3++3SO42﹣+4H2O
A、布洛芬的分子式为C13H18O2 B、布洛芬与苯乙酸是同系物 C、1mol 布洛芬最多能与3mol 氢气发生加成反应 D、布洛芬在苯环上发生取代反应,其一氯代物有4种15. 配制一定物质的量浓度的Na2CO3溶液时,下下列因素会导致溶液浓度偏高的是( )A、溶解时有少量液体溅出 B、洗涤液未全部转移到容量瓶中 C、容量瓶使用前未干燥 D、定容时液面未到刻度线16. 下列溶液中氢离子浓度最小的是( )A、10L0.10mol/LCH3COOH 溶液 B、2L 0.05mol/L H2SO4溶液 C、1L0.10mol/LHNO3溶液 D、2L0.1mol/LHCl溶液17. 等量的铁粉分别与足量的盐酸、水蒸气在一定的条件下充分反应,则在相同的条件下,产生氢气的物质的量之比是( )A、1:1 B、3:4 C、2:3 D、4:318. 25℃时,将10mL质量分数为50%(密度1.4g/mL)的硫酸稀释成100mL,下列说法正确的是( )A、纯硫酸的摩尔质量为98 B、上述100mL稀硫酸中含溶质14g C、上述稀释过程所需要的蒸馏水为90mL D、质量分数为50%的硫酸物质的量浓度为7.14mol/L19. 溶质都为1mol的NaHCO3溶液和Ba(OH)2溶液混合,能完整表示该反应的离子方程式是( )A、CO32﹣+Ba2+=BaCO3 B、HCO3﹣+OH﹣→H2O+CO32﹣ C、HCO3﹣+Ba2++OH﹣→H2O+BaCO3 D、2HCO3﹣+Ba2++OH﹣=BaCO3+2H2O+CO32﹣20. 工业上常用NaHSO3处理含Cr2O72﹣的废液,反应的离子方程式为:5H++Cr2O72﹣+3HSO3﹣→2Cr3++3SO42﹣+4H2O下列判断错误的是( )
A、氧化产物是SO42﹣ B、氧化剂与还原剂的物质的量之比是1:3 C、Cr2O72﹣表现了氧化性 D、还原1molCr2O72﹣ , 电子转移3mol二、综合题
-
21. 表为元素周期表的一部分:
IA
IIA
IIIA
IVA
VA
VIA
VIIA
二
C
N
①
三
②
③
④
P
⑤
⑥
请填写下列空白:
(1)、表中元素,原子半径最大的是(填写元素符号);①的核外电子排布式;③和⑥两元素形成化合物的电子式为 .(2)、②③④三种元素最高价氧化物对应的水化物中,碱性最强的是(填化学式).(3)、比较④、⑤两种元素的简单离子半径:>(填离子符号);元素④最高价氧化物对应的水化物与硝酸反应的离子方程式为 .(4)、列举一个事实来证明元素①比元素⑤的非金属性强 .(5)、若8g甲烷气体完全燃烧生成液态水时放出445.15kJ的热量,请写出其热化学方程式 .22. 氮的单质及其化合物性质多样,用途广泛.完成下列填空.
(1)、科学家正在研究利用催化技术将超音速飞机尾气中的NO和CO转变成CO2和N2:2NO+2CO 2CO2+N2+Q(Q>0)某温度下测得该反应在不同时间的CO浓度如表:
时间(s)
浓度(mol/L)
0
1
2
3
4
5
c(CO)
3.60×10﹣3
3.05×10﹣3
2.85×10﹣3
2.75×10﹣3
2.70×10﹣3
2.70×10﹣3
该反应平衡常数K的表达式为;温度升高,K值(选填“增大”、“减小”、“不变”);前2s内的平均反应速率v(N2)=;若上述反应在密闭容器中发生,达到平衡时能提高NO转化率的措施之一是 .
(2)、工业合成氨的反应温度选择500℃左右的原因是 .(3)、实验室在固定容积的密闭容器中加入1mol氮气和3mol氢气模拟工业合成氨,反应在一定条件下已达到平衡的标志是 .a.N2、H2、NH3的浓度之比为1:3:2
b.容器内的压强保持不变
c.N2、H2、NH3的浓度不再发生变化
d.反应停止,正、逆反应的速率都等于零
(4)、常温下向含1mol溶质的稀盐酸中缓缓通入1mol NH3(溶液体积变化忽略不计),反应结束后溶液中离子浓度由大到小的顺序是;在通入NH3的过程中溶液的导电能力(选填“变大”、“变小”、“几乎不变”).23. 乙烯是一种重要的化工原料,以乙烯为原料生产部分化工产品的反应如图(部分反应条件已略去):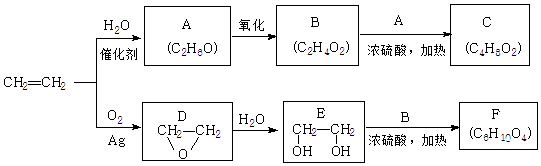
请回答下列问题:
(1)、A的名称是 , 含有的官能团名称是 , 实验室由A转化为乙烯的反应条件为 .(2)、B和A反应生成C的化学方程式为 , 该反应的类型为 .(3)、F的结构简式为 .(4)、写出D的同分异构体的结构简式 .(5)、乙炔也是常见的一种化工原料,它可以制取很多化工产品,例如:聚氯乙烯塑料.写出由乙炔合成聚氯乙烯的合成路线.(合成路线常用的表示方式为:A B… 目标产物)24. 孔雀石主要含Cu2(OH)2CO3 , 以及少量Fe、Si的化合物.可以用孔雀石为原料制备胆矾(CuSO4•5H2O),步骤如图:
请回答下列问题:
(1)、试剂①是一种常见的酸,写出其化学式 . 过滤所需要的玻璃仪器有(2)、实验室检验Fe3+的常用方法是 .(3)、溶液A中的金属离子有Cu2+、Fe2+、Fe3+ , 上述流程中需要用试剂②将溶液A中的Fe2+全部转化为Fe3+ , 从而形成溶液B,则试剂②能否用氯水(填“能”或“不能”,若“不能”,请解释原因).(4)、由溶液C获得胆矾,需要经过、、过滤等操作.(5)、取25.00mL溶液A,用1.000×10﹣2mol/LKMnO4标准溶液滴定.反应离子方程式为:5Fe2++MnO4﹣+8H+→5Fe3++Mn2++4H2O,若消耗标准溶液20.00mL,则溶液A中Fe2+的浓度为 .