2017年山东省德州市庆云县中考化学一模试卷
试卷更新日期:2017-08-15 类型:中考模拟
一、选择题
-
1. 2016年世界环境日主题为“改善环境质量 推动绿色发展”旨在动员大家从身边小事做起,共同履行环保责任,共建美丽家园.你认为下列做法不符合这一主题的是( )A、大力推广使用脱硫煤 B、提倡使用农家肥,合理使用化肥农药 C、垃圾分类处理,回收利用 D、工业废水压入地下,严禁直接排入河流2. 根据如图的信息判断,下列关于铝的说法正确的是( )
 A、氧化铝的化学式是AlO B、铝的原子核内有13个中子 C、铝的相对原子质量是26.982 D、在化学反应中,铝原子易失去电子形成Al+33. 下列图示的实验操作不正确的是( )A、给液体加热
A、氧化铝的化学式是AlO B、铝的原子核内有13个中子 C、铝的相对原子质量是26.982 D、在化学反应中,铝原子易失去电子形成Al+33. 下列图示的实验操作不正确的是( )A、给液体加热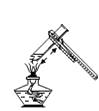 B、测溶液的pH
B、测溶液的pH 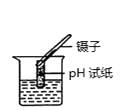 C、稀释浓硫酸
C、稀释浓硫酸 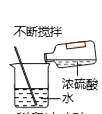 D、蒸发食盐水
D、蒸发食盐水  4. 推理是化学学习中常用的思维方法,下列说法正确的是( )A、稀有气体的性质不活泼,氖气是稀有气体,所以氖气的性质也不活泼 B、碳酸盐都能与盐酸反应生成无色气体,所以与盐酸反应生成无色气体的都是碳酸盐 C、中和反应生成盐和水,所以生成盐和水的反应都是中和反应 D、水能灭火,所以发生火灾都可以用水来灭火5. 将CO、CO2、HCl、H2O(气)和N2的混合气体依次通过足量的下列物质:①饱和氢氧化钠溶液 ②浓硫酸 ③灼热的氧化铜粉末(假设每步都充分反应),最后剩余气体是( )A、N2、CO2、H2O B、N2 C、N2、HCl D、N2、CO26. 将过量的稀硫酸加入到有生锈铁钉的试管中,不能观察到的现象是( )
4. 推理是化学学习中常用的思维方法,下列说法正确的是( )A、稀有气体的性质不活泼,氖气是稀有气体,所以氖气的性质也不活泼 B、碳酸盐都能与盐酸反应生成无色气体,所以与盐酸反应生成无色气体的都是碳酸盐 C、中和反应生成盐和水,所以生成盐和水的反应都是中和反应 D、水能灭火,所以发生火灾都可以用水来灭火5. 将CO、CO2、HCl、H2O(气)和N2的混合气体依次通过足量的下列物质:①饱和氢氧化钠溶液 ②浓硫酸 ③灼热的氧化铜粉末(假设每步都充分反应),最后剩余气体是( )A、N2、CO2、H2O B、N2 C、N2、HCl D、N2、CO26. 将过量的稀硫酸加入到有生锈铁钉的试管中,不能观察到的现象是( ) A、铁钉表面的锈迹消失,逐渐变得光亮 B、溶液由无色变为黄色,又由黄色变为浅绿色 C、一段时间后,铁钉表面有气泡生成 D、试管底部有红褐色沉淀生成7. 下列是日常生活中的一些事实,其中解释正确的是( )A、体温计中水银柱的升降﹣汞原子体积受热增大,遇冷减小 B、汽油比水更容易去除油污﹣汽油具有乳化作用 C、木桩埋入地下前先要将表面烧焦﹣碳在常温下的化学性质稳定 D、“人要实,火要虚”﹣木柴架空能够提高空气中氧气的含量8. 下列能正确反映相关实验过程中量的变化关系的图象是( )A、
A、铁钉表面的锈迹消失,逐渐变得光亮 B、溶液由无色变为黄色,又由黄色变为浅绿色 C、一段时间后,铁钉表面有气泡生成 D、试管底部有红褐色沉淀生成7. 下列是日常生活中的一些事实,其中解释正确的是( )A、体温计中水银柱的升降﹣汞原子体积受热增大,遇冷减小 B、汽油比水更容易去除油污﹣汽油具有乳化作用 C、木桩埋入地下前先要将表面烧焦﹣碳在常温下的化学性质稳定 D、“人要实,火要虚”﹣木柴架空能够提高空气中氧气的含量8. 下列能正确反映相关实验过程中量的变化关系的图象是( )A、 向氢氧化钠溶液中滴加足量的水
B、
向氢氧化钠溶液中滴加足量的水
B、 向硫酸和硫酸铜的混合溶液中滴加过量的氢氧化钠溶液
C、
向硫酸和硫酸铜的混合溶液中滴加过量的氢氧化钠溶液
C、 等质量的金属分别放入到足量的稀盐酸中
D、
等质量的金属分别放入到足量的稀盐酸中
D、 两份等体积的5%过氧化氢溶液
两份等体积的5%过氧化氢溶液
二、理解与应用
-
9. 化学与我们的生产、生活有着密切的联系,利用所学的化学知识可以帮助我们解决许多日常中的问题(1)、老年人定期补钙可以预防(填一种常见病症);(2)、油锅着火,迅速向锅内放入蔬菜灭火的理由是 .(3)、用熟石灰处理含硫酸的污水的化学方程式是 .(4)、农田中的作物植株矮小,叶片发黄,可建议施用下列肥料的 (填序号).A、NH4HCO3 B、Ca3(PO4)2 C、K2SO4 D、KNO3 .10. 如表是某物质在不同温度时的溶解度,请回答下列问题
温度/℃
0
20
40
60
80
100
溶解度/g
13.3
31.6
63.8
110
169
246
 (1)、分析表中数据,归纳处该物质的溶解度随温度变化的规律是 .(2)、20℃时,在装有12g该物质晶体的试管中,加入10g水并充分振荡,此时所得溶液为(选填“饱和”或“不饱和”)溶液,再将该试管放入盛有热水的烧杯中,使试管内溶液温度升至60℃,此时试管中的溶液的质量为克;(3)、20℃时,该物质水溶液的溶质质量分数最大是(精确到1%).11. 组成相似的盐具有一些相似的化学性质(1)、Cu(NO3)2溶液和CuSO4溶液中都含有的离子是(填离子符号)(2)、向Cu(NO3)2溶液中加入NaOH溶液,充分振荡,反应的化学方程式为;(3)、向CuSO4溶液中加入过量的锌片,充分反应后,可看到的现象是 , 如图表示该反应前后溶液中存在的主要离子:请写出每种图形代表的离子
(1)、分析表中数据,归纳处该物质的溶解度随温度变化的规律是 .(2)、20℃时,在装有12g该物质晶体的试管中,加入10g水并充分振荡,此时所得溶液为(选填“饱和”或“不饱和”)溶液,再将该试管放入盛有热水的烧杯中,使试管内溶液温度升至60℃,此时试管中的溶液的质量为克;(3)、20℃时,该物质水溶液的溶质质量分数最大是(精确到1%).11. 组成相似的盐具有一些相似的化学性质(1)、Cu(NO3)2溶液和CuSO4溶液中都含有的离子是(填离子符号)(2)、向Cu(NO3)2溶液中加入NaOH溶液,充分振荡,反应的化学方程式为;(3)、向CuSO4溶液中加入过量的锌片,充分反应后,可看到的现象是 , 如图表示该反应前后溶液中存在的主要离子:请写出每种图形代表的离子 ;
;  ;
;  . (填离子符号):
. (填离子符号):  12. 二氧化碳与氢氧化钠溶液作用没有明显的现象,某同学设计了如图所示的实验装置(A、B是气球)
12. 二氧化碳与氢氧化钠溶液作用没有明显的现象,某同学设计了如图所示的实验装置(A、B是气球) (1)、若该装置气密性良好,则将氢氧化钠溶液滴入锥形瓶中可观察到的现象是 , 产生此现象的原因是 .(2)、氯气(Cl2)是一种有刺激性气味,有毒的气体,氯气可与水反应:Cl2+H2O═HCl+HClO(次氯酸).若将锥形瓶中的CO2气体换成氯气,也可产生上述现象,试写出氯气与氢氧化钠溶液发生反应的化学方程式 .(3)、若想使装置中产生的现象与(1)中的现象相反,则胶头滴管和锥形瓶中应分别装入的药品是(写出一组即可) .
(1)、若该装置气密性良好,则将氢氧化钠溶液滴入锥形瓶中可观察到的现象是 , 产生此现象的原因是 .(2)、氯气(Cl2)是一种有刺激性气味,有毒的气体,氯气可与水反应:Cl2+H2O═HCl+HClO(次氯酸).若将锥形瓶中的CO2气体换成氯气,也可产生上述现象,试写出氯气与氢氧化钠溶液发生反应的化学方程式 .(3)、若想使装置中产生的现象与(1)中的现象相反,则胶头滴管和锥形瓶中应分别装入的药品是(写出一组即可) .三、实验与探究
-
13. 如图是实验室制取气体的常用仪器,回答下列问题
 (1)、标号为d的仪器名称是 .(2)、实验室用氯酸钾制取氧气,并用排水法收集.
(1)、标号为d的仪器名称是 .(2)、实验室用氯酸钾制取氧气,并用排水法收集.①该反应的化学方程式是;
②组装制取装置时,需选择如图中的仪器有(填序号);
(3)、实验室制取二氧化碳并检验:①收集二氧化碳时通常只用向上排空气法,其中的原因是 .
②将二氧化碳通入澄清的石灰水,反应的化学方程式是 .
14. 实验室有失去标签的四瓶无色溶液,分别为Ca(OH)、NaCO、稀盐酸、NaCl溶液中的一种,为鉴别它们,现将这四瓶无色溶液分别标号为A、B、C、D,化学兴趣小组的同学对此进行了探究【提出问题】A,B,C,D分别是什么溶液?
【实验药品】失去标签的四瓶溶液和无色酚酞试液
【实验仪器】试管、胶头滴管、烧杯等.
(1)、【收集证据】实验操作
实验现象
实验结论
①取四种溶液各少量于试管中,然后A与B、C与D溶液两两混合
A、B混合产生大量气泡,C,D混合无明显现象
A、B分别是溶液中的一种.
C,D分别是溶液中的一种
②取四种溶液各少量于试管中,然后A与C,B与D溶液两两混合
A、C混合产生白色沉淀,B,D混合无明显现象
A为溶液;C为溶液;由此区分出B、D溶液
(2)、【反思与体会】鉴别物质的关键是利用物质间反应出现的明显现象进行判断.【继续探究】
将四种溶液各少量倒入一洁净的烧杯中,再滴入几滴无色酚酞试液,充分反应静置后发现,烧杯底部有白色沉淀,上层清液为无色.则上层清液中一定含有的溶质是(指示剂除外),可能含有的溶质是为验证可能含有的溶质是否存在,应补充的实验设计是 .
四、计算题
-
15. 为测定某市售碳酸钙药品中碳酸钙的质量分数(杂质为SiO2 , 与稀盐酸不反应),某同学的方法是:将样品与稀盐酸反应,测定反应后生成的CO2质量,再根据CO2的质量求出样品中碳酸钙的质量,从而计算出样品中碳酸钙的质量分数.为测定生成CO2的质量,他设计了如下实验方案(已知:无水氯化钙是常见的干燥剂):

①按图组装好装置,检查装置气密性后,在分液漏斗中加入过量稀盐酸,并在干燥管中加入适量无水氯化钙样品,称得装置和药品的总质量为564.57g;
②在广口瓶中加入碳酸钙样品,称得装置和药品的总质量为574.57g;
③旋紧橡皮塞,打开分液漏斗旋塞,向广口瓶中滴加稀盐酸,使样品与稀盐酸完全反应;
④反应结束后,称得装置及装置内所有物质的总质量为570.57g
请根据上述实验回答下列问题:
(1)、该方案测得样品中碳酸钙的质量分数是多少(写出解题过程,计算结果精确到0.1%)?(2)、该实验中用稀盐酸与碳酸钙样品反应,而不用浓盐酸与碳酸钙样品反应,其原因是 . 若实验中不用无水氯化钙干燥,则测得样品中碳酸钙的质量分数与上述实验计算结果相比(选填“偏小”或“不变”或“偏大”).