2020年中考科学一轮复习15.物质科学-构成物质的粒子 元素
试卷更新日期:2020-02-21 类型:一轮复习
一、单选题
-
1. 思维导图有助于建构知识,如图是小金建立的有关物质宏观组成和微观构成的思维导图,其中“▲”应填入的是( )
 A、原子 B、中子 C、电子 D、质子2. 某品牌的纯牛奶的包装盒上标有:每100毫升中含钠58毫克、钙120毫克,这里的钠、钙是指( )A、元素 B、单质 C、原子 D、离子3. 最新科技报道,夏威夷联合天文中心的科学家在宇宙深处发现H3+离子和H3分子,以下关于它们的说法不正确的是( )A、H3+和H3都是构成物质的微粒 B、H3是单质 C、一个H3+中含有3个电子 D、一个H3中含有3个质子4. 如图为物质、元素及构成微粒的相互关系图,下列说法中不正确的是()
A、原子 B、中子 C、电子 D、质子2. 某品牌的纯牛奶的包装盒上标有:每100毫升中含钠58毫克、钙120毫克,这里的钠、钙是指( )A、元素 B、单质 C、原子 D、离子3. 最新科技报道,夏威夷联合天文中心的科学家在宇宙深处发现H3+离子和H3分子,以下关于它们的说法不正确的是( )A、H3+和H3都是构成物质的微粒 B、H3是单质 C、一个H3+中含有3个电子 D、一个H3中含有3个质子4. 如图为物质、元素及构成微粒的相互关系图,下列说法中不正确的是() A、a为分子,b为元素,c为离子 B、由图可知,分子、原子、离子都是构成物质的微粒 C、原子失去电子可形成阳离子,原子得到电子可形成阴离子 D、不同种元素的两种离子,质子数一定不相同,电子数也一定不相同5. 如图是四位同学对某一物质的化学式意义的描述( )
A、a为分子,b为元素,c为离子 B、由图可知,分子、原子、离子都是构成物质的微粒 C、原子失去电子可形成阳离子,原子得到电子可形成阴离子 D、不同种元素的两种离子,质子数一定不相同,电子数也一定不相同5. 如图是四位同学对某一物质的化学式意义的描述( ) A、C B、O3 C、SO2 D、NH36. 为庆祝元素周期表诞生 150 周年,联合国将 2019 年定为国际化学元素周期表年。如图是元素周期表的一部分,对相关信息叙述正确的是( )
A、C B、O3 C、SO2 D、NH36. 为庆祝元素周期表诞生 150 周年,联合国将 2019 年定为国际化学元素周期表年。如图是元素周期表的一部分,对相关信息叙述正确的是( ) A、碳原子的相对原子质量是 12.01g B、铝原子的核内中子数一定为 13 C、碳、铝、硅三种元素都属于非金属元素 D、铝元素和硅元素位于元素周期表的同一周期7. 如图是118号元素在元素周期表中的相关信息。下列有关该元素的说法正确的是( )
A、碳原子的相对原子质量是 12.01g B、铝原子的核内中子数一定为 13 C、碳、铝、硅三种元素都属于非金属元素 D、铝元素和硅元素位于元素周期表的同一周期7. 如图是118号元素在元素周期表中的相关信息。下列有关该元素的说法正确的是( )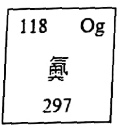 A、元素符号为Og B、该原子的电子数为179 C、该原子的中子数为118 D、相对原子质量为297克8. 硼是作物生长必需的微量营养元素,硼元素的相关信息如图所示。下列有关硼的说法正确的是( )
A、元素符号为Og B、该原子的电子数为179 C、该原子的中子数为118 D、相对原子质量为297克8. 硼是作物生长必需的微量营养元素,硼元素的相关信息如图所示。下列有关硼的说法正确的是( ) A、相对原子质量是10.81g B、属于金属元素 C、原子的核电荷数为5 D、原子核外有6个电子9. 科学世界里没有生命的阿拉伯数字也变得鲜活起来,它们在不同的位置表示着不同的含义。下列化学符号中数字“2”表示的意义正确的是( )A、Mg2+:一个镁离子带2个单位正电荷 B、CO2:二氧化碳中含有2个氧原子 C、2H:2个氢元素 D、 :氧化钙的化合价为+2价10. 通过化学式“H2O”可以获取的信息错误的是 ( )A、水这种物质 B、一个水分子 C、水分子是由氢、氧两种元素组成 D、一个水分子是由两个氢原子和一个氧原子构成11. 在科学世界里没有生命的阿拉伯数字也变得鲜活起来,它们在不同的位置表示着不同的含义。
A、相对原子质量是10.81g B、属于金属元素 C、原子的核电荷数为5 D、原子核外有6个电子9. 科学世界里没有生命的阿拉伯数字也变得鲜活起来,它们在不同的位置表示着不同的含义。下列化学符号中数字“2”表示的意义正确的是( )A、Mg2+:一个镁离子带2个单位正电荷 B、CO2:二氧化碳中含有2个氧原子 C、2H:2个氢元素 D、 :氧化钙的化合价为+2价10. 通过化学式“H2O”可以获取的信息错误的是 ( )A、水这种物质 B、一个水分子 C、水分子是由氢、氧两种元素组成 D、一个水分子是由两个氢原子和一个氧原子构成11. 在科学世界里没有生命的阿拉伯数字也变得鲜活起来,它们在不同的位置表示着不同的含义。①Mg2+:一个镁离子带2个单位正电荷;②CO2:二氧化碳中含有2个氧原子;③2H:2个氢原子;④ :氧化钙中钙的化合价为+2价;⑤6C:表示一个碳原子中有6个中子;⑥55Mn:表示锰元素是第55号元素。其中正确的是( )
A、①②③ B、②③⑥ C、③④⑤ D、①③④12. 有两种元素X和Y,它们化合成两种化合物A和B,化合物A中X所占质量分数为75%,化合物B中X占80%。已知A的化学式为XY4 , 则B的化学式为( )A、XY2 B、XY3 C、X2Y3 D、X3Y2二、填空题
-
13. 写出下列物质的化学式。(1)、熟石灰:(2)、石灰石:(3)、纯碱:(4)、胆矾:14. 原子、分子、离子都是构成物质的微观离子。在氮气、水、汞、氯化钠、铁,这五种物质中,由原子构成的物质是 , 由分子构成的物质是。15.(1)、用化学符号表示:
①3个二氧化碳分子;②氧化铁;③4个硫酸根离子;
(2)、指出化学符号中“2”的含义:H2O;Mg2+16. 元素周期表是学习科学的重要工具。下表是元素周期表的一部分,请回答下列问题。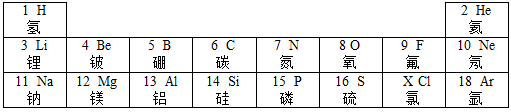 (1)、不同种元素之间最本质的区别是________不同。A、相对原子质量 B、质子数 C、中子数(2)、第3号元素属于(选填“金属”或“非金属”)元素。(3)、第12号元素和第17号元素组成化合物的化学式是。17. 用元素符号表示:(1)、氩气(2)、一个亚铁离子(3)、两个铵根离子18. 物质的用途总是与它的性质密切相关。请从下列物质中选取合适的物质填入空格内:盐酸、醋酸、碳铵、硝酸钾。长期使用铁锅炒菜,可有效减少缺铁性贫血症的发生,为了提高补铁效果,在炒菜时可加入适量的;为了使植物茎杆粗壮,农业上通常施用的化肥是(请写化学式)。19. 我国用新技术提纯了稀有金属铼(Re),为航空航天发动机核心部件的制造提供了原料。科学家早在1994年在俄罗斯择捉岛上的库德里亚维火山上发现了,该火山每年都向外以二硫化铼的形式最少喷出20公斤铼。
(1)、不同种元素之间最本质的区别是________不同。A、相对原子质量 B、质子数 C、中子数(2)、第3号元素属于(选填“金属”或“非金属”)元素。(3)、第12号元素和第17号元素组成化合物的化学式是。17. 用元素符号表示:(1)、氩气(2)、一个亚铁离子(3)、两个铵根离子18. 物质的用途总是与它的性质密切相关。请从下列物质中选取合适的物质填入空格内:盐酸、醋酸、碳铵、硝酸钾。长期使用铁锅炒菜,可有效减少缺铁性贫血症的发生,为了提高补铁效果,在炒菜时可加入适量的;为了使植物茎杆粗壮,农业上通常施用的化肥是(请写化学式)。19. 我国用新技术提纯了稀有金属铼(Re),为航空航天发动机核心部件的制造提供了原料。科学家早在1994年在俄罗斯择捉岛上的库德里亚维火山上发现了,该火山每年都向外以二硫化铼的形式最少喷出20公斤铼。
(1)、请写出二硫化铼的化学式;(2)、高铼酸钠(NaReO4)也是铢的重要来源之一,高铼酸钠中铼元素的化合价为。三、解答题
-
20. 伟大的科学家费曼说:“假如只允许把人类的科学史压缩成一句话,它就会是:一切东西都是由原子构成”。人类在探索物质是由什么构成的历史长河中,充满了智慧。(1)、1803年,近代化学之父,英国科学家道尔顿(Dalton J)在前人研究的基础上,提出“道尔顿原子论”:一切物质都由原子构成,原子很小、呈圆球状、不可再分……但由于受当时实验条件限制,道尔顿无法用事实证明自己的观点。
1811年,意大利化学家阿伏加德罗提出:有些物质也是由分子构成,原子的基本工作形式是分子。
1897年,汤姆森通过实验发现了电子,进一步发展了原子、分子论。汤姆森主要是纠正了“道尔顿原子论”中的观点。
1911年,卢瑟福又通过实验,推测原子是由和核外电子构成,并提出了沿用至今的现代原子结构理论。
(2)、道尔顿的原子论,不是事实的归纳,而是思维的产物,体现了直觉和想象在科学创造中的作用。在科学研究中,像汤姆森和卢瑟福这样,对实验现象进行解释的过程叫做。原子是一种看不见、摸不着的微粒,为了帮助人们理解原子的结构,这三位科学家都运用了来表达他们的理论成果。