山东省济宁2019-2020学年九年级上学期化学12月月考试卷
试卷更新日期:2020-02-17 类型:月考试卷
一、单选题
-
1. 我国古代下列古代发明或技术中,主要原理涉及化学变化的是( )A、矿石炼铁 B、水车灌溉 C、活字印刷 D、雕刻石像2. 从分子、原子角度对下面一些現象和变化的解释,合理的是( )A、花香四溢 分子很小,质量也很小 B、热胀冷缩 温度变化,分子或原子大小发生变化 C、滴水成冰 温度降低,分子间隔变小、停止运动 D、食品变质 分子发生变化,分子性质发生变化3. 用pH计测得一些物质的pH如下:
物质
苹果汁
西瓜汁
牛奶
鸡蛋清
炉具清洁剂
pH
2.9
5.8
6.4
7.6
12.5
下列说法正确的是( )
A、牛奶放置一段时间后变酸,pH变大 B、等量的西瓜汁比苹果汁所含氢离子数多 C、炉具清洁剂的碱性比鸡蛋清的碱性强 D、胃酸过多的人应该多喝苹果汁4. 下列有关实验现象的描述不正确的是()A、红磷在空气中燃烧,产生大量白烟 B、硫在氧气中燃烧,发出明亮的蓝紫色火焰 C、木炭在氧气中燃烧,发出白光,生成二氧化碳 D、铁在氧气中剧烈燃绕,火星四射,生成黑色固体5. 下列说法中正确的是()①分子、原子、离子都是构成物质的基本粒子
②缓慢氧化是进行的很缓慢,不会发光、放热的氧化反应
③凡是两种或两种以上物质发生的反应都是化合反应
④氧化反应不一定都是化合反应,化合反应也不一定都是氧化反应
A、①②③ B、①② C、②④ D、①④6. 下图是物质X溶于水中发生解离的微观示意图,其中能说明X是一种酸的是( )A、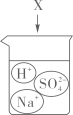 B、
B、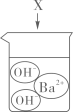 C、
C、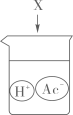 D、
D、 7. 能用于实验室制取CO2 , 并能随开随用、随关随停的装置是( )A、
7. 能用于实验室制取CO2 , 并能随开随用、随关随停的装置是( )A、 B、
B、 C、
C、 D、
D、 8. 某无色溶液X是稀盐酸、稀硫酸、NaOH溶液、Na2CO3溶液中的一种,取三份等质量的X溶液,向其中分別加入酚酞试液、Fe2O3粉末、BaCl2溶液,产生的现象如下表所述.根据现象判断,无色溶液X是( )
8. 某无色溶液X是稀盐酸、稀硫酸、NaOH溶液、Na2CO3溶液中的一种,取三份等质量的X溶液,向其中分別加入酚酞试液、Fe2O3粉末、BaCl2溶液,产生的现象如下表所述.根据现象判断,无色溶液X是( )加入的物质
酚酞试液
Fe2O3粉末
BaCl2溶液
实验现象
无明显现象
固体逐渐溶解,溶液变黄
无明现象
A、稀盐酸 B、稀硫酸 C、NaOH溶液 D、Na2CO3溶液9. 某同学对下列四个实验都设计了两种方案,其中第二方案比第一方案更方便合理的是()A
B
C
D
实验要求
除去二氧化碳中少量的氧气
清洗金属表面 油污
检验氧气是否集满
区分硬水和蒸馏水
第一方案
通过灼热炭粉
用洗洁精洗涤
带火星的木条放在瓶口
加入肥皂水
第二方案
通过灼热铜丝网
用水洗涤
点燃的木条伸入瓶内
蒸发结晶
A、A B、B C、C D、D10. 某有机物在9.6g氧气中恰好完全燃烧,生成8.8gCO2 和5.4gH2O. 下列说法正确的是()A、该有机物只含碳、氢两种元素 B、该有机物中一定含有碳、氢元素 C、该有机物中一定含有碳、氢、氧三种元素 D、无法确定二、填空题
-
11. 甘肃优秀学子、华东师范大学姜雪峰教授被国际纯粹与应用化学联合会遴选为“全球青年化学家元素周期表硫元素代表”。硫元素在元素周期表中的信息如图1所示,硫原子的结构示意图如图2所示:
 (1)、图2中x的数值是;(2)、硫元素和钠元素可形成硫化钠,其化学式为。(3)、用符合题意的化学用语表示下列加点部分的含义。
(1)、图2中x的数值是;(2)、硫元素和钠元素可形成硫化钠,其化学式为。(3)、用符合题意的化学用语表示下列加点部分的含义。①构成某硫单质的分子中含有8个硫原子;
②硫原子与氧原子结合形成的硫酸根离子。
12. 从H、C、N、 O、Na、S、 K七种元素中,选取有关的元素,用适当化学用语填空:(1)、不含电子的离子;(2)、含有10个电子的分子;(3)、溶于水后溶液温度升高的化合物;(4)、含两个根的化合物。13. 久置的苛性钠溶液易发生变质,这是由于它与发生了反应,反应的化学方程式为;如果要检验苛性钠溶液是否变质,可取出少量溶液于试管,向其中滴加足量稀硝酸,若有产 生,则证明已经变质。此反应的化学方程式。14. 20世纪20年代,就有人预言可能存在由4个氧原子构成的新型分子(O4),但一直没有得到证实。最近意大利一所大学的科学家使用普通氧分子和带正电荷的氧离子制造出这种新型氧分子,并用质谱仪器探测到了它的存在。下列叙述中正确的是(____)A、O2和O4的性质完全相同 B、一个O4分子中含有2个O2分子 C、O4是一种新型化合物 D、O2和O4混合形成的是混合物 E、O2和O4是两种不同的单质 F、合成O4的过程是化学变化三、科普阅读题
-
15. 钠的化学性质非常活泼,直到1807 年才由英国化学家戴维通过电解氢氧化钠得到单质金属钠。实验室通常金属钠保存在煤油或液体石蜡中,仍然会发生缓慢的氧化。请回答下列问题:(1)、写出金属钠发生缓慢氧化反应的化学方程式;(2)、探究金属钠与水反应时,发现有气体生成,收集气体并点燃,有明显爆鸣声:向反应后的溶液中滴加酚酞试剂,溶液呈红色。由此推断:钠与水反应的化学方程式为;(3)、根据金属活动性顺序推测:金属钠放入硫酸铜溶液中,溶液底部应出现金属铜的红色沉积物:经实验证明,实际观察到的是蓝色沉淀[Cu(OH)2]和一种盐。产生蓝色沉淀的原因是;(用化学方程式解释)。 如果往蓝色沉淀里加入稀盐酸,沉淀又消失了,用化学方程式表示发生这个现象的原因。
四、综合题
-
16. (一)下图所示为实验室中常见的气体制备和收集装置.

请回答下列问题:
(1)、实验室用高锰酸钾制取氧气,应选用的发生装置是(填字母序号)。若用装置B制取二氧化碳,反应的原理是(用化学方程式表示)。(2)、实验室用H2O2溶液和MnO2制取氧气,若选用C做发生装置,你认为选用C的优点是。(3)、欲使用装置E用排空气法收集二氧化碳,则气体应从(填“a”或“b”)端通入:欲使用装置E.用排水法收集氧气,先将瓶中装满水,再将气体从(填“a”或“b”)端通入。(4)、已知一氧化氮气体难落于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中装置(填字母序号)。(5)、(二)小红同学进行酸碱中和反应的实验(如图所示)。她向氢氧化钠溶液中滴加一定量稀盐酸后,想起氢氧化钠溶液中事先没有滴加指示剂,为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,井向试管中滴加几滴无色酚酞试液,振荡,观察到试管中溶液颜色没有变化。于是她对烧杯中的溶液进行了以下探究:小红认为此时烧杯中的溶液可能有以下三种情况:
①盐酸与氢氧化钠恰好完全反应:②氢氧化钠有剩余:③盐酸过量。
小明同学却断定不可能“氢氧化钠有剩余”,他的理由是:。
(6)、他们共同设计了一个实验方案,欲对上述其他两种可能情况进行验证。请根据相关内容填写如表:实验方法
可能观察到的现象
结论
将少量锌粒放入试管中,然后从烧杯中取适量溶液至试管中。
如果。
则盐酸过量
如果。
则盐酸与氢氧化钠恰好完全反应
(7)、经过讨论,他们认为利用下列几种物质代替锌粒,也可以达到验证目的。你认为其中不正确的是_____。(填序号).A、生锈的铁钉 B、碳酸钠粉末 C、硫酸钠粉末 D、氢氧化铜(8)、如图曲线能够表示小红所做试验中溶液pH变化趋势的是(填序号)。
五、计算题
-
17. 钙是人体必须的常量元素,每日必须摄入足够量的钙。 目前市场上的补钙药剂很多,如图是某种品牌的补钙药品的部分说明书。请回答下列问题:
 (1)、如果按用量服用,每天摄入钙元素的质量为。(2)、若每片钙片的质量为lg.则钙片中钙元素的质量分数为。18. 长期使用的热水锅炉会产生水垢。水垢主要成分是碳酸钙和氢氧化镁。某兴趣小组为了测定水垢中CaCO3的含量,将6g水垢粉碎放在烧杯中,然后向其中加入40g某浓度的稀盐酸,使之充分反应(水垢中除碳酸钙和氢氧化镁外都不与稀盐酸反应)。实验数据记录如下:
(1)、如果按用量服用,每天摄入钙元素的质量为。(2)、若每片钙片的质量为lg.则钙片中钙元素的质量分数为。18. 长期使用的热水锅炉会产生水垢。水垢主要成分是碳酸钙和氢氧化镁。某兴趣小组为了测定水垢中CaCO3的含量,将6g水垢粉碎放在烧杯中,然后向其中加入40g某浓度的稀盐酸,使之充分反应(水垢中除碳酸钙和氢氧化镁外都不与稀盐酸反应)。实验数据记录如下:反应时间/min
0
1
2
3
4
5
6
7
8
烧杯内所盛物
质的总质量/g
46.0
45.2
44.8
45.1
44.1
43.9
43.8
43.8
43.8
试计算:
(1)、表中有一数据是不合理的,该数据的测得时间是第min;(2)、水垢中CaCO3的质量分数(计算结果精确至0.1%)。
-
-