江苏省2020年普通高中学业水平合格性考试试题
试卷更新日期:2020-02-10 类型:水平会考
一、选择题:
-
1. 为充分利用资源和保护环境,近年来逐步实施了生活垃圾的分类处理。废弃的塑料袋、纸张、橡胶制品均属于( )A、单质 B、有机物 C、盐 D、氧化物2. 许多化学物质在日常生活中有俗名。下列物质的俗名与化学式对应正确的是( )A、双氧水—Na2O2 B、小苏打—NaOH C、胆矾—Cu(OH)2 D、干冰—CO23. 下图仪器中名称为圆底烧瓶的是( )A、
 B、
B、 C、
C、 D、
D、 4. 标准状况下,1 mol O2的体积约为( )A、5.6 L B、11.2 L C、22.4 L D、33.6 L5. 实验室有少量汞不慎撒落,处理方法是将硫黄粉撒在汞的表面,发生反应的化学方程式为Hg + S = HgS,该反应属于( )A、置换反应 B、化合反应 C、分解反应 D、复分解反应6. 大米是中国人的主食之一,其中含量最高的营养物质是淀粉。淀粉属于( )A、糖类 B、油脂 C、蛋白质 D、无机盐7. 下列变化属于化学变化的是( )A、金属腐蚀 B、碘的升华 C、氨气液化 D、矿石粉碎8. 下列物质含有离子键的是( )A、CO2 B、N2 C、KCl D、H2O9. 海水中蕴藏着丰富的化学资源,每千克海水中氯化物的含量如下图所示,其中物质的量浓度最大的金属离子是( )
4. 标准状况下,1 mol O2的体积约为( )A、5.6 L B、11.2 L C、22.4 L D、33.6 L5. 实验室有少量汞不慎撒落,处理方法是将硫黄粉撒在汞的表面,发生反应的化学方程式为Hg + S = HgS,该反应属于( )A、置换反应 B、化合反应 C、分解反应 D、复分解反应6. 大米是中国人的主食之一,其中含量最高的营养物质是淀粉。淀粉属于( )A、糖类 B、油脂 C、蛋白质 D、无机盐7. 下列变化属于化学变化的是( )A、金属腐蚀 B、碘的升华 C、氨气液化 D、矿石粉碎8. 下列物质含有离子键的是( )A、CO2 B、N2 C、KCl D、H2O9. 海水中蕴藏着丰富的化学资源,每千克海水中氯化物的含量如下图所示,其中物质的量浓度最大的金属离子是( )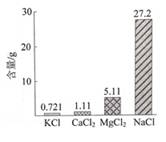 A、K+ B、Ca2+ C、Mg2+ D、Na+10. 下列化学用语表示正确的是( )A、苯的结构简式:C6H6 B、氢分子的电子式:H:H C、氧原子的结构示意图:
A、K+ B、Ca2+ C、Mg2+ D、Na+10. 下列化学用语表示正确的是( )A、苯的结构简式:C6H6 B、氢分子的电子式:H:H C、氧原子的结构示意图: D、硝酸钾的电离方程式:KNO3= K++ N5++ 3O2-
11. 反应4Al + 3MnO2 3Mn + 2Al2O3可用来制取Mn,下列有关该反应的说法正确的是( )A、Al是还原剂 B、MnO2发生氧化反应 C、Al的化合价降低 D、MnO2中O被还原12. 规范操作是实验的基本要求。下列操作规范的是( )A、
D、硝酸钾的电离方程式:KNO3= K++ N5++ 3O2-
11. 反应4Al + 3MnO2 3Mn + 2Al2O3可用来制取Mn,下列有关该反应的说法正确的是( )A、Al是还原剂 B、MnO2发生氧化反应 C、Al的化合价降低 D、MnO2中O被还原12. 规范操作是实验的基本要求。下列操作规范的是( )A、 转移溶液
B、
转移溶液
B、 搅拌溶液
C、
搅拌溶液
C、 熄灭酒精灯
D、
熄灭酒精灯
D、 取蒸发皿
13. 下列实验方案能达到目的的是( )A、用排水集气法收集HCl气体 B、用燃烧的木条检验N2和CO2 C、用KSCN溶液检验溶液中的Fe3+ D、用丁达尔效应鉴别Na2CO3溶液和NaHCO3溶液14. 在含有大量的H+、Ag+、NO3-的溶液中,还可能大量共存的离子是( )A、CO32- B、OH- C、Cl- D、Na+15. 下列反应中,不能用离子方程式H++ OH-= H2O来表示的是( )A、CH3COOH + NH3·H2O = CH3COONH4 + H2O B、H2SO4 + 2KOH = K2SO4 + 2H2O C、HNO3 + NaOH = NaNO3 + H2O D、HCl + NaOH = NaCl + H2O16. 碳原子成键的多样性、同分异构现象等是有机化合物种类繁多的原因。丁烷和2-甲基丙烷的结构式如下图所示:
取蒸发皿
13. 下列实验方案能达到目的的是( )A、用排水集气法收集HCl气体 B、用燃烧的木条检验N2和CO2 C、用KSCN溶液检验溶液中的Fe3+ D、用丁达尔效应鉴别Na2CO3溶液和NaHCO3溶液14. 在含有大量的H+、Ag+、NO3-的溶液中,还可能大量共存的离子是( )A、CO32- B、OH- C、Cl- D、Na+15. 下列反应中,不能用离子方程式H++ OH-= H2O来表示的是( )A、CH3COOH + NH3·H2O = CH3COONH4 + H2O B、H2SO4 + 2KOH = K2SO4 + 2H2O C、HNO3 + NaOH = NaNO3 + H2O D、HCl + NaOH = NaCl + H2O16. 碳原子成键的多样性、同分异构现象等是有机化合物种类繁多的原因。丁烷和2-甲基丙烷的结构式如下图所示:
下列关于上述两种物质的说法正确的是( )
A、分子式不同 B、碳氢键(C-H)数目不同 C、互为同分异构体 D、物理性质、化学性质完全相同17. 食醋中约含有3% ~5% 的乙酸(CH3COOH)。下列有关乙酸的叙述正确的是( )A、摩尔质量为60 g·mol-1 B、无色无味的液体 C、难溶于水 D、酸性比碳酸弱18. 下列有机反应的化学方程式正确的是( )A、CH2 = CH2 + Br2 → CH3—CHBr2 B、C2H4 + 3O2 2CO2 + 2H2O
C、CH3CH2OH + Na → CH3CH2Na + H2O
D、CH3CH2OH + CH3COOH CH3COOCH2CH3
19. 下列过程需要吸收热量的是( )A、甲烷在空气中燃烧 B、稀释浓硫酸 C、镁条与盐酸反应 D、冰融化成水20. 反应2NO + 2CO N2 + 2CO2可应用于汽车尾气的净化,下列关于该反应的说法正确的是( )A、升高温度能减慢反应速率 B、减小CO浓度能加快反应速率 C、使用恰当的催化剂能加快反应速率 D、达到化学平衡时,NO能100%转化为产物21. 某同学用如图所示装置探究原电池的工作原理,并推出下列结论,其中不正确的是( )
2CO2 + 2H2O
C、CH3CH2OH + Na → CH3CH2Na + H2O
D、CH3CH2OH + CH3COOH CH3COOCH2CH3
19. 下列过程需要吸收热量的是( )A、甲烷在空气中燃烧 B、稀释浓硫酸 C、镁条与盐酸反应 D、冰融化成水20. 反应2NO + 2CO N2 + 2CO2可应用于汽车尾气的净化,下列关于该反应的说法正确的是( )A、升高温度能减慢反应速率 B、减小CO浓度能加快反应速率 C、使用恰当的催化剂能加快反应速率 D、达到化学平衡时,NO能100%转化为产物21. 某同学用如图所示装置探究原电池的工作原理,并推出下列结论,其中不正确的是( ) A、锌片不断溶解,说明Zn失去电子 B、铜片上产生气泡,说明溶液中H+在其表面得到电子 C、电流计指针发生偏转,说明该装置将电能转换为化学能 D、该装置中发生的总反应为Zn + H2SO4 = ZnSO4 + H2↑22. 请阅读下列材料,回答问题。
A、锌片不断溶解,说明Zn失去电子 B、铜片上产生气泡,说明溶液中H+在其表面得到电子 C、电流计指针发生偏转,说明该装置将电能转换为化学能 D、该装置中发生的总反应为Zn + H2SO4 = ZnSO4 + H2↑22. 请阅读下列材料,回答问题。联合国将2019年定为“国际化学元素周期表年”,以纪念门捷列夫发现元素周期律150周年。元素周期律把元素及其化合物纳入一个统一的理论体系,为系统研究元素及其化合物提供了科学方法,为发现和探索新元素、新物质提供了有效思路。
(1)、为纪念门捷列夫,科学家将1955年人工合成的一种新元素用符号“Md”表示,中文命名为“钔”。核素 Md的质量数为( )A、101 B、157 C、258 D、359(2)、Mg和Si都属于元素周期表第3周期元素,它们原子结构中相同的是( )A、质子数 B、电子层数 C、核外电子数 D、最外层电子数(3)、判断Cl的非金属性比S的强,可依据的事实是( )A、HCl的热稳定性比H2S的强 B、氯气能溶于水,硫难溶于水 C、常温下,氯单质呈气态,硫单质呈固态 D、AgCl是白色固体,Ag2S是黑色固体(4)、锂是第2周期ⅠA族元素,下列有关锂元素性质推测正确的是( )A、最高化合价为+2 B、原子半径比钠的大 C、单质与水的反应比钠更剧烈 D、最高价氧化物对应的水化物碱性比钠的弱二、非选择题:本大题共3小题,共计22分。
-
23. 乙醇(CH3CH2OH)既是生活中常见的有机物,又是重要的化工原料。(1)、工业上可用乙烯制备乙醇,其反应的化学方程式为:
CH2 = CH2 + H2O CH3CH2OH
该反应属于反应(填“加成”或“取代”)。
(2)、官能团决定有机物的性质。乙醇中含有的官能团名称是。(3)、为探究乙醇的性质,某学生向试管中加入3 mL乙醇,将下端绕成螺旋状的铜丝在酒精灯火焰上灼烧至红热后,迅速插入乙醇中,可观察到铜丝表面由黑色变成红色,说明乙醇具有性。(4)、萃取是物质分离的一种方法。某学生拟用乙醇萃取溴水中的Br2 , 判断该方法是否可行:(填“是”或“否”),判断的理由是。24. 硝酸钙晶体[Ca(NO3)2·4H2O]常用于电子、仪表及冶金工业。一种利用CaO制备Ca(NO3)2·4H2O的流程如下: (1)、“制浆”过程中发生反应的化学方程式是。(2)、“气体X”的化学式是。(3)、Ca(NO3)2·4H2O的溶解度随温度变化的曲线如图所示。“酸化”后制取Ca(NO3)2·4H2O的操作主要包括加热浓缩、、过滤、洗涤、干燥。实验室过滤操作必须用到的玻璃仪器有烧杯、玻璃棒和。
(1)、“制浆”过程中发生反应的化学方程式是。(2)、“气体X”的化学式是。(3)、Ca(NO3)2·4H2O的溶解度随温度变化的曲线如图所示。“酸化”后制取Ca(NO3)2·4H2O的操作主要包括加热浓缩、、过滤、洗涤、干燥。实验室过滤操作必须用到的玻璃仪器有烧杯、玻璃棒和。 25. 绿矾(FeSO4·7H2O)是自然界存在的一种矿石,翠绿如宝石,很早就引起人们的重视。
25. 绿矾(FeSO4·7H2O)是自然界存在的一种矿石,翠绿如宝石,很早就引起人们的重视。材料一 《唐本草》和《天工开物》等古籍都记载中国很早就能焙烧绿矾制备铁红(主要成分是Fe2O3)。铁红颜色鲜艳,稳定无毒,是中国传统红色颜料的重要着色剂。
材料二 公元8世纪,阿拉伯炼金家查比尔曾提出,把绿矾焙烧可以蒸馏出“矾精”,它具有比较大的溶解力。绿矾焙烧是一种生产硫酸的古老方法。
(1)、某研究性学习小组用下图所示试验装置对绿矾的焙烧反应进行探究。
①实验过程中,装置A玻管中可观察到的实验现象是。
②装置C的作用是。
③该小组学生设计如下实验方案验证“矾精”是硫酸溶液:取U形管中的溶液少许于试管中,滴入(填试剂名称),溶液呈红色,说明“矾精”中含有H+;检验“矾精”中含有SO42-的方法是。
(2)、某工厂计划用绿矾焙烧工艺生产高纯度铁红(Fe2O3)160 kg,计算理论上所需绿矾的质量,写出计算过程。