2017年河南省信阳市中考化学二模试卷
试卷更新日期:2017-08-10 类型:中考模拟
一、选择题
-
1. 合金、氧化铝、硫酸铝三种物质的分类正确的是( )A、盐、氧化物、纯净物 B、单质、混合物、盐 C、混合物、氧化物、盐 D、混合物、盐、化合物2. 下列叙述不正确的是( )A、用互相刻画的方法,可比较硬铝和铝的硬度 B、用灼烧闻气味的方法,可区分棉纤维和蚕丝 C、加熟石灰粉末研磨,可鉴别硫酸铵和氯化铵 D、将冷碟子放在蜡烛火焰的上方,可得到炭黑3. 下列图示的实验操作不正确的是( )A、给液体加热
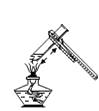 B、测溶液的pH
B、测溶液的pH 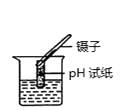 C、稀释浓硫酸
C、稀释浓硫酸 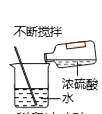 D、蒸发食盐水
D、蒸发食盐水  4. 下列叙述正确的是( )A、氯化钠是由钠离子和氯离子构成的化合物 B、分子在不停运动,原子不运动 C、原子的最外层电子数决定元素的种类 D、保持二氧化碳化学性质的粒子是碳原子和氧原子5. 下列四组结构示意图表示的元素在元素周期表中是同一横行的一组是( )A、
4. 下列叙述正确的是( )A、氯化钠是由钠离子和氯离子构成的化合物 B、分子在不停运动,原子不运动 C、原子的最外层电子数决定元素的种类 D、保持二氧化碳化学性质的粒子是碳原子和氧原子5. 下列四组结构示意图表示的元素在元素周期表中是同一横行的一组是( )A、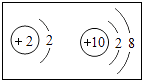 B、
B、 C、
C、 D、
D、 6. 如图为两种气体发生化学反应的微观示意图,其中相同的球代表相同的原子,你认为下列说法正确的是( )
6. 如图为两种气体发生化学反应的微观示意图,其中相同的球代表相同的原子,你认为下列说法正确的是( ) A、化学反应前后原子个数没有改变 B、分子是化学变化中的最小微粒 C、反应前后各元素化合价没有改变 D、该反应不是化合反应7. 物质在“潮湿的空气”中发生变化与空气中某些气体有关.下列说法不正确的是( )A、钢铁生锈与氧气、水蒸气有关 B、氢氧化钠固体潮解、变质,与水蒸气、二氧化碳有关 C、铜器表面生成铜绿[Cu2(OH)2CO3]与O2、CO2、水蒸气有关 D、生石灰堆放久了变质与氧气有关8. 在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前后各物质的质量分数如图所示.下列说法正确的是( )
A、化学反应前后原子个数没有改变 B、分子是化学变化中的最小微粒 C、反应前后各元素化合价没有改变 D、该反应不是化合反应7. 物质在“潮湿的空气”中发生变化与空气中某些气体有关.下列说法不正确的是( )A、钢铁生锈与氧气、水蒸气有关 B、氢氧化钠固体潮解、变质,与水蒸气、二氧化碳有关 C、铜器表面生成铜绿[Cu2(OH)2CO3]与O2、CO2、水蒸气有关 D、生石灰堆放久了变质与氧气有关8. 在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前后各物质的质量分数如图所示.下列说法正确的是( )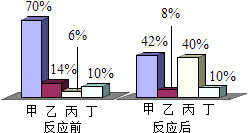 A、丙可能是单质 B、丁可能是该反应的催化剂 C、若消耗3g的乙,则生成17g的丙 D、甲、乙的质量之和一定等于生成丙的质量9. 按下列装置实验,不能达到对应目的是( )A、
A、丙可能是单质 B、丁可能是该反应的催化剂 C、若消耗3g的乙,则生成17g的丙 D、甲、乙的质量之和一定等于生成丙的质量9. 按下列装置实验,不能达到对应目的是( )A、 收集H2
B、
收集H2
B、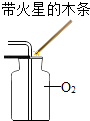 O2验满
C、
O2验满
C、 配制20%的Ca(OH)2溶液
D、
配制20%的Ca(OH)2溶液
D、 除去CO中的CO2
10. 两个烧杯中装有等质量的金属锌和镁,然后分别逐渐加入同浓度的稀硫酸,产生氢气的质量与加入硫酸的质量关系如图所示.下列说法正确的是( )
除去CO中的CO2
10. 两个烧杯中装有等质量的金属锌和镁,然后分别逐渐加入同浓度的稀硫酸,产生氢气的质量与加入硫酸的质量关系如图所示.下列说法正确的是( )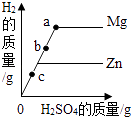 A、该图反映出镁比锌的金属活动性强 B、a点时,两个烧杯中的酸都恰好完全反应 C、b点时,两个烧杯中产生氢气的质量相同 D、c点时,两个烧杯中都有金属剩余11. 下列离子组合能在pH=12的溶液中大量共存的是( )A、K+、Cu2+、SO42﹣、Cl﹣ B、K+、Na+、NO3﹣、Cl﹣ C、CO32﹣、H+、Na+、Cl﹣ D、Ba2+、Cl﹣、Na+、SO42﹣12. 在一定的条件下,与氢氧化钠溶液、碳酸钾溶液、氧化铜、锌和氯化钡溶液五种物质均能发生反应的是( )A、稀盐酸 B、硫酸铜溶液 C、稀硫酸 D、二氧化碳13. 下列各物质无论以何种比例混合,其氯元素的质量分数不变的是( )A、HClO4、KClO3 B、NaClO、KCl C、KClO、KCl D、NaCl、KCl14. 用NaCl、CaCl2、AlCl3溶液分别与相同浓度的AgNO3溶液反应,生成等质量的AgCl,则它们所需AgNO3溶液的质量比是( )A、1:1:1 B、1:2:3 C、6:3:2 D、117:222:267
A、该图反映出镁比锌的金属活动性强 B、a点时,两个烧杯中的酸都恰好完全反应 C、b点时,两个烧杯中产生氢气的质量相同 D、c点时,两个烧杯中都有金属剩余11. 下列离子组合能在pH=12的溶液中大量共存的是( )A、K+、Cu2+、SO42﹣、Cl﹣ B、K+、Na+、NO3﹣、Cl﹣ C、CO32﹣、H+、Na+、Cl﹣ D、Ba2+、Cl﹣、Na+、SO42﹣12. 在一定的条件下,与氢氧化钠溶液、碳酸钾溶液、氧化铜、锌和氯化钡溶液五种物质均能发生反应的是( )A、稀盐酸 B、硫酸铜溶液 C、稀硫酸 D、二氧化碳13. 下列各物质无论以何种比例混合,其氯元素的质量分数不变的是( )A、HClO4、KClO3 B、NaClO、KCl C、KClO、KCl D、NaCl、KCl14. 用NaCl、CaCl2、AlCl3溶液分别与相同浓度的AgNO3溶液反应,生成等质量的AgCl,则它们所需AgNO3溶液的质量比是( )A、1:1:1 B、1:2:3 C、6:3:2 D、117:222:267二、填空题
-
15. 天然水中含有很多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是;用肥皂水检验某自来水是硬水还是软水时,发生的化学反应之一为:2C17H35COONa+X=(C17H35COO)2Ca↓+2NaCl,则X的化学式是 .16. 在氧气中点燃红磷的实验过程,固体变化如图所示.
 (1)、从燃烧条件分析,固体质量在t1前没有发生变化的原因为;(2)、该反应的化学方程式为;(3)、参加反应的氧气质量为g.17. 氢氧化钠和氢氧化钙是两种重要的碱,它们既有共性,也有个性.(1)、它们都能与二氧化碳发生反应,写出其中能大量吸收二氧化碳的化学方程式 .(2)、它们都能与酸发生中和反应,但能改良酸性土壤的是(填化学式).(3)、两者溶于水显著放热的是(填俗称),微溶于水的是(填俗称).(4)、氢氧化钙转化为氢氧化钠的化学方程式是 .18. 将6.5g含有一种杂质的锌粉与足量的稀硫酸反应,生成0.18g氢气,则该锌粉中混有的杂质是(填“铜”或“铝”);将纯净的锌粉加入到含有Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,若滤液中只含有一种溶质,则滤液中一定含有 , 若滤渣中含有两种金属,则滤液中可能含有 .19. 如图所示是A,B,C(均不含结晶水)三种物质的溶解度曲线,回答下列问题.
(1)、从燃烧条件分析,固体质量在t1前没有发生变化的原因为;(2)、该反应的化学方程式为;(3)、参加反应的氧气质量为g.17. 氢氧化钠和氢氧化钙是两种重要的碱,它们既有共性,也有个性.(1)、它们都能与二氧化碳发生反应,写出其中能大量吸收二氧化碳的化学方程式 .(2)、它们都能与酸发生中和反应,但能改良酸性土壤的是(填化学式).(3)、两者溶于水显著放热的是(填俗称),微溶于水的是(填俗称).(4)、氢氧化钙转化为氢氧化钠的化学方程式是 .18. 将6.5g含有一种杂质的锌粉与足量的稀硫酸反应,生成0.18g氢气,则该锌粉中混有的杂质是(填“铜”或“铝”);将纯净的锌粉加入到含有Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,若滤液中只含有一种溶质,则滤液中一定含有 , 若滤渣中含有两种金属,则滤液中可能含有 .19. 如图所示是A,B,C(均不含结晶水)三种物质的溶解度曲线,回答下列问题. (1)、将30℃的三种物质的饱和溶液冷却到20℃后,所得溶液中溶质的质量分数有小到大的关系是(用“<”连接).(2)、现有一定质量的B溶液,将该溶液在50℃下恒温蒸发10g水后析出了2.5gB晶体.再恒温蒸发5g水后,又析出了2.5gB晶体,则B物质在50℃时的溶解度是 .20. 一定条件下,4.8gCH4与16.0gO2恰好完全反应,生成10.8gH2O、4.4gCO2和xgCO,则x=;化学方程式为;CH4完全燃烧还需要O2的质量为g.
(1)、将30℃的三种物质的饱和溶液冷却到20℃后,所得溶液中溶质的质量分数有小到大的关系是(用“<”连接).(2)、现有一定质量的B溶液,将该溶液在50℃下恒温蒸发10g水后析出了2.5gB晶体.再恒温蒸发5g水后,又析出了2.5gB晶体,则B物质在50℃时的溶解度是 .20. 一定条件下,4.8gCH4与16.0gO2恰好完全反应,生成10.8gH2O、4.4gCO2和xgCO,则x=;化学方程式为;CH4完全燃烧还需要O2的质量为g.三、简答题
-
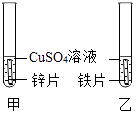
21. 请用化学方程式解释下列问题.(1)、正常雨水的pH约为5.6.(2)、工业上用赤铁矿(主要成分是Fe2O3)与一氧化碳反应来炼铁.22. 某同学为了比较铁、铜、锌的活动性顺序,设计了如图所示的实验.
 (1)、乙试管中发生反应的化学方程式为 .(2)、上述实验不能完全证明三种金属的活动性顺序.请你补充一个实验.23. 如图所示,A﹣F是初中化学常见的物质,其中A,B,E是氧化物.C,D,F是单质,A是造成温室效应的气体,A和B含有相同元素,D是密度最小的气体.图中“→”表示转化关系.
(1)、乙试管中发生反应的化学方程式为 .(2)、上述实验不能完全证明三种金属的活动性顺序.请你补充一个实验.23. 如图所示,A﹣F是初中化学常见的物质,其中A,B,E是氧化物.C,D,F是单质,A是造成温室效应的气体,A和B含有相同元素,D是密度最小的气体.图中“→”表示转化关系. (1)、物质B的一种化学性质 .(2)、C→D的化学方程式是 .(3)、物质F与物质E的相对分子质量差为 .24. 有一包白色固体,可能由氯酸钾、氢氧化钾、碳酸钙、氯化钡中的一种或几种物质组成.为探究该白色固体的组成.某小组学生取适量样品按如图所示流程进行实验,情回答下列问题.
(1)、物质B的一种化学性质 .(2)、C→D的化学方程式是 .(3)、物质F与物质E的相对分子质量差为 .24. 有一包白色固体,可能由氯酸钾、氢氧化钾、碳酸钙、氯化钡中的一种或几种物质组成.为探究该白色固体的组成.某小组学生取适量样品按如图所示流程进行实验,情回答下列问题. (1)、写出试管滤液中的物质能与二氧化碳反应的化学方程式 .(2)、白色沉淀Ⅱ的化学式为 .(3)、原白色固体中含有哪些物质?
(1)、写出试管滤液中的物质能与二氧化碳反应的化学方程式 .(2)、白色沉淀Ⅱ的化学式为 .(3)、原白色固体中含有哪些物质?四、综合应用题
-
25. 实验室选用以下装置制取纯净、干燥的CO2 , 并进一步探究CO2的性质.
 (1)、A装置中反应的化学方程式为 .(2)、要制取纯净、干燥的CO2 , 应选用的装置中导管接口从左到右的连接顺序为 .(3)、利用A装置还可以制取其他气体,有关反应的化学方程式为(写出一个即可)(4)、某同学在收集满CO2的集气瓶中放入燃烧的钠,发现钠继续燃烧,充分反应后生成黑色的碳和一种白色固体.
(1)、A装置中反应的化学方程式为 .(2)、要制取纯净、干燥的CO2 , 应选用的装置中导管接口从左到右的连接顺序为 .(3)、利用A装置还可以制取其他气体,有关反应的化学方程式为(写出一个即可)(4)、某同学在收集满CO2的集气瓶中放入燃烧的钠,发现钠继续燃烧,充分反应后生成黑色的碳和一种白色固体.[做出猜想]白色固体的成分可能为:
a.氧化钠 b.碳酸钠 c.氧化钠和碳酸钠的混合物 d.氢氧化钠
请指出以上不合理的猜想并说明理由: .
[查阅资料]氧化钠为白色粉末,溶于水生成氢氧化钠;碳酸钠溶液呈碱性.
[实验探究]取少量该样品溶于水,将溶液分成两份,一份中加入酚酞溶液,变红;另一份先加入过量CaCl2溶液,出现白色沉淀,过滤,向滤液里加酚酞溶液,无明显现象.
[得出结论]白色固体的成分为 .
(5)、氢氧化钠在工业中常用于吸收含有氯气的废气.氢氧化钠和氯气反应生成氯化钠、次氯酸钠(NaClO)和另一种氧化物.若要吸收71g氯气.理论上需要20%的氢氧化钠溶液的质量是多少?