2017年江苏省连云港市中考化学试卷
试卷更新日期:2017-08-08 类型:中考真卷
一、选择题
-
1. 连云港市正在创建国家级文明城市.下列做法与此不相符的是( )A、分类回收生活垃圾,垃圾资源化 B、加大空气质量监测,改善环境状况 C、预防治理水体污染,保护水资源 D、过度使用农药化肥,提高粮食产量2. 日常生活中时刻发生着变化,下列变化中包含化学变化的是( )A、美酒飘香 B、鸡蛋变臭 C、切割玻璃 D、滴水成冰3. 下列化学用语表示正确的是( )A、60个碳原子:C60 B、2个氢氧根离子:2OH C、金刚石:Au D、3个二氧化硫分子:3SO24. 正确的操作是实验成功的关键.下列图示实验操作正确的是( )A、
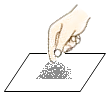 取用固体粉末
B、
取用固体粉末
B、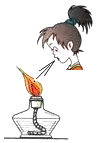 熄灭酒精灯
C、
熄灭酒精灯
C、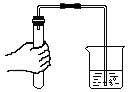 检查气密性
D、
检查气密性
D、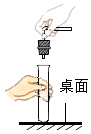 连接仪器
5. 下列有关实验现象的描述正确的是( )A、小木棍蘸取浓硫酸一段时间后,小木棍变黑 B、硝酸铵固体溶于水后,溶液的温度几乎不变 C、氢氧化钠固体久置于表面皿上,无明显现象 D、尿素和熟石灰混合研磨,产生刺激性气味的气体6. 如图是元素周期表的一部分.下列说法正确的是( )
连接仪器
5. 下列有关实验现象的描述正确的是( )A、小木棍蘸取浓硫酸一段时间后,小木棍变黑 B、硝酸铵固体溶于水后,溶液的温度几乎不变 C、氢氧化钠固体久置于表面皿上,无明显现象 D、尿素和熟石灰混合研磨,产生刺激性气味的气体6. 如图是元素周期表的一部分.下列说法正确的是( )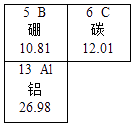 A、硼为金属元素 B、碳的原子序数是12.01 C、铝是地壳中含量最高的元素 D、三种原子中质量最大的是铝7. 维生素是人体必需的营养物质,维生素D2的化学式为C28H44O.下列说法正确的是( )A、维生素D2属于有机化合物 B、维生素D2中含有73个原子 C、维生素D2的相对分子质量是396g D、维生素D2中氢元素的质量分数最大8. 下列关于物质性质和用途的说法不正确的是( )A、干冰升华时吸收大量的热,干冰可用作制冷剂 B、铝不与空气反应,铝制品可不用涂保护层来防腐 C、小苏打能与酸反应生成气体,小苏打可制作发酵粉 D、稀有气体在通电时能发出不同颜色的光,稀有气体可制作霓虹灯9. 我国古代典籍中有“银针验毒”的记载,“银针验毒”的反应原理之一是4Ag+2H2S+O2═2X+2H2O,下列有关该反应的说法不正确的是( )A、反应属于氧化反应 B、X的化学式是Ag2S C、反应前后元素的种类不变 D、反应前后所有元素的化合价都发生了变化10. 下列实验方案能达到实验目的是( )
A、硼为金属元素 B、碳的原子序数是12.01 C、铝是地壳中含量最高的元素 D、三种原子中质量最大的是铝7. 维生素是人体必需的营养物质,维生素D2的化学式为C28H44O.下列说法正确的是( )A、维生素D2属于有机化合物 B、维生素D2中含有73个原子 C、维生素D2的相对分子质量是396g D、维生素D2中氢元素的质量分数最大8. 下列关于物质性质和用途的说法不正确的是( )A、干冰升华时吸收大量的热,干冰可用作制冷剂 B、铝不与空气反应,铝制品可不用涂保护层来防腐 C、小苏打能与酸反应生成气体,小苏打可制作发酵粉 D、稀有气体在通电时能发出不同颜色的光,稀有气体可制作霓虹灯9. 我国古代典籍中有“银针验毒”的记载,“银针验毒”的反应原理之一是4Ag+2H2S+O2═2X+2H2O,下列有关该反应的说法不正确的是( )A、反应属于氧化反应 B、X的化学式是Ag2S C、反应前后元素的种类不变 D、反应前后所有元素的化合价都发生了变化10. 下列实验方案能达到实验目的是( )实验目的
实验方法
A
除去KCl固体中的KClO3
加入少量MnO2固体,加热
B
鉴别硬水和软水
滴加肥皂水振荡,观察产生气泡的情况
C
比较人体吸入气体和呼出气体中O2的含量
将带火星的木条分别插入两种气体中
D
探究稀盐酸和NaOH溶液是否完全反应
向反应后溶液中加入AgNO3溶液
A、A B、B C、C D、D11. 如图是甲、乙固体的溶解度曲线,下列说法正确的是( )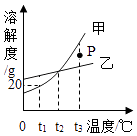 A、图中P点所表示的溶液是t3℃时甲的饱和溶液 B、可用t1℃时20%的甲溶液配制10%的甲溶液 C、若甲中含有少量乙,可采用冷却热饱和溶液的方法提纯甲 D、分别将t3℃等质量的甲、乙饱和溶液降温至t2℃,所得溶液中溶质质量相等12. 如图中甲﹣戊是初中化学教材中常见物质.甲、戊为氧化物且甲为黑色固体,乙、丙分别是酸和碱中的一种,丁是大理石的主要成分.(图“﹣”表示相连的物质间可发生反应,“→”表示一种物质可转化为另一种物质,反应条件、部分反应物与生成物均已略去).下列说法中不正确的是( )
A、图中P点所表示的溶液是t3℃时甲的饱和溶液 B、可用t1℃时20%的甲溶液配制10%的甲溶液 C、若甲中含有少量乙,可采用冷却热饱和溶液的方法提纯甲 D、分别将t3℃等质量的甲、乙饱和溶液降温至t2℃,所得溶液中溶质质量相等12. 如图中甲﹣戊是初中化学教材中常见物质.甲、戊为氧化物且甲为黑色固体,乙、丙分别是酸和碱中的一种,丁是大理石的主要成分.(图“﹣”表示相连的物质间可发生反应,“→”表示一种物质可转化为另一种物质,反应条件、部分反应物与生成物均已略去).下列说法中不正确的是( )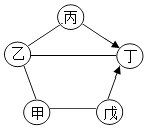 A、乙溶液能使紫色石蕊溶液变红 B、丙溶液能与戊反应生成丁 C、甲→戊只能通过置换反应实现 D、不能由甲通过一步反应生成丁
A、乙溶液能使紫色石蕊溶液变红 B、丙溶液能与戊反应生成丁 C、甲→戊只能通过置换反应实现 D、不能由甲通过一步反应生成丁二、解答题
-
13. “舌尖上的化学”.以下是厨房中一些实物图.
 (1)、牛肉富含的营养物质是 .(2)、碘盐中的“碘”是指(选填“元素”、“原子”或“单质”).食用碘盐是为了预防疾病.(填字母)
(1)、牛肉富含的营养物质是 .(2)、碘盐中的“碘”是指(选填“元素”、“原子”或“单质”).食用碘盐是为了预防疾病.(填字母)a.贫血 b.甲状腺肿大 c.夜盲症
(3)、为保障“舌尖上的安全”,下列做法合理的是 . (填字母)a.霉变大米蒸煮后食用 b.甲醛溶液浸泡虾仁防腐 c.适当使用食品添加剂
(4)、净水机所标物质中属于有机合成材料的是 , 净水机中使用活性炭来除去水中一些溶解的杂质,是因为活性炭具有作用.14. 科学方法对化学学习起着事半功倍的作用.(1)、分类归纳是研究化学物质的重要方法.如图1是某同学整理的铁及其化合物的知识网络图.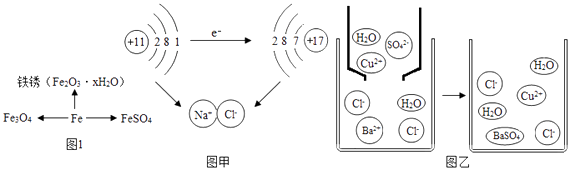
①铁丝燃烧生成Fe3O4的过程中(选填“放出”或“吸收”)热量.
②铁制品的锈蚀过程,实际上是铁与空气中的等发生化学反应的过程.
③与FeSO4中铁元素化合价相同的铁氧化物的化学式是 .
(2)、微观粒子模型化是研究化学变化的重要方法.①图甲是钠与氯气反应生成氯化钠的示意图.该图说明在化学反应过程中一定发生变化的是 . (填字母)
a.原子核 b.原子核最外层电子数 c.原子的电子层数
②图乙是硫酸铜溶液与氯化钡溶液反应示意图.从粒子角度分析该化学反应能发生的原因是 .
(3)、控制变量、设计对比实验是实验探究的重要方法.
①实验1中同时向烧杯中加入一粒相同大小的品红,发现整杯水变红的时间热水比冷水短.这是因为 .
②实验2中使用铜片是为了对比不同.
③实验3是大小形状相同的Mg、Zn、Fe、Cu四种金属同时投入到盐酸中发生的现象,金属周围的黑点表示生成的气体.下列结论不正确的是(填字母).
a.铜不能发生置换反应
b.四种金属中金属活动性最强的是Mg
c.等质量的锌和铁分别与足量的盐酸发生生成气体质量:Zn比Fe多.
15. 海洋是巨大的资源宝库,从海洋中可以获得很多物质,连云港水资源丰富.(1)、通过晾晒海水得到的粗盐中含有多种可溶性杂质和不溶性杂质(泥沙等).实验室中除去粗盐中不溶性杂质获得精盐的步骤是:溶解→过滤→蒸发→计算产率等.①过滤操作中玻璃棒的末端要轻轻的斜靠在一边.蒸发时为防止液滴飞溅,除用玻璃棒搅拌外,还可以采取的操作是 .
②下列操作可能导致精盐产率偏高的是(填字母)
a.食盐没有完全溶解即过滤 b.过滤时液面高于滤纸边缘
c.器皿上粘有的精盐没有全部转移到称量纸上
(2)、海水中含量最多的氯化物是氯化钠,其次是氯化镁.如图1是从海水中获得氯化镁溶液的流程.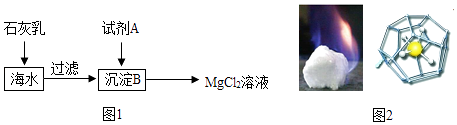
①在海水中加入石灰乳后,发生反应的化学方程式是 .
②上述过程中试剂A与沉淀B法神的是中和反应,则试剂A是(填名称) .
(3)、2017年5月18日,在中国南海海域实现可燃冰(CH4•nH2O)试采成功,这将使人类能源格局翻开新篇章.①可燃冰中,水分子形成一种空间笼状结构,甲烷和少量N2、CO2等分子填入笼内空隙中,无固定的化学计量关系,因此可燃冰属于(选填“纯净物”或“混合物”).
②若某种可燃冰中CH4与H2O的质量比是1:9,则该可燃冰中n= .
③可燃冰中甲烷完全燃烧的化学方程式是 .
16. “氧泡泡”系列产品去污能力强、绿色环保,已成为中国氧系清洁品类领导品牌,其主要成分是过碳酸钠(2Na2CO3•3H2O2).某化学活动小组对过碳酸钠产生了浓厚的兴趣,决定对其进行探究.【查阅资料】
Ⅰ.过碳酸钠在水中易离解成Na2CO3和H2O2 , 其水溶液具有Na2CO3和H2O2的双重性质;
Ⅱ.过碳酸钠与盐酸反应:2(2Na2CO3•3H2O2)+8HCl═8NaCl+4CO2↑+3O2↑+10H2O;
Ⅲ.过碳酸钠的去污能力主要与其在反应中释放处的“活性氧”有关,“活性氧”含量越高,去污能力越强.
(1)、20℃时,测得1%过碳酸钠水溶液的pH为10.5,说明其溶液呈(选填“酸性”、“中性”或“碱性”).(2)、向过碳酸钠水溶液中加入少量MnO2时产生大量气泡,发生反应的化学方程式是 .(3)、过碳酸钠样品中“活性氧”含量可按如下公式计算:“活性氧”含量= ×100%
为测定某过碳酸钠样品中“活性氧”含量,取20g样品按如图实验装置与足量盐酸反应.(已知样品中杂质不溶于水且不与盐酸反应,装置气密性良好)
①将盐酸慢慢地入A中,反应一段时间,观察到 , 停止滴加盐酸.
②装置B可吸收生成的CO2 , 该反应的化学方程式是 .
③甲同学认为若要得出生成氧气的质量,除要记录量筒内液体的读数外,还需要知道的数据是该实验条件下的 .
④将反应后A中所得溶液过滤、蒸发、结晶、烘干,称得固体质量为11.7g,乙同学据此计算出该过碳酸钠样品的“活性氧”含量,写出其计算过程 .
⑤完成上述探究后,丙同学提出:称量反应前后装置B的质量,其质量差就是反应生成CO2的质量,据此可计算出样品中“活性氧”含量.但丁同学认为该方案不合理,丁同学的理由是(填写一条即可)