2017年江苏省淮安市中考化学试卷
试卷更新日期:2017-08-08 类型:中考真卷
一、选择题
-
1. 下列变化中,属于化学变化的是( )A、粉笔折断 B、棉纱织布 C、木材燃烧 D、汽油挥发2. 下列实验操作错误的是( )A、
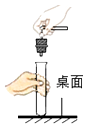 B、
B、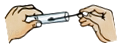 C、
C、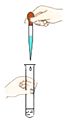 D、
D、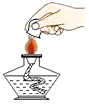 3. 下列生活中常见物质与水混合,能形成溶液的是( )A、牙膏 B、蔗糖 C、面粉 D、豆油4. 下列做法会危害人体健康的是( )A、饮用低温灭菌牛奶 B、食用新鲜蔬菜水果 C、用小苏打做发酵粉 D、用甲醛浸泡水产品5. 某博物馆藏有一柄古代铁剑,为防止其生锈,下列做法合理的是( )A、定期用清水冲洗,除去灰尘 B、放于体验区,让观众触摸 C、用盐水除去铁剑上的锈斑 D、放在充满氮气的展览柜中6. 焦亚硫酸钠在食品加工中常用作防腐剂、漂白剂和疏松剂.焦亚硫酸钠(Na2S2O5)中硫元素的化合价为( )A、﹣2 B、+3 C、+4 D、+57. 下列有关水的说法正确的是( )A、水中加入固体硝酸铵可降低溶液温度 B、通过活性炭的吸附可使硬水变为软水 C、为保护水资源,禁止使用化肥和农药 D、无色透明的深层地下水属于纯净物8. 如图是我国《可再生资源法》倡导的碳资源的转化与循环利用示意图.下列做法与该图体现的理念不符的是( )
3. 下列生活中常见物质与水混合,能形成溶液的是( )A、牙膏 B、蔗糖 C、面粉 D、豆油4. 下列做法会危害人体健康的是( )A、饮用低温灭菌牛奶 B、食用新鲜蔬菜水果 C、用小苏打做发酵粉 D、用甲醛浸泡水产品5. 某博物馆藏有一柄古代铁剑,为防止其生锈,下列做法合理的是( )A、定期用清水冲洗,除去灰尘 B、放于体验区,让观众触摸 C、用盐水除去铁剑上的锈斑 D、放在充满氮气的展览柜中6. 焦亚硫酸钠在食品加工中常用作防腐剂、漂白剂和疏松剂.焦亚硫酸钠(Na2S2O5)中硫元素的化合价为( )A、﹣2 B、+3 C、+4 D、+57. 下列有关水的说法正确的是( )A、水中加入固体硝酸铵可降低溶液温度 B、通过活性炭的吸附可使硬水变为软水 C、为保护水资源,禁止使用化肥和农药 D、无色透明的深层地下水属于纯净物8. 如图是我国《可再生资源法》倡导的碳资源的转化与循环利用示意图.下列做法与该图体现的理念不符的是( )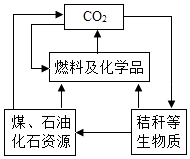 A、将秸秆加工转化为酒精燃料 B、二氧化碳作为原料生产尿素 C、过度开采煤、石油作为燃料 D、将石油精炼,制备合成材料9. 下列实验方案不能达到实验目的是( )
A、将秸秆加工转化为酒精燃料 B、二氧化碳作为原料生产尿素 C、过度开采煤、石油作为燃料 D、将石油精炼,制备合成材料9. 下列实验方案不能达到实验目的是( )选项
实验目的
实验方案
A
区别聚乙烯与聚氯乙烯
分别将两种塑料灼烧,闻气味
B
比较铜与银的金属活动性强弱
将铜和银分别放入盐酸中,观察现象
C
区别天然气与一氧化碳
分别点燃两种气体,检验燃烧产物
D
判断温度对溶解速率的影响
对比高锰酸钾固体在冷、热水中溶解的快慢
A、A B、B C、C D、D10. 下列四个图象中,能正确反映对应变化关系的是( )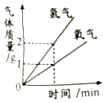

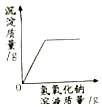

A、用CuFe2O4﹣x做催化剂,光分解水制氢气与氧气
B、向氯化钠的饱和溶液中加入硝酸钾
C、向混有少量硫酸的硫酸铜溶液中加入氢氧化钠溶液
D、向一定质量的碳酸钠溶液中加水
A、A B、B C、C D、D二、填充与简答题
-
11. 用符合要求的物质的序号填空.
①生石灰 ②盐酸 ③石墨 ④碘酒
(1)、可用于伤口消毒的是 .(2)、可用于制作铅笔芯的是 .(3)、可用作食品干燥剂的是 .12. 质量守恒定律的发现对化学的发展作出了巨大贡献.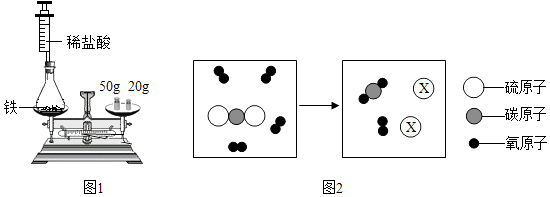 (1)、为验证质量守恒定律,小华设计如图1所示装置进行实验.
(1)、为验证质量守恒定律,小华设计如图1所示装置进行实验.实验时,先将装有药品的装置放在天平上,添加砝码,移动游码至天平平衡(如图1所示),然后取下装置,用针筒向锥形瓶中注入少量稀盐酸,反应后再将装置放置于天平上,观察到 , 从而验证了质量守恒定律.若将锥形瓶改为烧杯,则不能验证质量守恒定律,原因是 .
(2)、某反应的微观示意图如图2所示.①X的化学式是 .
②根据上述微观示意图,可得出化学反应遵循质量守恒定律的本质原因是 .
13. 如图所示是四种物质的溶解度曲线图,请回答下列问题. (1)、在60℃时,四种物质中溶解度最大的是 .(2)、将40℃时氯化钾的不饱和溶液,保持溶液温度不变,制成饱和溶液,可行的方法有(举1例).(3)、在t℃时,将30g氯化铵加入50g水中,充分溶解,所得溶液质量分数为(精确到0.1%).(4)、向饱和食盐水中加入足量的碳酸氢铵固体,会有溶解度较小的碳酸氢钠晶体析出,该反应的化学方程式是NaCl+NH4HCO3=NaHCO3↓+NH4Cl,请根据以上信息和图中物质的溶解度曲线,简述以硫酸铵固体为原料制取较纯硫酸钾晶体的方法: .14. 我国化学家傅鹰教授有一句名言“科学只给我们知识,而历史却给我们智慧”在化学学习中,了解知识的发展历程,可以促进我们正确理解科学本质.(1)、我国西汉时期就有“曾青得铁则化为铜”的记载,其中蕴涵的湿法冶铜原理为(用化学方程式表示).(2)、火药起源于唐朝.为使烟火产生耀眼的白光,可在其火药中加入(填一种金属名称).(3)、十八世纪,化学家们研究发现某些金属与酸反应能生成一种气体,该气体被喻为“会制造水的物质”,对上述反应原理的认识加快了推翻燃素学说的进程.该气体在空气中燃烧制造水的化学方程式是 .(4)、现代以来,人们对金属的认识不断深入,助推多种新材料的研制与使用.2017年5月5日我国首架试飞成功的大型客机C919使用了多种新材料,其中有锂铝合金,在飞机制造中使用该材料说明其具有的优点有(填序号).
(1)、在60℃时,四种物质中溶解度最大的是 .(2)、将40℃时氯化钾的不饱和溶液,保持溶液温度不变,制成饱和溶液,可行的方法有(举1例).(3)、在t℃时,将30g氯化铵加入50g水中,充分溶解,所得溶液质量分数为(精确到0.1%).(4)、向饱和食盐水中加入足量的碳酸氢铵固体,会有溶解度较小的碳酸氢钠晶体析出,该反应的化学方程式是NaCl+NH4HCO3=NaHCO3↓+NH4Cl,请根据以上信息和图中物质的溶解度曲线,简述以硫酸铵固体为原料制取较纯硫酸钾晶体的方法: .14. 我国化学家傅鹰教授有一句名言“科学只给我们知识,而历史却给我们智慧”在化学学习中,了解知识的发展历程,可以促进我们正确理解科学本质.(1)、我国西汉时期就有“曾青得铁则化为铜”的记载,其中蕴涵的湿法冶铜原理为(用化学方程式表示).(2)、火药起源于唐朝.为使烟火产生耀眼的白光,可在其火药中加入(填一种金属名称).(3)、十八世纪,化学家们研究发现某些金属与酸反应能生成一种气体,该气体被喻为“会制造水的物质”,对上述反应原理的认识加快了推翻燃素学说的进程.该气体在空气中燃烧制造水的化学方程式是 .(4)、现代以来,人们对金属的认识不断深入,助推多种新材料的研制与使用.2017年5月5日我国首架试飞成功的大型客机C919使用了多种新材料,其中有锂铝合金,在飞机制造中使用该材料说明其具有的优点有(填序号).①硬度大 ②密度小 ③易导电 ④耐腐蚀.
15. X、Y、Z、M、Q为生活中常见物质.Q为单质,其余为化合物,X为呼吸作用的产物,M为光合作用的产物,Z常温下为液体.各物质之间的转化关系如图所示(部分反应物、生成物、转化关系及反应条件未标出),回答下列问题: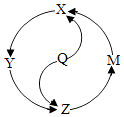 (1)、M属于(填“无机物”或“有机物”).(2)、Q的化学式为 .(3)、若Y属于盐类物质,则X→Y可能发生的化学反应方程式是(举1例).
(1)、M属于(填“无机物”或“有机物”).(2)、Q的化学式为 .(3)、若Y属于盐类物质,则X→Y可能发生的化学反应方程式是(举1例).三、实验与探究题
-
16. 根据如图回答下列问题:
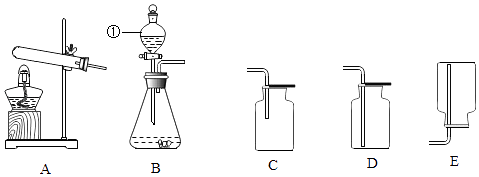 (1)、图B中标有序号①的仪器名称是 .(2)、组装好气体发生装置后,先应该检查装置的 , 然后再添加药品.(3)、欲收集密度比空气大的气体,应该选择的装置是(填序号).(4)、实验室用石灰石与稀盐酸反应制取二氧化碳的化学方程式是 .17. 小文同学利用长柄W形玻璃管,完成了课本上多个化学实验.
(1)、图B中标有序号①的仪器名称是 .(2)、组装好气体发生装置后,先应该检查装置的 , 然后再添加药品.(3)、欲收集密度比空气大的气体,应该选择的装置是(填序号).(4)、实验室用石灰石与稀盐酸反应制取二氧化碳的化学方程式是 .17. 小文同学利用长柄W形玻璃管,完成了课本上多个化学实验.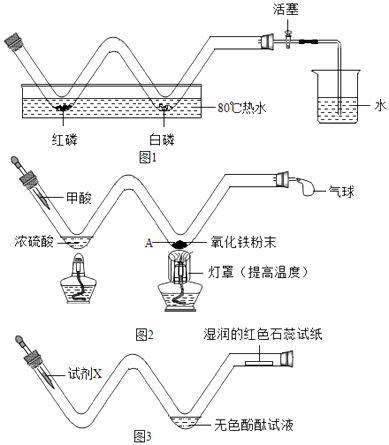 (1)、燃烧条件的探究与空气中氧气含量的粗略测定
(1)、燃烧条件的探究与空气中氧气含量的粗略测定①燃烧条件的探究:在如图1所示装置(省略夹持仪器,下同)中,向W形玻璃管中放入足量红磷和白磷,塞好橡皮塞,关闭活塞,然后将其放入80℃的热水中,观察到红磷不燃烧而白磷燃烧,说明可燃物发生燃烧应具备的条件是 .
②空气中氧气含量的粗略测定:为减小测量误差,待火焰熄灭后,将玻璃管 , 再打开活塞.
(2)、一氧化碳与氧化铁反应①甲酸(HCOOH)在热浓硫酸的作用下,分解生成一氧化碳和水,该反应的化学方程式是 .
②实验时,A处可以观察到的现象是 .
(3)、探究微粒的性质向玻璃管左端加入试剂X,观察到无色酚酞试液变红,湿润的红色石蕊试纸变蓝,试剂X可能是 , 该装置的优点有(答1点).
18. 氯化镁是一种重要的化工原料,同学们在实验室对其开展了系列研究.(1)、课题1:选择制取氯化镁的原料【查阅资料】
①全球海水中含有的盐类总质量为5亿亿吨,其中含有的各种离子占盐类总质量的百分含量如下表所示:
离子
Cl﹣
Na+
Mg2+
Ca2+
K+
其他
含量
55.06%
30.61%
3.69%
1.15%
1.10%
…
②工业生产中海水或卤水(海水晒盐后的剩余溶液)都可以作为制取氯化镁的原料.
【交流讨论】
同学们经讨论,一致选择卤水用于实验室制取氯化镁.你认为他们的理由是 .
(2)、课题2:由卤水制取氯化镁同学们设计如图所示方案,从卤水中制取氯化镁.
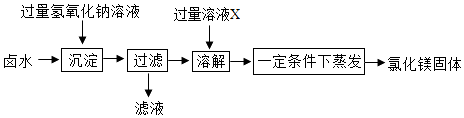
①溶液X的名称是 .
②部分同学认为上述制取方案不够完善,在“过滤”操作后缺少“洗涤”操作,从而导致制取的氯化镁不纯,可能混有的杂质是 .
(3)、课题3:测定氯化镁产品的纯度(氯化镁的质量分数)同学们设计如下实验方案对制得的氯化镁进行纯度测定.
【实验步骤】
①称取9.5g氯化镁样品,放于烧杯中,加足量的水溶解,形成溶液;
②向上述溶液中加入90g质量分数为10%的氢氧化钠溶液;
③充分反应后,过滤;
④…
⑤向所得溶液中加入几滴无色酚酞试液,溶液变红,再逐滴加入10%稀硫酸(密度为1.07g•mL﹣1),并 , 当观察到溶液恰好褪色且30s内红色不复现,停止加入稀硫酸;
⑥计算氯化镁样品的纯度.
(4)、【问题讨论】①为计算出氯化镁样品的纯度,除上述数据外,实验还需测量的数据是 .
②若缺少步骤④,则会导致氯化镁纯度测定不准确,步骤④的操作是 .
四、计算题
-
19. 高铁酸钠(Na2FeO4)是一种高效多功能水处理剂,工业上常采用次氯酸钠(NaClO)氧化法生产,反应原理用化学方程式表示为:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O(1)、在Fe(NO3)3中,铁元素和氮元素的质量比为(填最简比).(2)、现称取44.7g次氯酸钠,最多能制得高铁酸钠的质量是多少?(列式计算)
温馨提示:NaClO的相对分子质量为74.5;Na2FeO4的相对分子质量为166.