2017年北京市中考化学试卷
试卷更新日期:2017-08-08 类型:中考真卷
一、选择题
-
1. 下列做法中,不符合“尊重自然、自觉践行绿色生活”倡议的是( )A、人走关灯、少开空调 B、使用一次性餐具 C、自带水杯出行 D、对垃圾进行分类2. “含氟牙膏”中的“氟”指的是( )A、分子 B、原子 C、离子 D、元素3. 下列物质在氧气中燃烧,现象为火星四射,有黑色固体生成的是( )A、红磷 B、木炭 C、铁丝 D、酒精4. 下列人体所必需的元素中,缺乏后会导致贫血的是( )A、铁 B、钙 C、碘 D、锌5. 下列物质的性质,属于化学性质的是( )A、颜色 B、密度 C、可燃性 D、沸点6. 下列物质通常不会损害人体健康的是( )A、一氧化碳 B、黄曲霉素 C、水 D、甲醛7. 铬在元素周期表中信息如图所示,下列有关铬元素的说法正确的是( )
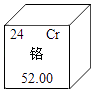 A、原子序数是24 B、属于非金属元素 C、一个铬原子核外有28个电子 D、相对原子质量为52.00g8. 下列物质中,属于纯净物的是( )A、氧气 B、糖水 C、食醋 D、大理石9. 下列方法能区分氧气和二氧化碳两瓶气体的是( )A、闻气味 B、观察颜色 C、倒入适量氢氧化钠溶液 D、将燃着的木条伸入集气瓶中10. 下列符号能表示两个氢分子的是( )A、2H B、2H2 C、H2 D、2H2O211. 土壤的酸碱度会影响植物的生长.下列植物在微酸性土壤中,不适宜种植的是( )
A、原子序数是24 B、属于非金属元素 C、一个铬原子核外有28个电子 D、相对原子质量为52.00g8. 下列物质中,属于纯净物的是( )A、氧气 B、糖水 C、食醋 D、大理石9. 下列方法能区分氧气和二氧化碳两瓶气体的是( )A、闻气味 B、观察颜色 C、倒入适量氢氧化钠溶液 D、将燃着的木条伸入集气瓶中10. 下列符号能表示两个氢分子的是( )A、2H B、2H2 C、H2 D、2H2O211. 土壤的酸碱度会影响植物的生长.下列植物在微酸性土壤中,不适宜种植的是( )植物
花生
苹果
西瓜
沙枣
适宜的pH范围
5.0~6.0
5.0~6.5
6.0~7.0
8.0~8.7
A、花生 B、苹果 C、西瓜 D、沙枣12. 硅是信息技术的关键材料.高温下氢气与四氯化硅(SiCl4)反应的化学方程式为:2H2+SiCl4 Si+4HCl,该反应属于( )A、化合反应 B、分解反应 C、置换反应 D、复分解反应13. 下列关于物质用途的描述不正确的是( )A、氧气可用作燃料 B、二氧化碳可用作气体肥料 C、干冰可用于人工降雨 D、铜丝可用作导线14. 如图为尿素【CO(NH2)2】中各元素质量分数的示意图,其中表示氮元素质量分数的是( )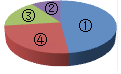 A、① B、② C、③ D、④15. 用“W”型玻璃管进行微型实验,如下图所示.下列说法不正确的是( )
A、① B、② C、③ D、④15. 用“W”型玻璃管进行微型实验,如下图所示.下列说法不正确的是( ) A、a处红棕色粉末变为黑色 B、a处的反应为CO+Fe2O3=2Fe+CO2 C、b处澄清石灰水变浑浊证明有CO2生成 D、可利用点燃的方法进行尾气处理16. 依据实验和溶解度曲线回答16~19题.
A、a处红棕色粉末变为黑色 B、a处的反应为CO+Fe2O3=2Fe+CO2 C、b处澄清石灰水变浑浊证明有CO2生成 D、可利用点燃的方法进行尾气处理16. 依据实验和溶解度曲线回答16~19题.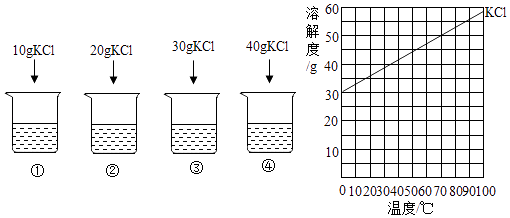
25℃时,向下列4只盛有100g水的烧杯中,分别加入不同质量的KCl固体,充分溶解.
①中溶液的质量为( )
A、10g B、90g C、100g D、110g17. 25℃时,向下列4只盛有100g水的烧杯中,分别加入不同质量的KCl固体,充分溶解.
上述溶液为饱和溶液的是( )
A、②③④ B、②④ C、③④ D、④18. 25℃时,向下列4只盛有100g水的烧杯中,分别加入不同质量的KCl固体,充分溶解.
能将不饱和KCl溶液变为饱和KCl溶液的方法是( )
A、升高温度 B、加水 C、加KCl固体 D、倒出部分溶液19. 25℃时,向下列4只盛有100g水的烧杯中,分别加入不同质量的KCl固体,充分溶解.
④中溶液的溶质质量分数约为( )
A、26% B、29% C、35% D、40%20. 实验小组用传感器探究稀NaOH溶液与稀盐酸反应过程中温度和pH的变化.测定结果如图所示.下列说法不正确的是( ) A、反应过程中有热量放出 B、30s时,溶液中溶质为HCl和NaCl C、该实验是将稀盐酸滴入稀NaOH溶液 D、从20s到40s,溶液的温度升高、pH增大
A、反应过程中有热量放出 B、30s时,溶液中溶质为HCl和NaCl C、该实验是将稀盐酸滴入稀NaOH溶液 D、从20s到40s,溶液的温度升高、pH增大二、非选择题
-
21. A或B中两题中任选一个作答,若两题均作答,按A计分.
A补齐物质与其用途的连线
B补齐标识与其含义的连线

 22. 如图所示的内容是某品牌饼干的配料.
22. 如图所示的内容是某品牌饼干的配料. (1)、配料中属于油脂的是 .(2)、碳酸氢钠的俗称是 .23. 葡萄的果肉和果皮中都含有丰富的营养物质.(1)、为使葡萄果实饱满、提高含糖量,在葡萄生长的中后期可适当施加硫酸钾、过磷酸钙等肥料,其中硫酸钾属于化学肥料中的肥.(2)、用硫酸铜配制的农药波尔多液,可以防治葡萄生长中的病害.溶解硫酸铜时不宜用铁制容器,用化学方程式表示其原因: .(3)、食用葡萄前要清洗干净,如图是一种清洗的方法.
(1)、配料中属于油脂的是 .(2)、碳酸氢钠的俗称是 .23. 葡萄的果肉和果皮中都含有丰富的营养物质.(1)、为使葡萄果实饱满、提高含糖量,在葡萄生长的中后期可适当施加硫酸钾、过磷酸钙等肥料,其中硫酸钾属于化学肥料中的肥.(2)、用硫酸铜配制的农药波尔多液,可以防治葡萄生长中的病害.溶解硫酸铜时不宜用铁制容器,用化学方程式表示其原因: .(3)、食用葡萄前要清洗干净,如图是一种清洗的方法.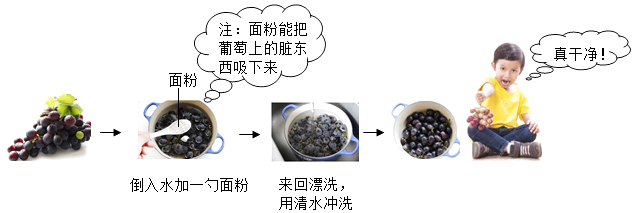
下列说法正确的是 (填序号).
A、面粉有利于去除葡萄皮上的脏东西 B、清洗干净后,建议吃葡萄不吐葡萄皮 C、葡萄富含糖类物质,糖尿病人不宜多食.24. 电解水实验如图所示.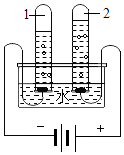 (1)、试管2中生成的气体为(2)、该反应的化学方程式为 .25. 太阳能吸附式制冷结露法空气取水器可用于野外获取淡水,工作原理如图所示.
(1)、试管2中生成的气体为(2)、该反应的化学方程式为 .25. 太阳能吸附式制冷结露法空气取水器可用于野外获取淡水,工作原理如图所示.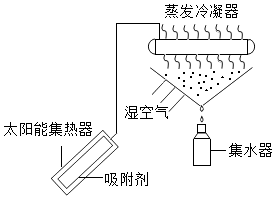 (1)、蒸发冷凝器中发生的是(填“物理”或“化学”)变化.(2)、吸附剂中主要物质为SiO2和CaCl2 , SiO2中硅元素的化合价为 , CaCl2中钙、氯元素的质量比为 .26. 2017年5月我国海域可燃冰试采获得成功.可燃冰(天然气水合物)是资源量丰富的高效清洁能源,能释放出天然气.(1)、生活中,可以利用天然气(主要成分是甲烷)获得热量.甲烷燃烧的化学方程式为 .(2)、工业上,可以利用甲烷获得氢气,其反应的微观示意图如下:
(1)、蒸发冷凝器中发生的是(填“物理”或“化学”)变化.(2)、吸附剂中主要物质为SiO2和CaCl2 , SiO2中硅元素的化合价为 , CaCl2中钙、氯元素的质量比为 .26. 2017年5月我国海域可燃冰试采获得成功.可燃冰(天然气水合物)是资源量丰富的高效清洁能源,能释放出天然气.(1)、生活中,可以利用天然气(主要成分是甲烷)获得热量.甲烷燃烧的化学方程式为 .(2)、工业上,可以利用甲烷获得氢气,其反应的微观示意图如下:
①图1所示反应的化学方程式为 .
②在图2横线处补全相应微粒的图示.
27. 载人航天器工作舱中的空气要与地球上的空气基本一致.资料:在同温同压下,气体的体积之比等于分子个数之比.
(1)、用微观示意图表示工作舱中空气的主要成分,下图中最合理的是(填序号). (2)、宇航员呼出的CO2用氢氧化锂(LiOH)吸收,生成Li2CO3和H2O,反应的化学方程式为(3)、航天器返回地面后,用Ca(OH)2与Li2CO3发生复分解反应,使(填化学式)再生.28. 阅读下面科普短文.
(2)、宇航员呼出的CO2用氢氧化锂(LiOH)吸收,生成Li2CO3和H2O,反应的化学方程式为(3)、航天器返回地面后,用Ca(OH)2与Li2CO3发生复分解反应,使(填化学式)再生.28. 阅读下面科普短文.说起二氧化硫(SO2),你可能首先想到它是空气质量播报中提及的大气污染物.其实你真的了解SO2吗?难道它只是有害物质吗?
SO2与食品工业
SO2作为防腐剂、漂白剂和抗氧化剂广泛用于食品行业.葡萄酒酿制中适量添加SO2 , 可防止葡萄酒在陈酿和贮藏过程中被氧化,抑制葡萄汁中微生物的活动.食糖加工过程中可使用SO2进行脱色.按照我国《食品添加剂使用标准(GB2760﹣2014)》,合理使用SO2不会对人体健康造成危害.
标准中部分食品SO2的最大残留量
食品
蜜饯
葡萄酒
食糖
水果干
巧克力
果蔬汁
最大残留量
0.35g/kg
0.25g/L
0.1g/kg
0.1g/kg
0.1g/kg
0.05g/kg
SO2与硫酸工业
硫酸是重要的化工原料,工业制硫酸的关键步骤是SO2的获取和转化.工业利用硫制硫酸的主要过程示意如下:

硫酸工业的尾气中含有少量SO2 , 若直接排放会污染空气,并导致硫酸型酸雨.工业上可先用氨水吸收,再用硫酸处理,将重新生成的SO2循环利用.
SO2与化石燃料
化石燃料中的煤通常含有硫元素,直接燃烧会产生SO2 . 为了减少煤燃烧产生的SO2污染空气,可以采取“提高燃煤质量,改进燃烧技术”的措施,例如,对燃煤进行脱硫、固硫处理;还可以采取“优化能源结构、减少燃煤使用”的措施,例如,北京大力推广的“煤改气、煤改电”工程,有效改善了空气质量.
现在,你对SO2一定有了新的认识,在今后的化学学习中你对SO2还会有更全面的认识!
依据文章内容回答下列问题.
(1)、按照国家标准,食糖中的SO2最大残留量为g/kg.(2)、葡萄酒酿制过程中SO2的作用是 .(3)、用硫制硫酸的主要过程中,涉及到的含硫物质有S、和H2SO4 .(4)、硫酸工业生产中,吸收尾气中SO2的物质是(5)、下列措施能减少SO2排放的是 (填序号).A、将煤块粉碎 B、对燃煤进行脱硫 C、推广煤改气、煤改电 D、循环利用工业尾气中的SO2 .29. 超细碳酸钙可用于生产钙片、牙膏等产品.利用碳化法生产超细碳酸钙的主要流程示意如下: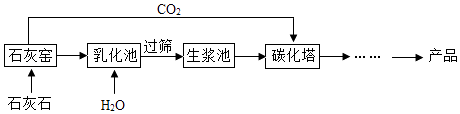 (1)、石灰石主要成分的化学式为 .(2)、乳化池中,生石灰与水发生反应,其化学方程式为(3)、过筛的目的是拦截(填“大于”或“小于”)筛孔直径的颗粒.(4)、碳化塔中反应的化学方程式为30. 工业上用硫铁矿烧渣(主要成分是Fe3O4、Fe2O3等)、煤粉作原料制备FeCO3的主要流程如下:
(1)、石灰石主要成分的化学式为 .(2)、乳化池中,生石灰与水发生反应,其化学方程式为(3)、过筛的目的是拦截(填“大于”或“小于”)筛孔直径的颗粒.(4)、碳化塔中反应的化学方程式为30. 工业上用硫铁矿烧渣(主要成分是Fe3O4、Fe2O3等)、煤粉作原料制备FeCO3的主要流程如下: (1)、焙烧炉中,发生的主要反应为:
(1)、焙烧炉中,发生的主要反应为:①3C+2O2 2CO+CO2
②Fe2O3+CO 2FeO+CO2
③Fe3O4+CO=3FeO+CO2
上述反应中的各物质,碳元素呈现种化合价.
(2)、酸浸槽中,FeO转化为FeSO4 , 加入的物质X是 .(3)、主反应器中,生成FeCO3的反应物为 .31. 如图为“领取奖杯游戏”的物质阶梯.当阶梯上相邻的物质之间能发生反应,方可向上攀登.例如,攀登阶梯甲能领取奖杯.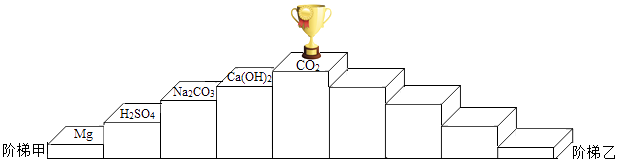 (1)、认识阶梯甲
(1)、认识阶梯甲①阶梯上的5种物质中,属于氧化物的是 , 俗称纯碱的是 .
②攀登过程中,H2SO4与Na2CO3发生反应的化学方程式为 .
(2)、搭建阶梯乙请你从O2、Fe、Fe2O3、HCl、NaOH中选择4种物质,写在图中相应的台阶上,能领取奖杯.
(3)、共享物质、重塑阶梯阶梯乙搭建完成后,若在阶梯甲和阶梯乙中各选择一种物质进行互换,也均能领取奖杯,则这两种物质是(任写一组即可).
32. 如右图所示,电子秤上的量筒中分别盛有蒸馏水、浓硫酸,放置一段时间. (1)、A中示数变小,从微粒的角度解释其原因是 .(2)、B中示数(填“变大”“不变”或“变小”),其原因是 .33. 如图所示,在白色点滴板1﹣6的孔穴中,分别滴加2滴紫色石蕊溶液.
(1)、A中示数变小,从微粒的角度解释其原因是 .(2)、B中示数(填“变大”“不变”或“变小”),其原因是 .33. 如图所示,在白色点滴板1﹣6的孔穴中,分别滴加2滴紫色石蕊溶液. (1)、孔穴6中溶液变为蓝色,说明碳酸钾溶液显(填“酸性”或“碱性”).(2)、溶液变为红色的孔穴有(填孔穴序号,下同).(3)、作为空白对照实验的孔穴是(4)、再向孔穴4中滴加稀硫酸,溶液变为紫色,用化学方程式解释其原因:34.
(1)、孔穴6中溶液变为蓝色,说明碳酸钾溶液显(填“酸性”或“碱性”).(2)、溶液变为红色的孔穴有(填孔穴序号,下同).(3)、作为空白对照实验的孔穴是(4)、再向孔穴4中滴加稀硫酸,溶液变为紫色,用化学方程式解释其原因:34.利用下图所示装置进行实验.
 (1)、打开K1 , 观察到蜡烛;A中发生反应的化学方程式为 .(2)、关闭K1、打开K2 , 观察到蜡烛缓慢的熄灭.蜡烛熄灭的原因是 .35. 请从A或B两题中任选一个作答,若两题均作答,按35﹣A计分.
(1)、打开K1 , 观察到蜡烛;A中发生反应的化学方程式为 .(2)、关闭K1、打开K2 , 观察到蜡烛缓慢的熄灭.蜡烛熄灭的原因是 .35. 请从A或B两题中任选一个作答,若两题均作答,按35﹣A计分.A用浓硫酸配制100g 9.8%的稀硫酸
B粗盐中难溶性杂质的去除
(1 )实验需要5.4mL浓硫酸和90mL水.量取两种液体用到的仪器有(填序号).
(2 )稀释时,需将浓硫酸缓慢倒入水中,并不断进行搅拌,其原因是 .
(1 )过滤需要用到的仪器有(填序号).
(2 )蒸发过程中,需不断进行搅拌,其原因是 .
可供选择的主要仪器:
①试管 ②烧杯 ③蒸发皿 ④托盘天平 ⑤10mL量筒 ⑥100mL量筒
⑦药匙 ⑧胶头滴管 ⑨漏斗 ⑩酒精灯⑪铁架台⑫玻璃棒
36. 如图所示,调节杠杆平衡.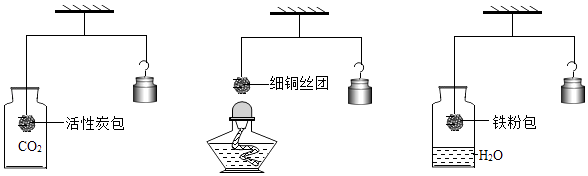 (1)、实验1:通入CO2一段时间后,活性炭包下沉,原因是(2)、实验2:加热细铜丝团一段时间后移走酒精灯,观察到铜丝变为黑色(CuO),细铜丝团(填“上升”或“下沉”).(3)、实验3:一段时间后,铁粉包下沉,是因为铁粉与发生反应.37. 利用下图装置进行实验(两支玻璃管内径相同).实验前K1、K2、K3均已关闭.
(1)、实验1:通入CO2一段时间后,活性炭包下沉,原因是(2)、实验2:加热细铜丝团一段时间后移走酒精灯,观察到铜丝变为黑色(CuO),细铜丝团(填“上升”或“下沉”).(3)、实验3:一段时间后,铁粉包下沉,是因为铁粉与发生反应.37. 利用下图装置进行实验(两支玻璃管内径相同).实验前K1、K2、K3均已关闭.实验装置
【实验1】制备气体
【实验2】测定空气中氧气含量
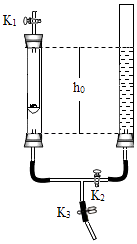
左管中带孔的燃烧匙盛有足量锌粒,右管盛有稀硫酸
Ⅰ.打开K1和K2 , 使反应发生
Ⅱ.在K1的导管口处收集气体
Ⅲ.…
左管中燃烧匙盛有足量白磷,右管盛有水
Ⅰ.光照引燃白磷
Ⅱ.待白磷熄灭,冷却,打开K2 , 至液面不再变化,右管中液体的高度为h1
(1)、实验1:锌与稀硫酸反应的化学方程式为;为使反应停止,Ⅲ中的操作是 .(2)、实验2:打开K2 , 右管中液面下降,原因是;计算空气中氧气体积分数的表达式为(用h0、h1表示).38. 高锰酸钾在生产、生活中有广泛应用.实验小组对高锰酸钾的某些性质进行研究.(1)、Ⅰ.不稳定性如图所示进行实验,受热分解的化学方程式为 , 3.16g KMnO4产生O2的质量为g.
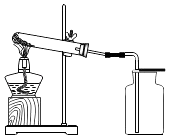 (2)、用向上排空气法收集O2的原因是 .(3)、Ⅱ.腐蚀性
(2)、用向上排空气法收集O2的原因是 .(3)、Ⅱ.腐蚀性【查阅资料】KMnO4溶液呈中性、有腐蚀性
【进行实验】
实验1:将新鲜鸡皮在不同浓度的KMnO4溶液中浸泡相同时间,现象如表
KMnO4溶液浓度
0.002%
0.01%
0.1%
1%
鸡皮的变化
无明显变化
边缘部分变为棕黄色
全部变为棕色
全部变为黑色
实验2:将铜片分别浸泡在4种浸泡相同时间,现象如下表.
编号
①
②
③
④
实验
25mL0.1%KMnO4溶液

25mL0.1%KMnO4溶液+10滴浓硫酸

25mL蒸馏水+10滴浓硫酸

25mL1%KMnO4溶液+10滴浓硫酸
铜片
质量/g
实验前
0.54
0.54
0.54
0.54
18小时后
0.54
0.52
0.54
0.43
【解释与结论】
实验1的目的是
(4)、实验2中通过对比②和④,得出的结论是 .(5)、实验2中,欲得出“KMnO4和硫酸共同作用对铜才有腐蚀性”的结论,需要对比(填编号).(6)、实验2中,铜片被腐蚀的反应如下,补全该反应的化学方程式.5Cu+2KMnO4+8H2SO4=5CuSO4+2MnSO4+K2SO4+ .