浙江省杭州市2018-2019学年八年级下学期科学期中考试试卷
试卷更新日期:2020-01-02 类型:期中考试
一、选择题(共22题,每题3分,共66分)
-
1. 历史上,安培曾经提出分子环形电流的假说来解释为什么磁体具有磁性,他认为在物质微粒的内部存在着一种环形的分子电流,分子电流会形成磁场,使分子相当于一个小磁体(如图所示)。根据安培的这一假说,以下说法正确的是( )
 A、这一假说能够说明磁可以生电 B、这一假说能够说明磁现象产生的本质 C、未磁化的物体,其微粒内部不含有这样的环形电流 D、磁化的物体,其微粒内部环形电流的方向是杂乱无章的2. 如图所示,用磁体的一极在钢棒上沿同一方向摩擦几次,可以使钢棒磁化。关于钢棒的磁极,下列说法中正确的是( )
A、这一假说能够说明磁可以生电 B、这一假说能够说明磁现象产生的本质 C、未磁化的物体,其微粒内部不含有这样的环形电流 D、磁化的物体,其微粒内部环形电流的方向是杂乱无章的2. 如图所示,用磁体的一极在钢棒上沿同一方向摩擦几次,可以使钢棒磁化。关于钢棒的磁极,下列说法中正确的是( ) A、若用磁体N极去摩擦钢棒,则钢棒左端为N极,右端为S极 B、若用磁体N极去摩擦钢棒,则钢棒左端为S极,右端为N极 C、若用磁体S极去摩擦钢棒,则钢棒左端为N极,右端为S极 D、以上说法都不对3. 如图所示,在水平放置的光滑绝缘杆ab上,挂有两个相同的金属环M和N。当两环均通以图示的相同方向的电流时,分析下列说法中,哪种说法是正确( )
A、若用磁体N极去摩擦钢棒,则钢棒左端为N极,右端为S极 B、若用磁体N极去摩擦钢棒,则钢棒左端为S极,右端为N极 C、若用磁体S极去摩擦钢棒,则钢棒左端为N极,右端为S极 D、以上说法都不对3. 如图所示,在水平放置的光滑绝缘杆ab上,挂有两个相同的金属环M和N。当两环均通以图示的相同方向的电流时,分析下列说法中,哪种说法是正确( ) A、静止不动 B、两环互相靠近 C、两环互相远离 D、两环同时向左运动4. 二十世纪初,为了研究物质内部的结构,物理学家做了大量的实验,揭示了原子内部的结构。发现了电子、中子和质子,如图所示是( )
A、静止不动 B、两环互相靠近 C、两环互相远离 D、两环同时向左运动4. 二十世纪初,为了研究物质内部的结构,物理学家做了大量的实验,揭示了原子内部的结构。发现了电子、中子和质子,如图所示是( ) A、卢瑟福的α粒子散射实验装置 B、卢瑟福发现质子的实验装置 C、汤姆逊发现电子的实验装置 D、查德威克发现中子的实验装置5. 关于家庭电路中电流大小的说法,正确的是( )A、家庭电路中的电流大小,由保险丝粗细决定,保险丝粗的电流大 B、家庭电路中的电流大小,由导线的粗细决定,导线较粗的电流大 C、家庭电路中的电流大小,由连入家庭电路中的用电器个数决定,个数多的电流大 D、以上说法均错误6. 在下列实验操作(或措施)与理由的关系中,正确的是( )A、做电解水实验时,向水中加入少量氢氧化钠溶液--反应加快,因氢氧化钠是催化剂 B、探究空气中氧气含量试验中红磷要足量--充分观察磷在空气中燃烧的现象 C、实验室制取蒸馏水时在蒸馏瓶中放入沸石--加快蒸馏速度 D、实验室用排水法收集氧气时要等气泡均匀连续放出再收集--防止收集到的气体不纯7. 如图是杋场的安检人员用手持金属探测器检查乘客的情景,当探测线圈靠近金属物体时,在金属物体中就会产生电流,如果能检测出这种变化,就可以判定探测线圈下面有金属物体了。图中能反映出金属探测器工作原理的是( )
A、卢瑟福的α粒子散射实验装置 B、卢瑟福发现质子的实验装置 C、汤姆逊发现电子的实验装置 D、查德威克发现中子的实验装置5. 关于家庭电路中电流大小的说法,正确的是( )A、家庭电路中的电流大小,由保险丝粗细决定,保险丝粗的电流大 B、家庭电路中的电流大小,由导线的粗细决定,导线较粗的电流大 C、家庭电路中的电流大小,由连入家庭电路中的用电器个数决定,个数多的电流大 D、以上说法均错误6. 在下列实验操作(或措施)与理由的关系中,正确的是( )A、做电解水实验时,向水中加入少量氢氧化钠溶液--反应加快,因氢氧化钠是催化剂 B、探究空气中氧气含量试验中红磷要足量--充分观察磷在空气中燃烧的现象 C、实验室制取蒸馏水时在蒸馏瓶中放入沸石--加快蒸馏速度 D、实验室用排水法收集氧气时要等气泡均匀连续放出再收集--防止收集到的气体不纯7. 如图是杋场的安检人员用手持金属探测器检查乘客的情景,当探测线圈靠近金属物体时,在金属物体中就会产生电流,如果能检测出这种变化,就可以判定探测线圈下面有金属物体了。图中能反映出金属探测器工作原理的是( ) A、
A、 B、
B、 C、
C、 D、
D、 8. 如图所示,将大的条形磁铁中间挖去一块,放入一可以自由转动的小磁针,当小磁针静止时,它的N极应指向( )
8. 如图所示,将大的条形磁铁中间挖去一块,放入一可以自由转动的小磁针,当小磁针静止时,它的N极应指向( ) A、左边a B、右边c C、b边或d边 D、不能确定9. 如图所示是拍摄机动车辆闯红灯的工作原理示意图。光控开关接收到红灯发出的光会自动闭合,压力开关受到机动车的压力会闭合,摄像系统在电路接通时可自动拍摄违章车辆。下列有关说法正确是( )
A、左边a B、右边c C、b边或d边 D、不能确定9. 如图所示是拍摄机动车辆闯红灯的工作原理示意图。光控开关接收到红灯发出的光会自动闭合,压力开关受到机动车的压力会闭合,摄像系统在电路接通时可自动拍摄违章车辆。下列有关说法正确是( ) A、只要光控开关接收到红光,摄像系就会自动拍摄 B、机动车只要驶过埋有压力开关的路口,摄像系统就会自动拍摄 C、只有光控开关和压力开关都闭合时,摄像系统才会自动拍摄 D、若将光控开关和压力开关并联,也能起到相同的作用10. 元素X的原子结构示意图为
A、只要光控开关接收到红光,摄像系就会自动拍摄 B、机动车只要驶过埋有压力开关的路口,摄像系统就会自动拍摄 C、只有光控开关和压力开关都闭合时,摄像系统才会自动拍摄 D、若将光控开关和压力开关并联,也能起到相同的作用10. 元素X的原子结构示意图为 ,下列说法不正确的是( ) A、X的常见单质的化学式可表示为X2 B、X的常见单质具有可燃性 C、酒精在Ⅹ的常见单质中完全燃烧生成CX2和H2X D、在人体组织里,葡萄糖在酶的催化作用下跟ⅹ的常见单质反应产生供机体活动和维持恒定体温的能量11. 对于Fe、Fe2+、Fe3+三种粒子的判断,正确的是 ( )
,下列说法不正确的是( ) A、X的常见单质的化学式可表示为X2 B、X的常见单质具有可燃性 C、酒精在Ⅹ的常见单质中完全燃烧生成CX2和H2X D、在人体组织里,葡萄糖在酶的催化作用下跟ⅹ的常见单质反应产生供机体活动和维持恒定体温的能量11. 对于Fe、Fe2+、Fe3+三种粒子的判断,正确的是 ( )①核电荷数相同 ②核外电子数相等 ③电子层结构相同 ④质量几乎相等⑤所含的质子数相等
A、①③④⑤ B、②③④ C、①④⑤ D、③④⑤12. 如图所示的是直流发电机的工作原理图,关于直流发电机下列说法中正确的是( ) A、直流发电机线圈内产生的是交流电,供给外部电路的是直流电 B、直流发电机线圈内产生的是直流电,供给外部电路的也是直流电 C、它是利用通电线圈在磁场中受到力的作用而转动的原理工作的 D、图中的 E,F 称为换向器,它的作用是改变线圈中的电流方向13. 电影《流浪地球》中的行星发动机运行时,我们可以使用的主要燃料偏二甲肼(化学式为C2H8N2)下列有关说法正确的是( )A、偏二甲肼中含有氮分子 B、每个偏二甲肼分子由12个原子构成 C、偏二甲肼具有可燃性,完全燃烧产物是CO2和H2O D、偏二甲肼中氢元素和氮元素的质量比4:114. Ⅹ元素1个原子的质量是m克,Y元素的相对原子质量为A;化合物XY2的相对分子质量是M,则W克XY2中含有Y的原子数是( )A、 B、 C、 D、15. 下列4个图象分别表示对应的四种操作过程,其中正确的是( )A、加热氯酸钾制取氧气
A、直流发电机线圈内产生的是交流电,供给外部电路的是直流电 B、直流发电机线圈内产生的是直流电,供给外部电路的也是直流电 C、它是利用通电线圈在磁场中受到力的作用而转动的原理工作的 D、图中的 E,F 称为换向器,它的作用是改变线圈中的电流方向13. 电影《流浪地球》中的行星发动机运行时,我们可以使用的主要燃料偏二甲肼(化学式为C2H8N2)下列有关说法正确的是( )A、偏二甲肼中含有氮分子 B、每个偏二甲肼分子由12个原子构成 C、偏二甲肼具有可燃性,完全燃烧产物是CO2和H2O D、偏二甲肼中氢元素和氮元素的质量比4:114. Ⅹ元素1个原子的质量是m克,Y元素的相对原子质量为A;化合物XY2的相对分子质量是M,则W克XY2中含有Y的原子数是( )A、 B、 C、 D、15. 下列4个图象分别表示对应的四种操作过程,其中正确的是( )A、加热氯酸钾制取氧气 B、二氧化锰与氯酸钾共热时二氧化锰的质量分数随反应时间的变化图象
B、二氧化锰与氯酸钾共热时二氧化锰的质量分数随反应时间的变化图象  C、红磷在密闭容器中燃烧时容器内物质的质量变化
C、红磷在密闭容器中燃烧时容器内物质的质量变化  D、红磷在密闭容器中燃烧时氧气含量的变化情况
D、红磷在密闭容器中燃烧时氧气含量的变化情况  16. 某密闭容器中有X、氧气和二氧化碳三种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表。根据表中信息,判断下列说法正确的是( )
16. 某密闭容器中有X、氧气和二氧化碳三种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表。根据表中信息,判断下列说法正确的是( )物质
X
O2
CO2
H2O
反应前质量/g
16
70
1
0
反应后质量/g
0
待测
45
36
A、该反应为置换反应 B、Ⅹ中一定含有碳、氢两种元素 C、表中“待测”值为5 D、反应生成的CO2和H2O的质量比为45:3617. 下列物质的一步转化过程不符合A B→C的是( )A、CO CO2→CaCO3 B、CO2 C16H12O6→H2O C、O2 H2O+H2 D、H2O O2→FeO18. 如图表示一定质量的KClO3和MnO2固体混合物受热过程中,某变量y随时间的变化趋势。纵坐标表示的是( )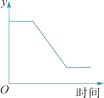 A、固体中氧元素的质量 B、生成O2的质量 C、固体中MnO2的质量 D、固体中钾元素的质量分数19. 如图,在密封的纸盒上挖一个直径10cm的圆形小洞,并在洞口前方约1米的位置,放置一根点燃的蜡烛,用双手在纸盒两侧拍击,蜡烛熄灭。蜡烛熄灭的主要原因是( )
A、固体中氧元素的质量 B、生成O2的质量 C、固体中MnO2的质量 D、固体中钾元素的质量分数19. 如图,在密封的纸盒上挖一个直径10cm的圆形小洞,并在洞口前方约1米的位置,放置一根点燃的蜡烛,用双手在纸盒两侧拍击,蜡烛熄灭。蜡烛熄灭的主要原因是( ) A、缺乏可燃物 B、缺乏O2 C、排出的气流中CO2的含量高 D、温度降到了可燃物的着火点以下20. 下列探究实验中,与制造电风扇的原理相同的是( )A、通电导体在磁场中受力运动
A、缺乏可燃物 B、缺乏O2 C、排出的气流中CO2的含量高 D、温度降到了可燃物的着火点以下20. 下列探究实验中,与制造电风扇的原理相同的是( )A、通电导体在磁场中受力运动 B、同种电荷相互排斥
B、同种电荷相互排斥  C、导体在磁场中左右运动时,电流表指针偏转
C、导体在磁场中左右运动时,电流表指针偏转  D、不同的电磁铁吸引的小铁钉数目不同
D、不同的电磁铁吸引的小铁钉数目不同  21. 小明在学习家庭电路时,安装了两盏白炽灯和两个插座,如图所示。如果两插座中均连入家用电器,且将电路中的开关全部闭合,那么各用电器工作的情况是( )
21. 小明在学习家庭电路时,安装了两盏白炽灯和两个插座,如图所示。如果两插座中均连入家用电器,且将电路中的开关全部闭合,那么各用电器工作的情况是( ) A、甲、乙、丙、丁都正常工作 B、只有甲、乙、丁正常工作 C、只有甲正常工作 D、只有乙正常工作22. 下列是某位同学对阶段学习的有关内容的归纳:①工业上采用分离液态空气法制取氧气②氧气不易溶于水,故可以用排水法收集;③物质与氧气的反应都属于氧化反应;④制取任何气体之前应先检查装置的气密性;⑤氧气的用途很多,比如可以做燃料;⑥分子和原子的本质区别是分子可分,原子不可分。该同学归纳正确的是( )A、①②④ B、①②③④ C、②③④⑥ D、①②③④⑤⑥
A、甲、乙、丙、丁都正常工作 B、只有甲、乙、丁正常工作 C、只有甲正常工作 D、只有乙正常工作22. 下列是某位同学对阶段学习的有关内容的归纳:①工业上采用分离液态空气法制取氧气②氧气不易溶于水,故可以用排水法收集;③物质与氧气的反应都属于氧化反应;④制取任何气体之前应先检查装置的气密性;⑤氧气的用途很多,比如可以做燃料;⑥分子和原子的本质区别是分子可分,原子不可分。该同学归纳正确的是( )A、①②④ B、①②③④ C、②③④⑥ D、①②③④⑤⑥二、填空题(共8题,共37分)
-
23. 如图所示,甲、乙为两根外形相同的钢棒,当乙从甲的左端水平向右移到右端,若两根钢棒间吸引力的大小不变,则棒有磁性;若两钢棒间吸引力先由大变小,然后由小变大,则棒有磁性。
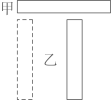 24. 如下图所示,甲乙为条形磁体,中间是电磁体,虚线是表示磁板间磁场分布情况的磁感线,则可以判断图中A、B、C、D四个磁极依次是 , , , 。
24. 如下图所示,甲乙为条形磁体,中间是电磁体,虚线是表示磁板间磁场分布情况的磁感线,则可以判断图中A、B、C、D四个磁极依次是 , , , 。 25. 用化学符号填空:2个氮原子;n个钠离子;3个硫酸根离子 ;地壳中含量最多的金属元素与最多的非金属元素组成化合物的化学式;(“●"表示氢原子,“○”表示氧原子)
25. 用化学符号填空:2个氮原子;n个钠离子;3个硫酸根离子 ;地壳中含量最多的金属元素与最多的非金属元素组成化合物的化学式;(“●"表示氢原子,“○”表示氧原子) 表示;氯化亚铁中铁元素的化合价为+2 。 26.(1)、某三价金属与氧元素形成的化合物中氧元素质量分数为30%,则该金属的相对原子质量为。(2)、A、B两元素相对原子质量之比为2:1,仅由这两种元素组成的化合物里,A、B两元素质量比为2:3,则该化合物的化学式为;若其中B为-n价,则此化合物中A元素的化合价为。(3)、元素R可与氧形成多种化合物,其中RO中含氧53.3%,那么相对分子质量为76,含氧量为63.16%的R与氧元素形成的化合物的化学式是。27. 如图所示是磁带录音机录音原理的示意图。请根据原理图试解释磁带录音机的录音原理。录音时,话筒将信号转换为信号(利用了原理)送到录音磁头;录音磁头是一个蹄形 , 它的磁性强弱随电信号变化,将信号转换为信号(利用了电流的效应);录音磁带贴着录音磁头移动,上面的磁粉被 , 声音信号被记录在磁带上,从而实现录音功能。
表示;氯化亚铁中铁元素的化合价为+2 。 26.(1)、某三价金属与氧元素形成的化合物中氧元素质量分数为30%,则该金属的相对原子质量为。(2)、A、B两元素相对原子质量之比为2:1,仅由这两种元素组成的化合物里,A、B两元素质量比为2:3,则该化合物的化学式为;若其中B为-n价,则此化合物中A元素的化合价为。(3)、元素R可与氧形成多种化合物,其中RO中含氧53.3%,那么相对分子质量为76,含氧量为63.16%的R与氧元素形成的化合物的化学式是。27. 如图所示是磁带录音机录音原理的示意图。请根据原理图试解释磁带录音机的录音原理。录音时,话筒将信号转换为信号(利用了原理)送到录音磁头;录音磁头是一个蹄形 , 它的磁性强弱随电信号变化,将信号转换为信号(利用了电流的效应);录音磁带贴着录音磁头移动,上面的磁粉被 , 声音信号被记录在磁带上,从而实现录音功能。 28. 请根据下图回答问题:
28. 请根据下图回答问题: (1)、仪器A的名称是 , 仪器B的名称是。(2)、用KClO3与MnO2混合制取并收集纯净O2 , 应选用上图中的 (填序号),反应的化学方程式是。(3)、实验室制取并收集CO2 , 应选用上图中的(填序号),反应的化学方程式是;如何检验已集满一瓶CO2气体。29. 中国是全球第一个实现在海域“可燃冰”试开采中获得连续稳定产气的国家。“可燃冰”是甲烷和水在低温、高压条件下形成的水合物(CH4·nH2O)。(1)、在常温常压下,“可燃冰”会发生反应:CH4·nH2O=CH4+nH2O,该反应属于(填基本反应类型);(2)、甲烷可制成合成气(CO、H2),再制成甲醇(CH3OH),代替日益供应紧张的燃油。
(1)、仪器A的名称是 , 仪器B的名称是。(2)、用KClO3与MnO2混合制取并收集纯净O2 , 应选用上图中的 (填序号),反应的化学方程式是。(3)、实验室制取并收集CO2 , 应选用上图中的(填序号),反应的化学方程式是;如何检验已集满一瓶CO2气体。29. 中国是全球第一个实现在海域“可燃冰”试开采中获得连续稳定产气的国家。“可燃冰”是甲烷和水在低温、高压条件下形成的水合物(CH4·nH2O)。(1)、在常温常压下,“可燃冰”会发生反应:CH4·nH2O=CH4+nH2O,该反应属于(填基本反应类型);(2)、甲烷可制成合成气(CO、H2),再制成甲醇(CH3OH),代替日益供应紧张的燃油。由合成气制甲醇的反应方程式为: ,由甲烷制成合成气有两种方法:
① ;②
从原料配比角度比较方法①和②,更适宜用于合成甲醇的方法是(填序号)。
30. 在反应A+3B=2C+2D中,已知A和C的相对分子质量之比为7:11,一定量的A和B恰好完全反应后,生成4.4gC和1.8gD,则参加反应的A、B的质量之和为 , 参加反应的B的质量和生成D的质量比为 。三、实验、简答题(共4题,37分)
-
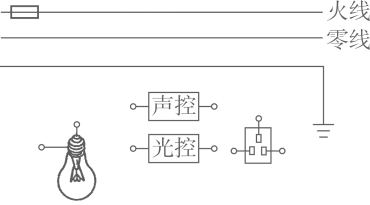
31. 居民楼的楼道里,夜间楼道灯一直亮着会造成浪费,科研人员用“光敏”材料制成“光控开关”,它能在天黑时自动闭合,天亮时自动断开;利用“声敏”材料制成“声控开关”,它能在有人走动发出声音时闭合,无人走动时自动断开。请将图中的“光控开关”、“声控开关”、灯泡用笔画线代替导线正确连入电路,要求只有在夜间有声音时灯才亮的自动控制电路,同时安装一个不受开关控制的三孔插座。
 32. 如图所示是小何同学探究电磁铁的磁性强弱跟哪些因素有关的实验装置,A是电磁铁,B是弹簧,C是铁块。图示中的弹簧长度为15cm。a、b两接线柱之间的线圈匝数是1500匝,a、c两接线柱之间的线圈匝数是2500匝。实验数据已记录在下表中。
32. 如图所示是小何同学探究电磁铁的磁性强弱跟哪些因素有关的实验装置,A是电磁铁,B是弹簧,C是铁块。图示中的弹簧长度为15cm。a、b两接线柱之间的线圈匝数是1500匝,a、c两接线柱之间的线圈匝数是2500匝。实验数据已记录在下表中。实验次数
通过螺线管电流/A
螺线管的匝数(选用接线柱)
弹簧长度/cm
1
1
a、b
16
2
1.5
a、b
17
3
2
a、b
17.8
4
2
a、c
18.5
 (1)、此实验通过比较弹簧B被拉长的长度来判断弹簧所受拉力的大小,从而就可以判断通电螺线管的强弱,这种科学方法通常叫做法。(2)、通过分析第1、2、3次实验数据,你可得出的结论是:当相同时,通过螺线管中的越大,弹簧B被拉长的越长,通电螺线管的磁性。(3)、通过分析第3、4次实验数据,你可得出的结论是。33. 四硫化钠(Na2S4)固体可替代红磷测定空气中氧气的体积分数,反应原理为2Na2S4+O2+2H2O=8S↓+4NaOH
(1)、此实验通过比较弹簧B被拉长的长度来判断弹簧所受拉力的大小,从而就可以判断通电螺线管的强弱,这种科学方法通常叫做法。(2)、通过分析第1、2、3次实验数据,你可得出的结论是:当相同时,通过螺线管中的越大,弹簧B被拉长的越长,通电螺线管的磁性。(3)、通过分析第3、4次实验数据,你可得出的结论是。33. 四硫化钠(Na2S4)固体可替代红磷测定空气中氧气的体积分数,反应原理为2Na2S4+O2+2H2O=8S↓+4NaOH【査阅资料】①Na2S4受热时,会与空气中的水蒸气反应,生成少量有毒气体硫化氢
②硫代硫酸钠(Na2S2O3)可溶于水,常温下与NaOH溶液不反应。
③NaOH溶液可吸收硫化氢和二氧化碳。
【实验过程】

①取0.5g碳酸钠、0.2g硫粉混合后置于试管中,加入(如图①所示,夹持装置已略去),制得Na2S4 , 反应为:4Na2CO3+12S+X 2Na2S4+2Na2S2O3+4CO2 , X的化学式为。
②冷却后,取下棉花,放置一段时间,再向该试管中加入10mL水,迅速塞紧橡胶塞,充分振荡。测量液面至橡胶塞下沿的距离,记录数据h1(如图②所示);
③将该试管插入水中(如图③所示),拔下橡胶塞,观察到 , 塞紧橡胶塞。将试管取出,倒转过来,测量液面至橡胶塞下沿的距离h2 , 记录数据h2。理论上h2:h1= ;
④按照①~③再重复实验2次。3次实验数据如下表所示。
第1次
第2次
第3次
h1/cm
11.0
11.4
11.6
h2/cm
8.7
9.1
9.2
【解释与结论】根据第1次实验数据,计算空气中氧气的体积分数为%(结果精确到0.1%);
【反思与评价】实验过程①中浓NaOH溶液的作用是;若实验过程②中,取下棉花后,未放置一段时间即进行后续操作,测定结果(填“偏大”、“偏小”或“无影响”),理由是:。
34. 硅的原子结构示意图,如图所示纯硅是通过以下过程制取的:
(一)制粗硅:①SiO2(石英砂)+2C(焦炭) Si(粗硅)+2CO↑
(二)制纯硅:②Si(粗)+2Cl2 SiCl4③SiCl4+2H2 Si(纯)+4HCl
纯净的无色透明的硅的氧化物(SiO2)晶体就是通常所说的水晶,这也许你不熟悉,但说起沙子,你一定不会陌生,沙子的主要成分即是SiO2 , SiO2的化学性质与CO2有些类似
请根据以上信息,回答以下问题:
(1)、X的值为 。(2)、推断SiO2的物理性质(三点即可)、、。(3)、请写出SiO2与NaOH溶液反应的化学方程式:。(4)、在反应①②③中,②属于。(填基本反应类型)(5)、化学上将只要有元素的化合价发生了变化的化学反应就叫做氧化还原反应,氧化还原反应中含有化合价升高了的元素的反应物叫还原剂,反应①中的还原剂是(写化学式)。四、分析、计算题(共3题,20分)
-
35. 根据题意回答问题:(1)、用质量守恒定律解释:镁带燃烧后生成物的质量增加(2)、若用镁带燃烧来验证质量守恒定律,应如何改进实验裝置?36. 把超强磁铁分别吸附在干电池的正负极两端,制成电磁动力“小车”,并将它放入铜质螺线管中,如图甲,“小车”就能沿着螺线管运动。图乙是它的示意图。
 (1)、在图乙上画出螺线管中的电流方向。(2)、实验中发现,必须将“小车”全部推入螺线管,“小车”才能运动,“小车”运动的原因是。(3)、进一步探究发现,“小车”运动的方向与电池正负极位置和超强磁铁的极性有关。将如图乙装配的小车放入螺线,则小车的运动方向是。(4)、要使“小车”运动速度增大,请提出一种方法:。37. 水在很多实验中都有着非常重要的作用,请对下列实验指定容器中的水做出相应的解释。
(1)、在图乙上画出螺线管中的电流方向。(2)、实验中发现,必须将“小车”全部推入螺线管,“小车”才能运动,“小车”运动的原因是。(3)、进一步探究发现,“小车”运动的方向与电池正负极位置和超强磁铁的极性有关。将如图乙装配的小车放入螺线,则小车的运动方向是。(4)、要使“小车”运动速度增大,请提出一种方法:。37. 水在很多实验中都有着非常重要的作用,请对下列实验指定容器中的水做出相应的解释。实验装置
硫在氧气中燃烧

测定空气中氧气含量

铁丝在氧气中燃烧

排水法收集氢气

解释
⒈集气瓶中的水:
⒉量筒中的水:
⒊集气瓶中的水:
⒋集气瓶中的水: