2017年贵州省遵义市汇川区中考化学模拟试卷
试卷更新日期:2017-08-01 类型:中考模拟
一、选择题
-
1. 下列实验仪器中,主要制作材料属于有机合成材料的是( )A、烧杯 B、塑料水槽 C、蒸发皿 D、铁架台2. 下列物质可作为氮肥的是( )A、CaCl2 B、Ca(H2PO4)2 C、NH4HCO3 D、K2SO43. 下列能源不属于化石燃料的是( )A、煤 B、氢气 C、石油 D、天然气4. 水果、蔬菜中富含的营养素是( )A、维生素 B、蛋白质 C、糖类 D、油脂5. 物质的性质决定用途,下列物质的用途中利用其物理性质的是( )A、活性炭作吸附剂 B、稀盐酸作除锈剂 C、生石灰作干燥剂 D、碘酒作消毒剂6. 类比归纳是学习化学的重要方法,以下说法中正确的是( )A、单质是由同种元素组成的,所以只含一种元素的物质一定是单质 B、在稀硫酸中有H+和SO42﹣ , 所以稀硫酸能导电 C、CO2和CO都是碳的氧化物,所以它们的化学性质相似 D、草木灰和碳酸氢铵是常用的肥料,所以将二者混合施用,可增加肥效7. 下列关于金属的说法正确的是( )A、铝制品抗腐蚀能力较铁制品弱 B、酸溶液可以保存在铁质容器中 C、用CuSO4溶液、Fe和Ag三种物质可以验证Fe、Cu、Ag三种金属的活动性强弱顺序 D、铁制品生锈产生的铁锈是一种疏松多孔的物质,它的主要成分是Fe3O48. 科学家发现火星大气层中含有一种称为硫化羰的物质,化学式为COS.已知硫化羰与二氧化碳的结构相似,但能在氧气中完全燃烧.下列有关硫化羰的说法错误的是( )
A、硫化羰是由分子构成的 B、硫化羰可作为理想燃料 C、硫化羰不能用作灭火剂 D、硫化羰完全燃烧会生成CO2和SO2两种氧化物9. 下列实验方案,实验设计达不到实验目的是( )方案
实验目的
实验设计
A
比较人体吸入的空气和呼出气体中氧气的含量
将燃着的木条分别插入空气样品和呼出气体的样品中
B
鉴别CO和CO2
分别通过灼热的CuO
C
验证燃烧的条件之一是温度要达到可燃物的着火点
用玻璃棒分别蘸取酒精和水,放在酒精灯火焰上加热片刻
D
除去CaCl2溶液中少量的盐酸
加入过量的碳酸钙,待没有气泡产生后,过滤
A、A B、B C、C D、D10. 某同学为了测定铜镁合金样品中铜的质量分数,将100g稀盐酸分2次加入到盛有5g该样品的烧杯中,所得数据如表,则下列说法中错误的是( )次数
实验前
第1次
第2次
加入稀盐酸的质量/g
0
50
50
剩余固体的质量/g
5
3
2
A、第1次加入稀盐酸后剩余固体中还有镁 B、第2次所加入的稀盐酸未反应完 C、每50g稀盐酸和1g镁恰好完全反应 D、合金样品中铜的质量分数为40%二、非选择题
-
11. 下表是我国生活饮用水的部分标准.
项目
标准
感官指标
无异味、异臭
化学指标
pH:6.5﹣8.5,游离氯≥0.3mg/L,铁<0.3mg/L…
(1)、感官指标表现的是自来水的 性质(填“物理”或“化学”);(2)、若化学指标中的pH=6.7时,表明自来水呈性;(3)、生活中可用来区别硬水和软水.12. 我国曾发生多次将工业用盐如亚硝酸钠(NaNO2)误作食盐用于烹调而引起的中毒事件.(1)、食盐主要成分的化学式为;(2)、亚硝酸钠和食盐中都含有的离子的化学符号是;(3)、亚硝酸钠与氯化铵共热能发生反应,其化学方程式为:NaNO2+NH4Cl NaCl+X↑+2H2O,则X的化学式为 , 该化学方程式里的含氮物质中,氮元素未表现出的化合价为价(填序号)A.+3 B.﹣3 C.0 D.+5.
13. 请根据图中所示实验装置回答问题.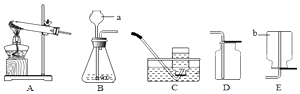 (1)、仪器a的名称为 , 在二氧化碳、氢气两种气体中,能用D装置收集的是;(2)、实验室用B装置制备氢气的原理可用化学方程式表示为(3)、用高锰酸钾制备氧气时,选用A时,有不足之处是 .14. “微观﹣宏观﹣符号”三重表征是化学独特的表示物质及其变化的方法,请结合图示完成下列问题:
(1)、仪器a的名称为 , 在二氧化碳、氢气两种气体中,能用D装置收集的是;(2)、实验室用B装置制备氢气的原理可用化学方程式表示为(3)、用高锰酸钾制备氧气时,选用A时,有不足之处是 .14. “微观﹣宏观﹣符号”三重表征是化学独特的表示物质及其变化的方法,请结合图示完成下列问题: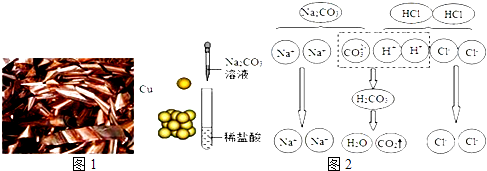 (1)、图1中,“Cu”表示多种信息,如表示铜元素、金属铜单质,还能表示;(2)、从微粒的角度说明图2反应的实质是;(3)、如图3所示,在一定条件下,A与B反应生成C和D,该反应的化学方程式为 .
(1)、图1中,“Cu”表示多种信息,如表示铜元素、金属铜单质,还能表示;(2)、从微粒的角度说明图2反应的实质是;(3)、如图3所示,在一定条件下,A与B反应生成C和D,该反应的化学方程式为 .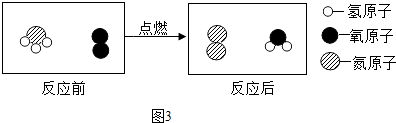 15. 乐乐查阅资料发现CaCl2可用作干燥剂.他设计了下面的转化方法,用CaCO3制得CaCl2 . 图中“→”表示物之间的转化关系,“→”上方为反应条件或参与反应的另一种物质.
15. 乐乐查阅资料发现CaCl2可用作干燥剂.他设计了下面的转化方法,用CaCO3制得CaCl2 . 图中“→”表示物之间的转化关系,“→”上方为反应条件或参与反应的另一种物质.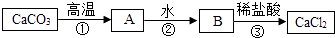
请回答下列问题:
(1)、A的化学式为;反应①②③都不涉及的基本反应类型是反应.(2)、牛牛认为CaCO3经一步反应就可以转化为CaCl2 , 反应的化学方程式为 .(3)、对比两同学的转化关系,我们发现熟练掌握物质的化学性质可以优化物质的转化途径.写出物质B经一步转化为CaCO3的化学方程式 .16.数型图象是研究化学问题的一种常见描述方法,根据下列图象进行回答:
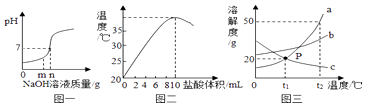 (1)、图一是用盐酸和氢氧化钠进行中和反应时,反应过程中溶液的pH变化曲线.向盐酸中加入的氢氧化钠溶液质量为mg时,所得溶液中含有的离子为(填离子符号);(2)、图二是20℃时,取10mL10%的NaOH溶液于烧杯中,逐滴加入10%的盐酸,随着盐酸的加入,烧杯中溶液温度与加入盐酸体积的变化关系.
(1)、图一是用盐酸和氢氧化钠进行中和反应时,反应过程中溶液的pH变化曲线.向盐酸中加入的氢氧化钠溶液质量为mg时,所得溶液中含有的离子为(填离子符号);(2)、图二是20℃时,取10mL10%的NaOH溶液于烧杯中,逐滴加入10%的盐酸,随着盐酸的加入,烧杯中溶液温度与加入盐酸体积的变化关系.①由图可知中和反应是放热反应,你的依据为;
②甲同学用氢氧化钠固体与稀盐酸反应也能得到相同结论,乙同学认为不严密,因为;
(3)、图三是a、b、c三种物质的溶解度曲线.a与c的溶解度相交于P点,据图回答:①t1℃时,接近饱和的c物质溶液,在不改变溶液质量的条件下,可用的方法达到饱和状态;
②将t2℃时,150ga物质的饱和溶液降温到t1℃时,可以析出ga物质.
17. 有C、Al、C2H6、H2SO4、NaOH、NaNO3六种物质.(1)、根据不同的分类标准,把它们进行如下分类:①属于有机物的是:C2H6②属于含氧化合物的是:H2SO4、NaOH、NaNO3
③含有钠元素的是:NaOH、NaNO3④属于金属单质的是:请你参照①~④的模式,写出另一种分类标准,并列出符合该标准的物质(从上面六种物质中选择):;
(2)、请你完成鉴别H2SO4、NaOH、NaNO3三种物质稀溶液的实验方案:(查阅资料:NaNO3溶液为无色,呈中性.)
实 验 步 骤
实 验 现 象
实 验 结 论
18. 实验设计是化学实验的重要环节,请根据下列实验要求回答相关问题:【活动与探究一】用对比实验方法探究二氧化碳的性质.
实验一
实验二

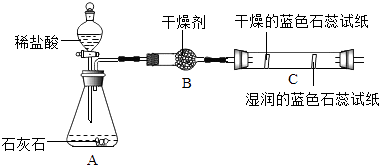 (1)、实验一中振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生反应的化学方程式为;对比A瓶与(填“B”或“C”) 瓶的实验现象,可证明CO2能与NaOH发生反应.(2)、实验二观察到C装置中发生的现象是 , 结论是(用语言表示).(3)、【活动与探究二】用变量控制方法探究影响物质溶解性的因素.
(1)、实验一中振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生反应的化学方程式为;对比A瓶与(填“B”或“C”) 瓶的实验现象,可证明CO2能与NaOH发生反应.(2)、实验二观察到C装置中发生的现象是 , 结论是(用语言表示).(3)、【活动与探究二】用变量控制方法探究影响物质溶解性的因素.实验三
实验四
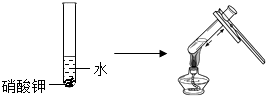
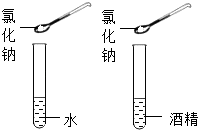
实验三目的是探究对硝酸钾溶解性的影响;实验四是探究对物质溶解性的影响.
19. 为测定某敞口放置的氢氧化钠溶液的变质情况,某同学实验并记录如图: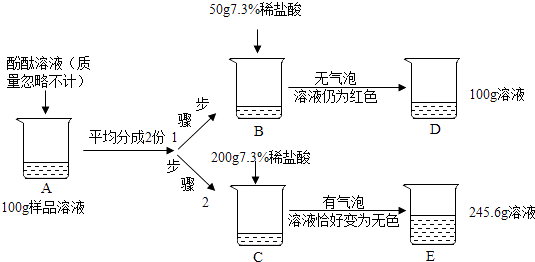 (1)、配置如图实验所用的稀盐酸,需要质量分数为36.5%的浓盐酸的质量是(2)、B烧杯中发生反应的化学方程式为;(3)、根据已知条件求解C烧杯溶液中碳酸钠质量(x)的比例式为;(4)、向E烧杯内加入54.4g水,所得不饱和溶液中溶质的质量分数为;(5)、D烧杯溶液中溶质的化学式为;(6)、原氢氧化钠溶液中变质的氢氧化钠与未变质的氢氧化钠质量比为 .
(1)、配置如图实验所用的稀盐酸,需要质量分数为36.5%的浓盐酸的质量是(2)、B烧杯中发生反应的化学方程式为;(3)、根据已知条件求解C烧杯溶液中碳酸钠质量(x)的比例式为;(4)、向E烧杯内加入54.4g水,所得不饱和溶液中溶质的质量分数为;(5)、D烧杯溶液中溶质的化学式为;(6)、原氢氧化钠溶液中变质的氢氧化钠与未变质的氢氧化钠质量比为 .