天津市津南区2019-2020学年九年级上学期化学期中考试试卷
试卷更新日期:2019-12-09 类型:期中考试
一、单选题
-
1. 下列变化属于化学变化的是()A、分离液态空气制氧气 B、蜡烛燃烧 C、水结冰 D、酒精挥发2. 地壳中含量最多的金属元素和非金属元素组成的物质的化学式是 ( )
A、Al2O3 B、AlO C、SiO2 D、FeO3. 下列有关物质分类的说法,正确的是( )A、单质:铁、水蒸气 B、化合物:过氧化氢、水银 C、氧化物:二氧化锰、冰水混合物 D、混合物:高锰酸钾、澄清的石灰水4. 下列图示的实验基本操作正确的是()A、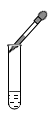 滴加液体
B、
滴加液体
B、 点燃酒精灯
C、
点燃酒精灯
C、 称量药品的质量
D、
称量药品的质量
D、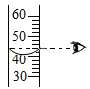 量取液体体积
5. 下列符号既能表示一种元素,又能表示该元素的一个原子,还能表示一种单质的是( )A、N2 B、He C、O D、2Fe6. 根据下列四种粒子的结构示意图,所获取的信息错误的是()
量取液体体积
5. 下列符号既能表示一种元素,又能表示该元素的一个原子,还能表示一种单质的是( )A、N2 B、He C、O D、2Fe6. 根据下列四种粒子的结构示意图,所获取的信息错误的是()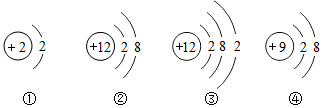 A、它们表示三种元素 B、②表示的是阴离子 C、③表示的元素是金属元素 D、①不带电,而④是带电的7. 下列家庭小实验,不能成功的是( )A、收集一玻璃杯的呼出气体 B、观察蜡烛燃烧的火焰 C、观察颜色区分白酒和白醋 D、煮沸使硬水变成软水8. 下列关于实验现象的叙述,正确的是( )A、硫在氧气中燃烧发出淡蓝色火焰 B、镁条燃烧发出耀眼白光 C、铁丝在空气中剧烈燃烧火星四射 D、蜡烛在氧气中燃烧,生成二氧化碳和水9. 2008年北京奥运会主体育场的外形好似“鸟巢”(The Bird Nest),有一类物质也好似鸟巢,如化学式是B5H9的五硼烷(如图)。下列有关五硼烷的说法错误的是()
A、它们表示三种元素 B、②表示的是阴离子 C、③表示的元素是金属元素 D、①不带电,而④是带电的7. 下列家庭小实验,不能成功的是( )A、收集一玻璃杯的呼出气体 B、观察蜡烛燃烧的火焰 C、观察颜色区分白酒和白醋 D、煮沸使硬水变成软水8. 下列关于实验现象的叙述,正确的是( )A、硫在氧气中燃烧发出淡蓝色火焰 B、镁条燃烧发出耀眼白光 C、铁丝在空气中剧烈燃烧火星四射 D、蜡烛在氧气中燃烧,生成二氧化碳和水9. 2008年北京奥运会主体育场的外形好似“鸟巢”(The Bird Nest),有一类物质也好似鸟巢,如化学式是B5H9的五硼烷(如图)。下列有关五硼烷的说法错误的是() A、五硼烷属于化合物 B、五硼烷的相对分子质量是64 C、五硼烷中硼元素和氢元素的质量比为5∶9 D、一个五硼烷分子由5个硼原子和9个氢原子构成10. 下列四个反应的生成物都是C,如果C的化学式为A2B5 , 则该反应的化学方程式为()A、2AB2+B2=2C B、3AB2+B2=2C C、4AB2+B2=2C D、AB2+4B2=2C11. 下列物质的鉴别方法错误的是( )A、用肥皂水鉴别硬水和软水 B、用红砖粉末鉴别蒸馏水和双氧水 C、用观察颜色的方法鉴别O2和SO2 D、用燃着的木条鉴别二氧化碳和氢气12. 卫星运载火箭的动力由高氯酸铵(NH4ClO4)发生反应提供,化学方程式为:2NH4ClO4 N2↑+Cl2↑+2O2↑+4X.则X的化学式是( )A、H2 B、H2O C、H2O2 D、HCl13. 某铁的氧化物中,铁元素的质量分数为70%,则该铁的氧化物中铁的化合价为( )A、+1 B、+2 C、+3 D、+414. 下列实验合理的是( )A、
A、五硼烷属于化合物 B、五硼烷的相对分子质量是64 C、五硼烷中硼元素和氢元素的质量比为5∶9 D、一个五硼烷分子由5个硼原子和9个氢原子构成10. 下列四个反应的生成物都是C,如果C的化学式为A2B5 , 则该反应的化学方程式为()A、2AB2+B2=2C B、3AB2+B2=2C C、4AB2+B2=2C D、AB2+4B2=2C11. 下列物质的鉴别方法错误的是( )A、用肥皂水鉴别硬水和软水 B、用红砖粉末鉴别蒸馏水和双氧水 C、用观察颜色的方法鉴别O2和SO2 D、用燃着的木条鉴别二氧化碳和氢气12. 卫星运载火箭的动力由高氯酸铵(NH4ClO4)发生反应提供,化学方程式为:2NH4ClO4 N2↑+Cl2↑+2O2↑+4X.则X的化学式是( )A、H2 B、H2O C、H2O2 D、HCl13. 某铁的氧化物中,铁元素的质量分数为70%,则该铁的氧化物中铁的化合价为( )A、+1 B、+2 C、+3 D、+414. 下列实验合理的是( )A、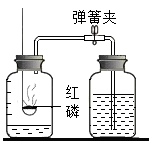 测定空气里氧气的含量
B、
测定空气里氧气的含量
B、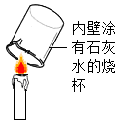 验证蜡烛含有碳元素
C、
验证蜡烛含有碳元素
C、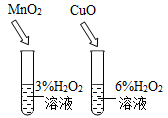 比较不同催化剂的催化效果
D、
比较不同催化剂的催化效果
D、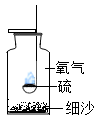 硫在氧气中燃烧
硫在氧气中燃烧
二、多选题
-
15. 下列说法错误的是( )A、墙内开花墙外香说明分子不断运动 B、镁的相对原子质量是24g C、物体的热胀冷缩现象说明分子遇热体积变大、遇冷体积变小 D、6000L氧气在加压情况下可装入容积为40L的钢瓶中说明分子间有间隔
三、填空题
-
16.(1)、矿物质水中元素及国标含量如下表所示,请用化学用语回答下列问题。
矿物质水中主要成分(mg/L)
偏硅酸
硫酸根
氯离子
钙
钠
钾
镁
①矿物质水中含有的镁元素;
②久置的水中溶有一定量的氧气,请表示出2个氧分子;
③表中的一种阴离子;
(2)、现有H、O、N、C四种元素,请选用其中的元素写出符合下列要求的物质各一个(用化学式表示):①焊接金属时常用作保护气的是﹔②人体中含量最多的物质;③供给呼吸的气体是。
17.(1)、溴元素在元素周期表中的信息与溴原子结构示意图如图1、2所示,则 。该元素属于(填“金属”、“非金属”或“稀有气体”),溴化钠的化学式为。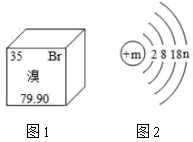 (2)、不同种元素最本质的区别是不同。18. 水和空气都是重要的自然资源(1)、下图为电解水的装置简图。
(2)、不同种元素最本质的区别是不同。18. 水和空气都是重要的自然资源(1)、下图为电解水的装置简图。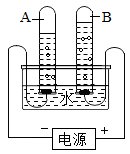
①通电一段时间后,A中的气体怎样检验;
②这个实验说明水是由组成的;反应的化学方程式是。
(2)、下图装置常用来测定空气中氧气的含量。下列认识正确的是______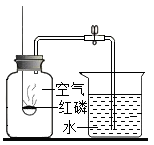 A、燃烧匙中的红磷可以换成细铁丝 B、该实验可说明 难溶于水 C、红磷燃烧一停止立即打开弹簧夹 D、红磷的量不足会导致进入集气瓶中水的体积大于19. 写出下列反应的化学方程式:(1)、镁条在氧气中燃烧:;(2)、氢气在空气中燃烧:;(3)、细铁丝铁在氧气中燃烧:。(4)、硫燃烧。
A、燃烧匙中的红磷可以换成细铁丝 B、该实验可说明 难溶于水 C、红磷燃烧一停止立即打开弹簧夹 D、红磷的量不足会导致进入集气瓶中水的体积大于19. 写出下列反应的化学方程式:(1)、镁条在氧气中燃烧:;(2)、氢气在空气中燃烧:;(3)、细铁丝铁在氧气中燃烧:。(4)、硫燃烧。四、流程题
-
20. 构建知识的网络是一种重要的学习方法。(1)、请将微粒名称或物质的化学式填入下图A,B,C,D相应方框内,从而完成粒子与物质之间的正确的关系图
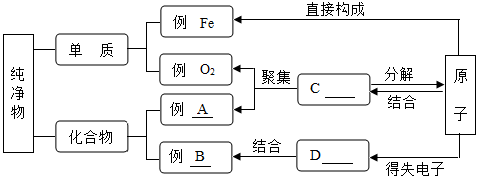
ABCD
(2)、国庆期间,金浩同学去蓟州旅游时,用瓶装了一些山下的泉水,带回实验室,在老师的指导下,按下列流程进行实验,制取蒸馏水.请回答下列问题: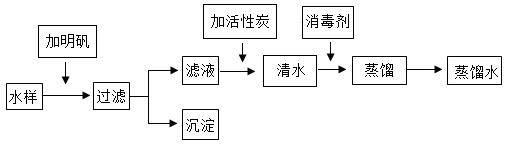
①操作I的名称是。
②向滤液中加入活性炭,利用其性,可以除去水样中的色素和异味。
③实验室制取蒸馏水的烧瓶中,通常加入几粒碎瓷片或沸石,其作用是;生活中软化硬水的一种常用方法是。
④若用课本中“课外实验”自制的简易净水器也可对泉水进行初步净化,请写出制作过程中用到的任意两种主要材料。
五、推断题
-
21. A,B…H八种物质,有如图所示关系:其中A是一种暗紫色固体,H是一种能使澄清石灰水变浑浊的气体,F是相对分子量最小的氧化物。试推断:
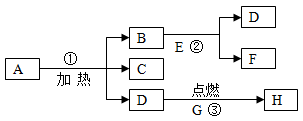 (1)、写出下列物质的名称:C。(2)、反应③的基本类型:反应,该反应中体现了D的性。(3)、写出反应①的化学方程式。写出反应②的化学方程式。(4)、反应②中B的作用为。
(1)、写出下列物质的名称:C。(2)、反应③的基本类型:反应,该反应中体现了D的性。(3)、写出反应①的化学方程式。写出反应②的化学方程式。(4)、反应②中B的作用为。六、实验题
-
22. 实验室制取气体时所需的一些装置如图所示。据图回答下列问题:
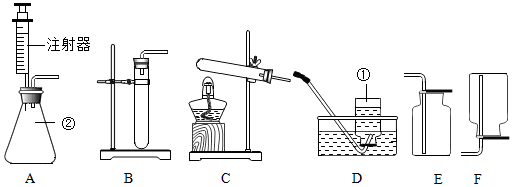 (1)、写出指定仪器的名称:①;②;(2)、小明同学想以氯酸钾和二氧化锰为原料制取一瓶干燥的氧气,他选择了C装置,你帮他选择的收集装置是(填装置标号,下同),写出该方法制氧气的化学方程式;检验该气体已收集满的方法是。(3)、实验室用高锰酸钾制氧气在试管口放棉花团的作用是;实验结束后发现试管破裂,你认为可能的原因是(写一种即可)(4)、实验室在常温下用块状电石(主要成分CaC2)与水反应制取不易溶于水的乙炔(C2H2)气体,同时还生成氢氧化钙,请写出该反应的化学方程式该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂。你认为最适合制取并收集乙炔气体的装置组合是。23. 定量研究对于化学科学发展有重大作用,因此我们应该掌握好有关质量守恒定律的相关知识。(1)、在验证质量守恒定律时,下列A、B、C三个实验设计中,不能达到实验目的是(选填序号),理由是。
(1)、写出指定仪器的名称:①;②;(2)、小明同学想以氯酸钾和二氧化锰为原料制取一瓶干燥的氧气,他选择了C装置,你帮他选择的收集装置是(填装置标号,下同),写出该方法制氧气的化学方程式;检验该气体已收集满的方法是。(3)、实验室用高锰酸钾制氧气在试管口放棉花团的作用是;实验结束后发现试管破裂,你认为可能的原因是(写一种即可)(4)、实验室在常温下用块状电石(主要成分CaC2)与水反应制取不易溶于水的乙炔(C2H2)气体,同时还生成氢氧化钙,请写出该反应的化学方程式该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂。你认为最适合制取并收集乙炔气体的装置组合是。23. 定量研究对于化学科学发展有重大作用,因此我们应该掌握好有关质量守恒定律的相关知识。(1)、在验证质量守恒定律时,下列A、B、C三个实验设计中,不能达到实验目的是(选填序号),理由是。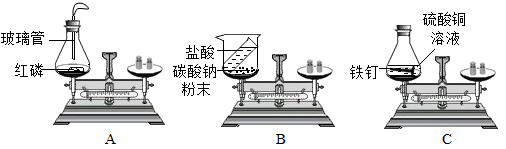 (2)、从微观角度分析,解释反应中,质量守恒定律成立的原因是:_____。
(2)、从微观角度分析,解释反应中,质量守恒定律成立的原因是:_____。①原子数目 ②分子数目 ③元素种类 ④物质种类 ⑤原子种类 ⑥原子质量
A、①④⑥ B、①⑤⑥ C、①②⑥ D、②③⑤(3)、碳在氧气中燃烧的化学方程式是: 。这个式子不仅表明了反应物是表示了参加反应的各物质之间的质量关系,即在点燃的条件下,每份质量的碳与份质量的氧气恰好完全反应生成份质量的二氧化碳。(4)、如图表示一定质量的 和 固体混合物受热过程中,某变量y随时间的变化趋势,纵坐标表示的是_____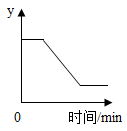 A、生成 的质量 B、固体中 的质量 C、固体中氧元素的质量 D、固体中钾元素的质量分数
A、生成 的质量 B、固体中 的质量 C、固体中氧元素的质量 D、固体中钾元素的质量分数七、科学探究题
-
24.(1)、英国科学家法拉第曾以蜡烛为主题,对青少年发表了一系列演讲,其演讲内容被编成《蜡烛的化学史》一书。下列有关蜡烛燃烧的叙述正确的是________A、蜡烛燃烧时,在顶端会形成一个液态石蜡的凹槽 B、用玻璃管从蜡烛火焰中引出的白烟是水蒸气 C、蜡烛燃烧时,液态石蜡抵达烛芯上汽化并燃烧(2)、“分解过氧化氢制氧气的反应中二氧化锰的催化作用”,以及“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣。
[提出问题]氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
[实验探究]
实验步骤
实验现象
I.分别量取5 ml 5%过氧化氢溶液放入A、B两支试管中,向A试管中加入a g氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。
A试管中产生气泡,带火星木条复燃,B试管中无明显现象
II.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,试管中均产生气泡,带火星木条均复燃如此反复多次试验,观察现象。
式管中均产生气泡,带火星木条均复燃
III.将实验II中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为a g。
/
IV.分别量取5mL5%过氧化氢溶液放入
C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。
/
[实验结论]
①A中产生的气体是。
②实验II、III证明:氧化铁的和在反应前后均没有发生变化,可以作过氧化氢分解的催化剂。
[实验评价]
③实验设计IV的目的是。
(3)、10 g A和足量B混合加热,充分反应后10 g A生成6 g C和8 g D,则参加反应的A和B的质量比为________A、1∶1 B、2∶3 C、4∶1 D、5∶2八、计算题
-
25. 葡萄糖( )是一种有甜味、易溶于水的白色粉末状固体.请根据葡萄糖的化学式进行以下计算:(1)、葡萄糖的相对分子质量是。(2)、葡萄糖中各元素质量比是 。(3)、每个葡萄糖分子中共有个原子。(4)、一定质量的葡萄糖溶解于水,得到的混合物中氢原子与氧原子的个数比 , 若该混合物中含氧元素的质量分数是80%,则碳元素的质量分数是。
-
-
-
-