2017年湖北省荆州市中考化学试卷
试卷更新日期:2017-07-24 类型:中考真卷
一、选择题
-
1. 下列成语涉及化学变化的是( )A、百炼成钢 B、香气四溢 C、木已成舟 D、水乳交融2. 下列物质属于纯净物的是( )A、石油 B、干冰 C、生铁 D、糖水3. 化学与生活密切相关,下列说法不正确的是( )A、用小苏打焙制糕点 B、油锅着火用锅盖盖灭 C、用灼烧法鉴别棉线与羊毛 D、胃酸过多的病人应多食用食醋4. 实验室配制100g 10%的NaCl溶液,不需要用到的仪器是( )A、酒精灯 B、托盘天平 C、胶头滴管 D、烧杯5. 下列说法不正确的是( )A、原子呈电中性 B、原子中一定含有质子 C、化学反应前后原子的种类不变 D、保持水的化学性质的微粒是氢原子和氧原子6. 往KOH溶液中加水,溶液的pH变化正确的是( )A、
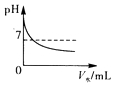 B、
B、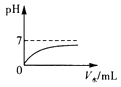 C、
C、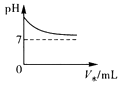 D、
D、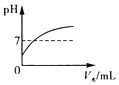 7. 某高性能锂电池,其反应原理可表示为:Li+MnO2=LiMnO2 , 已知锂元素在化合物中显+1价,下列说法正确的是( )A、LiMnO2是氧化物 B、该反应是化合反应 C、此反应中,二氧化锰是催化剂 D、LiMnO2中锰元素的化合价显+2价8. 下列关于维生素C(C6H8O6)的说法不正确的是( )A、1个维生素C分子由6个碳原子,8个氢原子,6个氧原子构成 B、维生素C的相对分子质量为176 C、维生素C中C、H、O三种元素的质量比为3﹕4﹕3 D、维生素C中氢元素的质量分数约为4.5%9. 某溶液能使紫色石蕊溶液变蓝,下列各组离子在该溶液中能大量共存的是( )A、SO42﹣、NO3﹣、Ba2+、Cl﹣ B、Cu2+、Na+、NO3﹣、K+ C、K+、CO32﹣、NO3﹣、Cl﹣ D、H+、Ba2+、K+、NO3﹣10. 除去下列各物质中的少量杂质,所用方法不可行的是( )
7. 某高性能锂电池,其反应原理可表示为:Li+MnO2=LiMnO2 , 已知锂元素在化合物中显+1价,下列说法正确的是( )A、LiMnO2是氧化物 B、该反应是化合反应 C、此反应中,二氧化锰是催化剂 D、LiMnO2中锰元素的化合价显+2价8. 下列关于维生素C(C6H8O6)的说法不正确的是( )A、1个维生素C分子由6个碳原子,8个氢原子,6个氧原子构成 B、维生素C的相对分子质量为176 C、维生素C中C、H、O三种元素的质量比为3﹕4﹕3 D、维生素C中氢元素的质量分数约为4.5%9. 某溶液能使紫色石蕊溶液变蓝,下列各组离子在该溶液中能大量共存的是( )A、SO42﹣、NO3﹣、Ba2+、Cl﹣ B、Cu2+、Na+、NO3﹣、K+ C、K+、CO32﹣、NO3﹣、Cl﹣ D、H+、Ba2+、K+、NO3﹣10. 除去下列各物质中的少量杂质,所用方法不可行的是( )选项
物质
杂质
除杂方法
A
NaNO3
Na2CO3
加足量稀盐酸,蒸发结晶
B
Cu
Fe
加足量的稀硫酸,过滤
C
CO2
CO
通过灼热的CuO
D
CaO
CaCO3
高温煅烧
A、A B、B C、C D、D11. 如图各物质均为初中化学常见的物质(反应条件省略),下列说法正确的是( )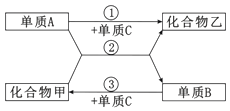 A、常温下,化合物乙一定是无色气体 B、化合物甲可能含有3种元素 C、反应②一定是置换反应 D、单质B一定是金属铜12. 物质X与Ca(OH)2水溶液发生反应的化学方程式为:X+Ca(OH)2=Y+Cu(OH)2↓,下列说法正确的是( )A、X可能是酸 B、X和Y的相对分子质量之差为24 C、X可能是单质,也可能是化合物 D、Y只可能是CaCl2
A、常温下,化合物乙一定是无色气体 B、化合物甲可能含有3种元素 C、反应②一定是置换反应 D、单质B一定是金属铜12. 物质X与Ca(OH)2水溶液发生反应的化学方程式为:X+Ca(OH)2=Y+Cu(OH)2↓,下列说法正确的是( )A、X可能是酸 B、X和Y的相对分子质量之差为24 C、X可能是单质,也可能是化合物 D、Y只可能是CaCl2二、非选择题
-
13. 回答下列问题:(1)、缺(填元素名称)可能导致骨质疏松,易得佝偻病.(2)、是一种工业用盐,它有毒、有咸味、外形与食盐相似.(3)、米和面中含有的糖类物质主要是 , 在人体的消化系统中最终变为葡萄糖.(4)、香烟烟气中的是一种极易与血液中的血红蛋白结合的有毒气体.14. 2017年3月22日是世界水日,水是人类宝贵的自然资源,根据所学知识回答下列问题:(1)、火箭使用的燃料液氢在助燃剂液氧中燃烧的化学方程式为 .(2)、日常生活中通常向水中滴加来检验硬水和软水.(3)、高铁酸钠(Na2FeO4)被广泛应用于自来水净化消毒,其原理为:
4Na2FeO4+10=4Fe(OH)3(胶体)+3+8NaOH(请将化学方程式补充完整).
(4)、水是常用的溶剂,某酒精(C2H5OH)的水溶液,溶质与溶剂中氢原子个数比为1:2,则该溶液中溶质的质量分数为(精确到1%).15. 如图为A、B、C、D四种粒子的结构示意图以及硒元素在元素周期表中的信息,请按要求填空: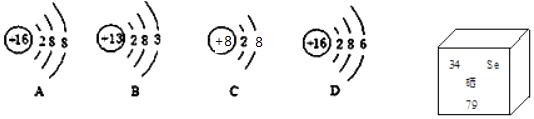 (1)、A、B、C、D四种粒子中,属于同种元素的是(填序号),C粒子的符号为 .(2)、由A元素和B元素形成的化合物的化学式为 .(3)、该硒原子的中子数是 .16. A、B、C三种物质的溶解度曲线如图所示,请回答下列问题:
(1)、A、B、C、D四种粒子中,属于同种元素的是(填序号),C粒子的符号为 .(2)、由A元素和B元素形成的化合物的化学式为 .(3)、该硒原子的中子数是 .16. A、B、C三种物质的溶解度曲线如图所示,请回答下列问题: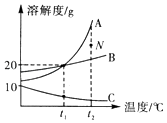 (1)、N点对应的是物质A的(“饱和”或“不饱和”)溶液.(2)、加热C的饱和溶液,出现浑浊现象,其原因是 .(3)、除去A中少量的B,步骤是:加水溶解,蒸发浓缩, , 过滤,洗涤,干燥.(4)、t1℃时,将A、B、C各8g分别加入盛有50g水的烧杯中,充分溶解,测得三种溶液中溶质的质量分数分别为w(A)、w(B)、w(C),则三者之间的大小关系是 .17. 有一包固体,可能由KNO3、BaCl2、NH4Cl、Na2CO3、Na2SO4、MgCl2中的一种或几种组成,为了探究该固体组成,某化学小组将固体溶于水配成溶液并开展以下实验,已知步骤Ⅱ中无气泡产生,且白色沉淀部分溶解,请回答下列问题:
(1)、N点对应的是物质A的(“饱和”或“不饱和”)溶液.(2)、加热C的饱和溶液,出现浑浊现象,其原因是 .(3)、除去A中少量的B,步骤是:加水溶解,蒸发浓缩, , 过滤,洗涤,干燥.(4)、t1℃时,将A、B、C各8g分别加入盛有50g水的烧杯中,充分溶解,测得三种溶液中溶质的质量分数分别为w(A)、w(B)、w(C),则三者之间的大小关系是 .17. 有一包固体,可能由KNO3、BaCl2、NH4Cl、Na2CO3、Na2SO4、MgCl2中的一种或几种组成,为了探究该固体组成,某化学小组将固体溶于水配成溶液并开展以下实验,已知步骤Ⅱ中无气泡产生,且白色沉淀部分溶解,请回答下列问题: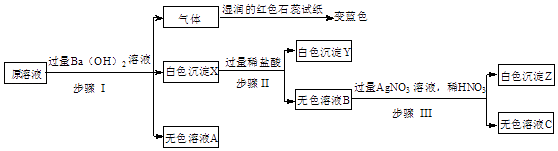 (1)、步骤Ⅰ产生的气体为 .(2)、原固体中一定含有的物质是 .(3)、步骤Ⅱ中发生反应的化学方程式为 .(4)、无色溶液C中阳离子的符号为18. 实验室部分装置如图所示,回答下列问题:
(1)、步骤Ⅰ产生的气体为 .(2)、原固体中一定含有的物质是 .(3)、步骤Ⅱ中发生反应的化学方程式为 .(4)、无色溶液C中阳离子的符号为18. 实验室部分装置如图所示,回答下列问题: (1)、仪器X的名称是 .(2)、实验室常用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷(CH4)气体,其发生装置为 .(3)、实验室用装置B制O2的化学方程式为 .(4)、某同学欲用活泼金属单质和稀盐酸反应制取纯净干燥的H2 , 请从这些装置中选择并连接成一套组合装置,按照气流从左到右的流向,写出所选装置接口的连接顺序:→→→→→→→→→…(可不填满,也可补充).19. 某化学小组将少量过氧化钠(Na2O2)粉末加入盛水的试管中,看到有大量气泡产生.
(1)、仪器X的名称是 .(2)、实验室常用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷(CH4)气体,其发生装置为 .(3)、实验室用装置B制O2的化学方程式为 .(4)、某同学欲用活泼金属单质和稀盐酸反应制取纯净干燥的H2 , 请从这些装置中选择并连接成一套组合装置,按照气流从左到右的流向,写出所选装置接口的连接顺序:→→→→→→→→→…(可不填满,也可补充).19. 某化学小组将少量过氧化钠(Na2O2)粉末加入盛水的试管中,看到有大量气泡产生.【提出问题】
过氧化钠与水反应生成了什么物质?
【作出猜想】
甲同学:生成氢氧化钠
乙同学:生成碳酸钠
丙同学:生成氢气
丁同学:生成氧气
(1)、大家一致认为乙同学的推测不正确,理由是 .(2)、【实验探究】实验方法
实验现象
实验结论
用试管收集生成的气体,堵住试管口,移近酒精灯火焰,点燃
无现象
用试管收集生成的气体,将带火星的木条伸入试管内
有氧气生成
溶液变红
溶液显碱性
(3)、【得出结论】过氧化钠与水反应的化学方程式为 .
(4)、【反思拓展】根据所学知识,请你预测将少量过氧化钠粉末加入硫酸铜溶液中的反应现象 .
20. 某腐蚀印刷电路板的废液经处理后只含有CuCl2和FeCl2两种溶质,为了分析处理后废液的组成,取200g该废液加入40g废铁屑(杂质不溶于水,也不参与反应),恰好完全反应,过滤经处理得到16g铜,往滤液中加入足量的硝酸银溶液,经过滤、干燥、称量,最终得到114.8gAgCl固体.回答下列问题:(1)、往废液中加入废铁屑发生反应的化学方程式为 ,往滤液中加入硝酸银溶液发生反应的化学方程式为 .
(2)、求滤液中溶质的质量分数(精确到1%).(3)、求200g废液中FeCl2的质量分数(精确到1%).