2017年福建省中考化学试卷
试卷更新日期:2017-07-24 类型:中考真卷
一、选择题
-
1. 下列可供人呼吸的气体是( )A、氧气 B、氢气 C、氮气 D、二氧化碳2. 人体缺乏某种元素会导致骨质疏松症,该元素是( )A、铁 B、碘 C、钙 D、锌3. 中药砒霜的主要成分为三氧化二砷(As2O3),可用于治疗肿瘤,其中砷元素的化合价为( )A、﹣3 B、+3 C、﹣2 D、+24. 下列人体体液中,酸性最强的是( )A、唾液(pH约6.6﹣7.1) B、胃酸(pH约0.8﹣1.5) C、胆汁(pH约6.8﹣7.4) D、血液(pH约7.35﹣7.45)5. 下列四支试管中,铁钉锈蚀最快的是( )A、
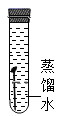 B、
B、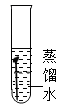 C、
C、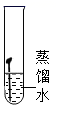 D、
D、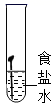 6. 欲配制10.0%的NaCl溶液50g部分操作如图所示,正确的是( )A、
6. 欲配制10.0%的NaCl溶液50g部分操作如图所示,正确的是( )A、 取固体
B、
取固体
B、 称固体
C、
称固体
C、 量取水
D、
量取水
D、 写标签
7. 十八世纪,拉瓦锡用放大镜聚集日光使玻璃罩内的金刚石燃烧,得到二氧化碳,坦南特进一步研究确认金刚石仅由碳元素组成.下列说法错误的是( )A、金刚石属于有机物 B、金刚石燃烧过程放出热量 C、金刚石具有可燃性 D、聚集日光使温度达到金刚石的着火点8. 炼铁炉中某反应的微观示意图(不同的球代表不同原子)如下所示.下列说法正确的是( )
写标签
7. 十八世纪,拉瓦锡用放大镜聚集日光使玻璃罩内的金刚石燃烧,得到二氧化碳,坦南特进一步研究确认金刚石仅由碳元素组成.下列说法错误的是( )A、金刚石属于有机物 B、金刚石燃烧过程放出热量 C、金刚石具有可燃性 D、聚集日光使温度达到金刚石的着火点8. 炼铁炉中某反应的微观示意图(不同的球代表不同原子)如下所示.下列说法正确的是( ) A、该反应属于化合反应 B、反应前后原子数目发生变化 C、反应前后各元素化合价均不变 D、反应前后元素种类发生变化9. 如图是甲、乙两种固体物质的溶解度曲线,下列说法错误的是( )
A、该反应属于化合反应 B、反应前后原子数目发生变化 C、反应前后各元素化合价均不变 D、反应前后元素种类发生变化9. 如图是甲、乙两种固体物质的溶解度曲线,下列说法错误的是( ) A、t1℃时,25g甲充分溶解于100g水中,配得甲的饱和溶液 B、t2℃时,甲、乙饱和溶液的溶质质量分数相等 C、若甲中含有少量乙,可用溶解、过滤的方法提纯甲 D、将甲的饱和溶液从t2℃时降温到t1℃,可析出晶体10. 常温下,往盛放适量M物质的烧杯中逐渐加入N物质并充分搅拌,如图横坐标x表示N物质的质量,纵坐标y表示烧杯中的某物理量(见表).下列实验与图象对应关系合理的是( )
A、t1℃时,25g甲充分溶解于100g水中,配得甲的饱和溶液 B、t2℃时,甲、乙饱和溶液的溶质质量分数相等 C、若甲中含有少量乙,可用溶解、过滤的方法提纯甲 D、将甲的饱和溶液从t2℃时降温到t1℃,可析出晶体10. 常温下,往盛放适量M物质的烧杯中逐渐加入N物质并充分搅拌,如图横坐标x表示N物质的质量,纵坐标y表示烧杯中的某物理量(见表).下列实验与图象对应关系合理的是( )M
N
y
A
水
氧化钙
溶液的温度
B
水
氢氧化钠
溶液的pH
C
饱和氯化钠溶液
氯化钠
溶液的溶质质量分数
D
硫酸铜溶液
铁粉
溶液的质量
 A、A B、B C、C D、D
A、A B、B C、C D、D二、解答题
-
11. 近期,央视对“用棉花代替肉松饼”的消息进行辟谣.资料表明:肉松使用动物肌肉制作的蓬松絮状肉制品,棉花主要含有植物纤维.(1)、棉花属于(填“天然”或“合成”)有机高分子材料.(2)、肉松中含量最多的营养素是 .(3)、可用燃烧法鉴别肉松与棉花,点燃时闻到烧焦羽毛气味的是 .(4)、制作肉松饼使用的发酵粉中含有碳酸氢铵(NH4HCO3).碳酸氢铵中氢和氧两种元素的质量比为 .12. 农业废弃物是指农业生产过程中废弃的有机物,入秸秆、蔗渣等.(1)、农业废弃物经发酵处理可获得沼气(主要成分为甲烷).甲烷完全燃烧的化学方程式为 .(2)、闽籍科学家张俐娜发明了一种快速溶解农业废弃物的“神奇溶剂”.该“神奇溶剂”中氢氧化钠、尿素和水的质量比为7:12:81.
①“神奇溶剂”是一种溶液,其溶质有 .
②某次生产需用到100kg“神奇溶剂”.现仅有氢氧化钠溶液和尿素来配制,所用的氢氧化钠溶液的溶质质量分数为(列出计算式即可).
③利用该“神奇溶剂”溶解农业废弃物生产的新型纤维素膜,在土壤中能完全降解.利用此膜代替普通塑料,可缓解的环境问题是(写一点)
13. 模型使联系宏观与微观的桥梁.(1)、如图1是钠原子结构示意图.
①X的数值为 .
②“11”指的是 .
③钠原子在化学反应中易失去1个电子,形成(填离子符号).
(2)、如图2使氢分子和氧分子运动的示意图.
①在A、B和C中,能比较得出“温度越高,分子运动速度越快”的是(填标号).
②从图中可见,影响分子运动速率的因素除温度外,还与有关.
③举一个能说明“温度升高,分子运动速率加快”的生活事例 .
14. 如图是包含物质A、B、C、D和盐酸卡片的“化学拼图”,相邻两张卡片所标的物质(或其溶液)间能发反应. (1)、A不可能是(填标号)
(1)、A不可能是(填标号)a.Mg b.Fe c.Ag d.Zn
(2)、若B为铁锈的主要成分Fe2O3 , B与盐酸反应的化学方程式为 .(3)、若C为碳酸钠①C与D的反应属于(填基本反应类型)
②D与盐酸反应的化学方程式为(写一个)
③将二氧化碳通入C溶液,可化合生成碳酸氢钠(NaHCO3),该反应的反应物有种.
15. 根据问题填空:(1)、化学小组选用如图装置制取并收集氧气.
①仪器的名称:a是 , b是 .
②实验室制取氧气的化学方程式为(写一个),实验时对应的气体发生和收集装置分别是(填标号,下同)和 .
(2)、碘化钾(KI)是白色固体,保存不当会被氧化为单质碘(I2)而泛黄变质.化学小组查得以下资料:Ⅰ.对于碘化钾变质的原理,有两种不同的反应:
甲:4KI+2CO2═2K2CO3+2I2
乙:4KI+O2+2H2O═4KOH+2I2
Ⅱ.KOH与NaOH的化学性质相似.
为探究碘化钾变质原理的合理性,开展以下实验.
【实验过程】
[实验1]取适量碘化钾固体暴露于空气中一端时间,观察到固体泛黄,往泛黄的固体中加入足量稀硫酸,产生无色无味的气体,通入澄清石灰水中,澄清石灰水变浑浊.
①石灰水变浑浊的原因是(用化学方程式表示)
②化学小组认为:据此现象,还不能得出“反应甲是造成碘化钾变质的原因”的结论.理由是 .
[实验2]
按如图所示装置进行实验,数日后,观察到碘化钾固体无泛黄现象.

③据此现象,可得出的结论是 .
[实验3]
按如图所示装置进行实验,数日后,观察到碘化钾固体无泛黄现象.

查阅文献获知,常温下某些气体和固体反应须在潮湿环境中进行.
化学小组据此改进实验,很快观察到固体泛黄的现象.
④简述化学小组改进实验的具体措施 .
【实验结论】
⑤根据上述实验,化学小组得出的结论:碘化钾固体泛黄变质是碘化钾与共同作用的结果.
 16. “人工固氮”每年能生产11.9亿吨氨(NH3),反应原理为:N2+3H2 2NH3(1)、根据化学方程式计算:“人工固氮”每年固定氮气的质量是多少?(2)、每年全球“雷电固氮”约能固定0.98亿吨氮气,“人工固氮”固定氮气的质量相当于“雷电固氮”的倍.
16. “人工固氮”每年能生产11.9亿吨氨(NH3),反应原理为:N2+3H2 2NH3(1)、根据化学方程式计算:“人工固氮”每年固定氮气的质量是多少?(2)、每年全球“雷电固氮”约能固定0.98亿吨氮气,“人工固氮”固定氮气的质量相当于“雷电固氮”的倍.