湖南省怀化市洪江市2018-2019学九年级上学期化学期中考试试卷
试卷更新日期:2019-12-06 类型:期中考试
一、单选题
-
1. 下列有关物质的应用中,利用原理为化学变化的是()A、用活性炭清除电冰箱中的异味 B、用生石灰吸收水蒸气 C、在研钵内将胆矾研碎 D、石墨粉润滑机床2. 将混有少量氯化钾的高锰酸钾放入试管中加热,完全反应后试管中的剩余固体共有 ( )A、2种 B、3种 C、4种 D、5种3. 植物的光合作用可表示为:CO2 + H2O 淀粉 + O2 , 由此可推知,淀粉中一定含有的元素为( )A、碳元素 B、氢元素 C、碳、氢两种元素 D、碳、氢、氧三种元素4. 除去下列物质中含有的少量杂质(括号内的物质),所选试剂不合理的是( )A、CaO(CaCO3):稀盐酸 B、NaOH溶液[Ca(OH)2溶液]:碳酸钠溶液 C、Cu(Fe):硫酸铜溶液 D、CO(CO2):氢氧化钠溶液5. 下列关于一氧化碳和二氧化碳的说法中,正确的是( )A、一氧化碳和二氧化碳均具有可燃性 B、一氧化碳和二氧化碳均能与水反应 C、一氧化碳和二氧化碳的密度均大于空气的密度 D、一氧化碳和二氧化碳在一定条件下可以相互转化6. PM2.5是指大气中直径小于或等于2.5微米的颗粒物,2.5微米以下的细颗粒物主要来自化石燃料的燃烧等。以下不属于化石燃料的是()A、天然气 B、石油 C、酒精 D、煤7. 工业上制得一氧化氮的化学方程式为:4X + 5O2 4NO + 6H2O,则X的化学式为( )A、N2 B、NO2 C、NH3 D、N2O58. 下列指定反应的化学方程式正确的是( )A、铁丝在氧气中燃烧:4Fe+3O2 2Fe2O3 B、铜和硝酸银反应:Cu+AgNO3=CuNO3+ Ag↓ C、铜绿和稀盐酸反应:Cu2(OH)2CO3+4HCl = 2CuCl2+3H2O+CO2↑ D、过氧化钠与二氧化碳反应生成纯碱和氧气:2Na2O2+CO2=2Na2CO3+O2↑9. 下列实验操作错误的是( )A、
 取用固体粉末
B、
取用固体粉末
B、 检验氢气纯度
C、
检验氢气纯度
C、 液体的量取
D、
液体的量取
D、 倾倒二氧化碳
10. 在科学家的努力下,又有四种新元素相继被发现并命名,填满了元素周期表的第七周期,形成了一张完整规范的元素周期表。如图为 号元素的有关信息,下列说法错误的是( )
倾倒二氧化碳
10. 在科学家的努力下,又有四种新元素相继被发现并命名,填满了元素周期表的第七周期,形成了一张完整规范的元素周期表。如图为 号元素的有关信息,下列说法错误的是( )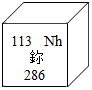 A、鉨元素属于金属元素 B、“ ”表示鉨元素、一个鉨原子、鉨这种物质 C、鉨原子的原子序数为 ,其核内有113个质子 D、鉨元素的相对原子质量为11. 喝酒不开车,开车不喝酒.酒后驾驶是一种违法行为.酒精的化学式为C2H5OH.下列有关酒精的说法正确的是( )A、酒精中氢元素的质量分数最大 B、酒精中碳、氢元素的质量比为1:3 C、酒精属于化合物 D、酒精是由2个碳原子、6个氢原子和1个氧原子构成的12. 推理是一种重要的思维方法,以下推理合理的是( )A、酸中一定含有氢元素,所以含有氢元素的物质一定是酸 B、置换反应有单质生成,所以有单质生成的反应一定是置换反应 C、化学反应前后原子总数不变,所以化学反应前后分子总数也不变 D、化学反应伴随能量变化,所以金属腐蚀过程中一定伴随能量变化13. 下列变化中都属于物理变化的是( )
A、鉨元素属于金属元素 B、“ ”表示鉨元素、一个鉨原子、鉨这种物质 C、鉨原子的原子序数为 ,其核内有113个质子 D、鉨元素的相对原子质量为11. 喝酒不开车,开车不喝酒.酒后驾驶是一种违法行为.酒精的化学式为C2H5OH.下列有关酒精的说法正确的是( )A、酒精中氢元素的质量分数最大 B、酒精中碳、氢元素的质量比为1:3 C、酒精属于化合物 D、酒精是由2个碳原子、6个氢原子和1个氧原子构成的12. 推理是一种重要的思维方法,以下推理合理的是( )A、酸中一定含有氢元素,所以含有氢元素的物质一定是酸 B、置换反应有单质生成,所以有单质生成的反应一定是置换反应 C、化学反应前后原子总数不变,所以化学反应前后分子总数也不变 D、化学反应伴随能量变化,所以金属腐蚀过程中一定伴随能量变化13. 下列变化中都属于物理变化的是( )①酒精挥发 ②镁条在空气中燃烧 ③二氧化碳通入澄清石灰水 ④矿石粉碎
⑤湿衣服晾干 ⑥铁钉生锈 ⑦煤燃烧 ⑧火药爆炸
A、①④⑤ B、②③④ C、⑥⑦⑧ D、③⑥⑧14. 下列实验方案可行的是( )A、将水倒入盛有浓硫酸的烧杯中配制稀硫酸 B、用氢氧化钠溶液除去CO2中的HCl气体 C、用BaCl2溶液除去KNO3溶液中少量的K2SO4 D、分离CaCl2、CaCO3的混合物,主要操作为溶解、过滤、蒸发等15. 下列属于可再生能源的是( )A、煤 B、石油 C、天然气 D、酒精16. 下列物质的用途与性质对应关系错误的是()选项
A
B
C
D
用
途




金刚石做玻璃刀
石墨做电池电极
不锈钢做水壶
钛合金制造船舶设备
性质
金刚石硬度大
石墨很软
不锈钢有导热性
钛合金抗腐蚀性强
A、A B、B C、C D、D17. 下列反应的化学方程式书写完全正确的是( )A、铁在氧气中燃烧:2Fe+3O2 2Fe2O3 B、盐酸除铁锈:Fe2O3+6HCl=2FeCl3+3H2O C、密闭容器中燃烧红磷验证质量守恒定律:2P+O2 P2O5 D、甲烷燃烧:CH4+O2=CO2+H2O18. 下列有关溶液的说法正确的是()A、配制好6%的NaCl溶液,装瓶时不小心撒漏一部分,瓶中NaCl溶液浓度仍为6% B、长期放置后不会分层的液体一定是溶液 C、KNO3饱和溶液一定比不饱和溶液溶质质量分数大 D、降低饱和溶液的温度,一定有晶体析出19. A,B,C三种不含结晶水的固体物质的溶解度曲线如图,下列说法中错误的是( )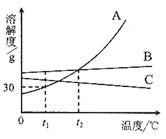 A、t1℃时,A的饱和溶液65 g中含有溶剂50 g ; B、t2℃时, 将A,B,C三种物质的饱和溶液降温至t1℃,C溶液中溶质的 质量分数保持不变; C、在t2℃,A,B两种溶液中溶质的质量分数相同; D、要从B溶液中得到B通常可采用蒸发溶剂使其结晶的方法。20. 某同学为了探究甲、乙、丙、丁四种物质之间能否发生反应,将它们混合密闭在一容器中, 高温加热一段时间后,检测其中部分物质的质量,并与加热前比较(见下表)。下列判断错误的是( )
A、t1℃时,A的饱和溶液65 g中含有溶剂50 g ; B、t2℃时, 将A,B,C三种物质的饱和溶液降温至t1℃,C溶液中溶质的 质量分数保持不变; C、在t2℃,A,B两种溶液中溶质的质量分数相同; D、要从B溶液中得到B通常可采用蒸发溶剂使其结晶的方法。20. 某同学为了探究甲、乙、丙、丁四种物质之间能否发生反应,将它们混合密闭在一容器中, 高温加热一段时间后,检测其中部分物质的质量,并与加热前比较(见下表)。下列判断错误的是( )物质
甲
乙
丙
丁
反应前质量/g
2
30
6
3
反应后质量/g
12
2
x
3
A、x=24 B、丁可能是催化剂 C、容器内发生的是分解反应 D、反应中 甲和丙的质量比是 1:2二、填空题
-
21. 用下列常见物质来完成以下各题:(填序号)
①干冰②葡萄糖③石墨④硝酸铵固体⑤水银
(1)、溶于水后溶液温度降低的是;(2)、可做干电池电极的是;(3)、用于人工降雨的是;(4)、温度计中含有的物质是;(5)、人体主要的供能物质的是。22. 化学用语可准确、简洁地记录、表达和交流化学信息。请用化学符号填写:①地壳中含量最多的金属元素;
②两个氯分子;
③二氧化硫中硫元素显正4价。
23. 在化学方程式4P+5O2 2P2O5中,生成物是 , 反应中每份质量的磷与份质量的氧气反应,生成份质量的五氧化二磷.该反应的基本类型属于反应.24. 写出下列化学反应方程式。(1)、电解水:。(2)、酒精(C2H5OH)完全燃烧:。(3)、用红磷测定空气中氧气含量:。(4)、工业上用一氧化碳和磁铁矿石(主要成分Fe3O4)在高温下炼铁:。25. 随着人们生活水平的不断提高,汽车已走进千家万户。制造汽车要用到含铜、铁、铝等成分的多种金属材料。(1)、在汽车电路中,经常用铜作导线,这是利用了铜的性;(2)、车体多用钢材制造.其表面喷漆不仅美观,而且可有效防止与接触而生锈;(3)、在实验室中探究铝、铜的金属活动性顺序,除铝、铜外,还需要用到的试剂是。(填一种即可)26. 如表是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答:温度/℃
10
20
30
40
溶解度/g
氯化钠
35.8
36.0
36.3
36.6
碳酸钠
12.2
21.8
39.7
53.2
①由表中数据可知,溶解度随温度变化较大的物质是 , 氯化钠与碳酸钠溶解度相等的温度范围是至℃.
②10℃时,分别配制表中两种物质的饱和溶液,其中溶质质量分数较大的物质是;20℃时,100g水最多能溶解gNaCl;
③向烧杯中加100g水和50.0g碳酸钠配成40℃的溶液,再冷却到20℃,烧杯中析出固体为g(不考虑结晶水);若在碳酸钠溶液中混有少量的氯化钠,则分离的方法可采用 .
三、流程题
-
27. 如图是工业炼铁的流程图,根据图示回答下列问题:
 (1)、工业炼铁过程中,常常需要将焦炭粉碎,其目的是: , 焦炭在炼铁中的作用有:、。(2)、过程中有一个吸热反应, 改为:上述过程中有些反应吸热 请写出一个吸热反应的化学方程式。(3)、炼铁过程中还有一种关键原料: 填名称 ,作用是:。
(1)、工业炼铁过程中,常常需要将焦炭粉碎,其目的是: , 焦炭在炼铁中的作用有:、。(2)、过程中有一个吸热反应, 改为:上述过程中有些反应吸热 请写出一个吸热反应的化学方程式。(3)、炼铁过程中还有一种关键原料: 填名称 ,作用是:。四、实验题
-
28. 请根据下列实验装置图回答问题:
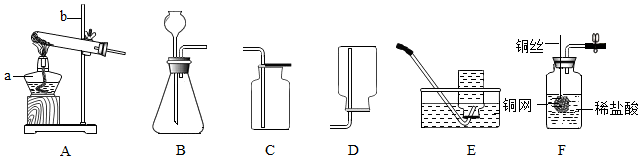 (1)、仪器a的名称是 ,仪器b的名称是。(2)、实验室用过氧化氢溶液和二氧化锰制取氧气,该反应可用装置C收集氧气,证明收集满气体的方法是。(3)、实验室制取CO2 , 发生反应的化学方程式为 , 装置F是小亮制取CO2的气体发生装置,用它代替B装置的优点是(答出一点即可)。(4)、加热氯化铵和熟石灰固体混合物制取NH3 , 可选用的发生装置是 (填字母序号)。
(1)、仪器a的名称是 ,仪器b的名称是。(2)、实验室用过氧化氢溶液和二氧化锰制取氧气,该反应可用装置C收集氧气,证明收集满气体的方法是。(3)、实验室制取CO2 , 发生反应的化学方程式为 , 装置F是小亮制取CO2的气体发生装置,用它代替B装置的优点是(答出一点即可)。(4)、加热氯化铵和熟石灰固体混合物制取NH3 , 可选用的发生装置是 (填字母序号)。五、科学探究题
-
29. 某化学兴趣小组在实验室中模拟炼铁,他们把焦炭和氧化铁粉末合加强热,得到无色气体A和黑色粉末B(如图所示)。
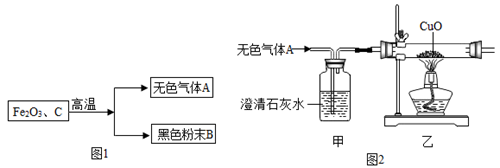 (1)、他们炼铁反应的化学方程式是。(2)、经分析得知,无色气体A不含有单质,黑色粉末B的成分是一种或两种单质。甲、乙两个兴趣小组分别对无色气体A和黑色粉末B的成分进行探究。
(1)、他们炼铁反应的化学方程式是。(2)、经分析得知,无色气体A不含有单质,黑色粉末B的成分是一种或两种单质。甲、乙两个兴趣小组分别对无色气体A和黑色粉末B的成分进行探究。(猜想与假设)甲组认为无色气体A中可能有CO2 , 也可能有CO。
乙组认为黑色粉末的成分中存在以下两种情况:
①只含有。
②含有铁和碳。
(3)、(实验探究)为验证甲组的猜想,同学们按下图所示装置进行实验。
装置甲的作用是 , 装置乙的作用是。当看到甲中澄清石灰水变浑浊,乙中后,可以确定无色气体A是CO2、CO的混合气体。有同学提出把甲、乙交换位置,让气体A先通过热的氧化铜也可以达到同样的实验目的,你的判断是(填“可以”或“不可以”)。
(4)、为验证乙组中假设②是否成立,设计实验用物理和化学两种方法完成以下探究。实验方法
实验操作
实验现象
实验结论
物理方法
假设二成立
六、计算题
-
-