2016-2017学年江西省赣州市四所高中联考高一下学期期中化学试卷
试卷更新日期:2017-07-20 类型:期中考试
一、选择题
-
1. 元素性质呈周期性变化的决定因素是( )A、元素原子核外电子层排布呈周期性变化 B、元素相对原子质量依次递增 C、元素原子半径大小呈周期性变化 D、元素的最高正化合价呈周期性变化2. 已知A、B两元素的原子序数,其中可形成AB2型共价化合物的是( )
①6和16 ②12和17 ③20和9 ④7和8.
A、①③ B、①④ C、②③ D、③④3. 13C﹣NMR(核磁共振)可用于含碳化合物的结构分析.下列有关13C的说法不正确的是( )A、13C的质量数是13,核内有6个电子 B、13C 与12C是两种不同的核素 C、13C 与12C互为同位素 D、13C 与12C 的化学性质有很大的差别4. 根据原子结构及元素周期律的知识,下列叙述正确的是( )A、由于分子中氢原子数:H2SO4>HClO4 , 故酸性:H2SO4>HClO4 B、由子F元素的最低化合价为﹣1价,故F元素的最高化合价为+7价 C、硅处于金属与非金属的过渡位置,故硅可用作半导体材枓 D、Cl﹣、S2﹣、Ca2+、K+半径逐渐减小5. 下列关于元素周期表的描述正确的是( )A、有7个周期,18个族 B、第IA族元素也称为碱金属元素 C、元素种类最多的族为第IIIB族 D、第七周期若排满,最多可排50种元素6. 下列各组物质中化学键的类型完全相同的是( )A、NH4Cl H2O CO2 B、NaCl MgCl2 Na2O C、H2O Na2O CO2 D、CaCl2 NaOH H2SO47. 2013年7月23日人民网报道,河南省柘城县科技创新“创”出金刚石产业新天地.1mol石墨在一定条件下完全转化为金刚石,其能量变化如图所示,△E1=393.5kJ,△E2=395.4kJ,下列说法正确的是( )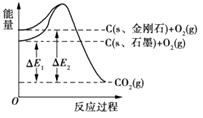 A、1 mol石墨完全转化为金刚石需吸收1.9 kJ的能量 B、石墨转化为金刚石属于物理变化 C、金刚石的稳定性强于石墨的 D、1 mol金刚石的能量大于1mol CO2的能量8. 金属元素钫(Fr)在自然界中含量极少.它的21个已知同位素都有放射性.它是碱金属元素中最重的元素.根据它在周期表中的位置预言其性质,其中不正确的是( )A、在已知碱金属元素中具有最大的原子半径 B、其氧化物对应的水化物是极强的碱 C、在空气中燃烧时生成氧化物Fr2O D、在已知碱金属元素单质中熔点最低9. 下列化学用语的书写,正确的是( )A、H2S的电子式:
A、1 mol石墨完全转化为金刚石需吸收1.9 kJ的能量 B、石墨转化为金刚石属于物理变化 C、金刚石的稳定性强于石墨的 D、1 mol金刚石的能量大于1mol CO2的能量8. 金属元素钫(Fr)在自然界中含量极少.它的21个已知同位素都有放射性.它是碱金属元素中最重的元素.根据它在周期表中的位置预言其性质,其中不正确的是( )A、在已知碱金属元素中具有最大的原子半径 B、其氧化物对应的水化物是极强的碱 C、在空气中燃烧时生成氧化物Fr2O D、在已知碱金属元素单质中熔点最低9. 下列化学用语的书写,正确的是( )A、H2S的电子式: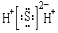 B、硫原子的结构示意图:
B、硫原子的结构示意图: 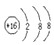 C、氮气的电子式:
C、氮气的电子式:  D、水分子的结构式:
D、水分子的结构式:  10. 下列说法正确的是( )A、金属与非金属元素形成的化合物一定是离子化合物 B、干冰气化过程中只需克服分子间作用力 C、HF的热稳定性很好,是因为HF分子间存在氢键 D、常温常压下,气态单质分子中,每个原子的最外层都具有8电子稳定结构11. X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如图所示.若X原子的最外层电子数是内层电子数的2倍,下列说法中正确的是( )
10. 下列说法正确的是( )A、金属与非金属元素形成的化合物一定是离子化合物 B、干冰气化过程中只需克服分子间作用力 C、HF的热稳定性很好,是因为HF分子间存在氢键 D、常温常压下,气态单质分子中,每个原子的最外层都具有8电子稳定结构11. X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如图所示.若X原子的最外层电子数是内层电子数的2倍,下列说法中正确的是( ) A、X、Y对应的氧化物都是酸性氧化物 B、最高价氧化物对应水化物的酸性W比Z弱 C、Z比Y更容易与氢气化合 D、W、Z对应的最高价氧化物对应的水化物的相对分子质量相等12. 下列说法或表示方法中,正确的是( )
A、X、Y对应的氧化物都是酸性氧化物 B、最高价氧化物对应水化物的酸性W比Z弱 C、Z比Y更容易与氢气化合 D、W、Z对应的最高价氧化物对应的水化物的相对分子质量相等12. 下列说法或表示方法中,正确的是( )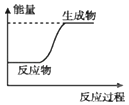 A、等质量的硫蒸气和硫固体分别完全燃烧,前者放出的热量少 B、如图可表示C和H2O(g)反应过程中的能量变化 C、吸热反应一定要加热,才能进行 D、已知中和热为57.3 kJ•mol﹣1 , 则浓硫酸与NaOH溶液反应生成 1mol H2O时,共放出57.3 kJ的能量13. 在含有元素硒(Se) 的保健品已经开始进入市场,已知它与氧元素同族,与钾元素同周期,关于硒的说法中正确的是( )A、Se的原子序数为 24 B、Se的氢化物的还原性比硫化氢气体强 C、Se的非金属性比Br强 D、Se的最高价氧化物分子式为:SeO214. 几种短周期素的原子半径及主要化合价如下表:下列叙述正确的是( )
A、等质量的硫蒸气和硫固体分别完全燃烧,前者放出的热量少 B、如图可表示C和H2O(g)反应过程中的能量变化 C、吸热反应一定要加热,才能进行 D、已知中和热为57.3 kJ•mol﹣1 , 则浓硫酸与NaOH溶液反应生成 1mol H2O时,共放出57.3 kJ的能量13. 在含有元素硒(Se) 的保健品已经开始进入市场,已知它与氧元素同族,与钾元素同周期,关于硒的说法中正确的是( )A、Se的原子序数为 24 B、Se的氢化物的还原性比硫化氢气体强 C、Se的非金属性比Br强 D、Se的最高价氧化物分子式为:SeO214. 几种短周期素的原子半径及主要化合价如下表:下列叙述正确的是( )元素代号
X
Y
Z
W
原子半径/pm
160
143
70
66
主要化合价
+2
+3
+5、+3、﹣3
﹣2
A、X、Y元素的金属性X<Y B、一定条件下,Z单质与W的常见单质直接生成ZW2 C、Y的最高价氧化物对应的水化物能溶于氨水 D、Z的气态氢化物与其最高价氧化物对应的水化物可以反应15. 氢化钠(NaH)是一种白色的离子化合物,其中钠元素是+1价;氢化钠与水反应放出H2 . 下列叙述中,正确的是( )A、NaH在水中显碱性 B、NaH中氢元素的离子的电子层排布与氖原子的电子层排布相同 C、微粒半径H﹣<Li+ D、NaH与H2O反应时,水作还原剂16. 表是某些化学键的键能,则生成2mol H2O(g)时,放出的能量为( )化学键
H﹣H
O=O
H﹣O
键能(KJ/mol)
436
496
463
A、242KJ B、442 KJ C、484 KJ D、448KJ二、非选择题
-
17. 表是元素周期表的一部分,已知⑤为短周期元素,其单质为淡黄色固体,据表回答有关问题:
①
②
③
④
⑤
⑥
⑦
⑧
⑨
(1)、画出元素⑧的原子结构示意图(2)、在这些元素中,最活泼的非金属元素是 , 最不活泼的元素是(写元素符号 ).(3)、在这些元素的最高价氧化物对应水化物中,碱性最强的是(写化学式),呈两性的氢氧化物是(写化学式),写出两者之间反应的离子方程式:(4)、在⑥与⑨中,化学性质较活泼的是(写元素符号 ),写出可以验证该结论的一个化学反应方式 .18. 某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.(1)、Ⅰ.将钠、钾、镁、铝各1mol分别投入到足量的0.1mol•L﹣1的盐酸中,试预测实验结果:与盐酸反应最快.(2)、Ⅱ.利用下图装置可以验证非金属性的变化规律.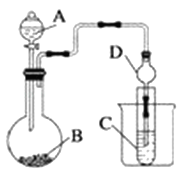
仪器A的名称为 , 干燥管D的作用是 .
(3)、若要证明非金属性:S>C>Si,则A中加、B中加NaHCO3溶液、C中加 , 观察到C中溶液的现象为 .19. 填写下列空白:(1)、某元素的气态氢化物的化学式XH4 , 则其最高价氧化物对应的水化物的化学式为 .(2)、氧元素有三种核素16O、17O、18O,它们在自然界中所占的原子个数百分比分别为a%、b%、c%,则氧元素的相对原子质量为 .(3)、物质的量相同的H2O和D2O与足量钠反应,放出的气体的质量之比为 .(4)、X2﹣含中子N个,X的质量数为A,则1g X的氢化物中含质子的物质的量是mol.(5)、铷和另一种碱金属形成的合金4.6g与足量的水反应后,产生0.2g氢气,则此合金中另一碱金属可能是: .20. A,B,C,D,E、F、G七种短周期元素,原子序数依次增大.由A、B形成的单质在一定条件下可生成气体X且X的水溶液呈碱性;D原子K层电子数是其M层电子数的2倍;E的简单阳离子与X具有相同电子数,且E的简单阳离子是同周期中简单离子半径最小的元素;F元素的原子最外层比次外层少两个电子,C和G的最外层电子数之和为13.则(1)、C在周期表中的位置为;(2)、写出:D在C单质中燃烧所生成淡黄色的固体的电子式(3)、A,B,D,E四种元素的原子半径由大到小的顺序为 . (用元素符号表示 )(4)、G的单质在反应中常作氧化剂,该单质的水溶液与F的低价氧化物反应的化学方程式为 .(5)、写出由A,C,D,F这四种元素共同组成的2种化合物在水溶液中发生反应的离子方程式: .21. 某同学设计如下三个实验方案以探究某反应是放热反应还是吸热反应: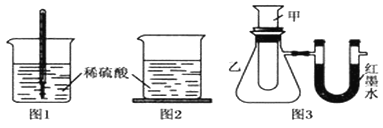
方案一:如图1,在小烧杯里放一些除去氧化铝保护膜的铝片,然后向烧杯里加入10mL 2mol•L﹣1稀硫酸,再插入一支温度计,温度计的温度由20℃逐渐升至35℃,随后,温度逐渐下降至30℃,最终停留在20℃.
方案二:如图2,在烧杯底部用熔融的蜡烛粘一块小木片,在烧杯里加入10mL 2mol•L﹣1硫酸溶液,再向其中加入氢氧化钠溶液,片刻后提起烧杯,发现小木片脱落下来.
方案三:如图3,甲试管中发生某化学反应,实验前U形管红墨水液面相平,在化学反应过程中,通过U形管两侧红墨水液面高低判断某反应是吸热反应还是放热反应.
序号
甲试管里发生反应的物质
U形管里红墨水液面
①
氧化钙与水
左低右高
②
氢氧化钡晶体与氯化铵晶体(充分搅拌)
?
③
铝片与烧碱溶液
左低右高
④
铜与浓硝酸
左低右高
根据上述实验回答相关问题:
(1)、方案一中,温度先升高的原因是 , 升至最大值后又逐渐下降的原因是 .(2)、方案二中,小木片脱落的原因是 .(3)、由方案三的现象得出结论:①③④组物质发生的反应都是(填“吸热”或“放热”)反应.(4)、方案三实验②的U形管中的现象为 , 说明反应物的总能量(填“大于”“小于”或“等于”)生成物的总能量.