2017年山东省德州市禹城市中考化学一模试卷
试卷更新日期:2017-07-19 类型:中考模拟
一、选择题
-
1. 在下列生活和生产过程中,发生了化学变化的是( )A、菠萝榨汁 B、海水晒盐 C、谷物酿酒 D、石头雕像2. 下列图示实验操作正确的是( )A、
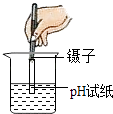 测待测溶液pH
B、
测待测溶液pH
B、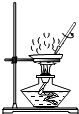 蒸发
C、
蒸发
C、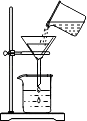 过滤
D、
过滤
D、 氧气验满
3. 下列归类错误的是( )
氧气验满
3. 下列归类错误的是( )选项
归类
物质或现象
A
化石燃料
煤、石油、天然气
B
常见的碱
烧碱、熟石灰、纯碱
C
营养物质
淀粉、油脂、蛋白质
D
环境问题
酸雨、温室效应、PM2.5超标
A、A B、B C、C D、D4. 我国药学家屠呦呦因研究青蒿素获得2015年诺贝尔医学奖.青嵩素的化学式为C15H22O5 , 下列说法正确的是( )A、青蒿素分子由三种元素组成 B、青蒿素是一种有机物 C、青蒿素含有42个原子 D、青蒿素中氢元素的质量分数最大5. 甲烷和水在一定条件下反应可制得水煤气(混合气体),下图即该反应的微观示意图.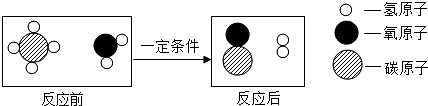
根据上述微观示意图得出的结论中,正确的是( )
A、该反应前后各元素的化合价均不变 B、该反应属于置换反应 C、参加反应的甲烷和水的质量比为8:9 D、反应后生成的 和
和 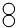 两物质的分子个数比为1:1
6. 如图是甲、乙、丙三种物质的溶解度曲线,下列说法错误的是( )
两物质的分子个数比为1:1
6. 如图是甲、乙、丙三种物质的溶解度曲线,下列说法错误的是( )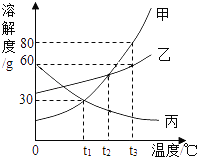 A、甲中混有少量杂质乙,可采用降温结晶的方法进行提纯 B、t3℃时,将甲、丙的饱和溶液降温,甲溶液溶质的质量分数减小,丙不变 C、t2℃时,甲、丙溶液中溶质的质量分数甲>丙 D、t1℃时,60g水中溶解18g甲可得到其饱和溶液7. 逻辑推理是一种重要的化学思维方法,下列推理合理的是( )A、向某固体上滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐 B、因为氧化物含有氧元素,所以含氧元素的化合物都是氧化物 C、通常盐是由金属阳离子和酸根阴离子构成的,硝酸铵中没有金属阳离子,不属于盐 D、因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成里一定含有碳元素和氢元素8. 归纳与反思是学习化学的重要环节.下列各项归纳完全正确的是( )
A、甲中混有少量杂质乙,可采用降温结晶的方法进行提纯 B、t3℃时,将甲、丙的饱和溶液降温,甲溶液溶质的质量分数减小,丙不变 C、t2℃时,甲、丙溶液中溶质的质量分数甲>丙 D、t1℃时,60g水中溶解18g甲可得到其饱和溶液7. 逻辑推理是一种重要的化学思维方法,下列推理合理的是( )A、向某固体上滴加稀盐酸,有气泡产生,则该固体一定是碳酸盐 B、因为氧化物含有氧元素,所以含氧元素的化合物都是氧化物 C、通常盐是由金属阳离子和酸根阴离子构成的,硝酸铵中没有金属阳离子,不属于盐 D、因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成里一定含有碳元素和氢元素8. 归纳与反思是学习化学的重要环节.下列各项归纳完全正确的是( )A.性质与用途
B.安全常识
氧气有助燃性﹣﹣做燃料
熟石灰呈碱性﹣﹣改良酸性土壤
一氧化碳有还原性﹣﹣用于冶炼金属
皮肤沾上浓硫酸﹣﹣用氢氧化钠溶液中和
炒菜时油锅起火﹣﹣弃锅逃走
假酒中毒﹣﹣甲醇引起
C.日常生活经验
D.物质与微粒构成
区别软水和硬水﹣﹣肥皂水
衣服上的圆珠笔油﹣﹣用汽油或酒精搓洗
鉴别真黄金和假黄金(铜锌合金)﹣﹣观察颜色
金属铜﹣﹣由铜原子构成
氧气﹣﹣由氧气分子构成
氯化钠由Na+和Cl﹣构成
A、A B、B C、C D、D二、解答题
-
9. 化学用语是一种信息丰富,国际通用比较简明的化学语言,请用化学用语填空:(1)、最简单的有机物 .(2)、保持氮气化学性质的最小粒子 .(3)、硝酸银溶液中的阴离子 .10. 生活与化学密切相关,处处充满着化学知识.(1)、下列食物中,维生素含量比较丰富的是(填字母)
 (2)、下列食堂中的常见用品,其主要材料属于合成材料的是 (填字母).A、棉布围裙 B、陶瓷碗 C、不锈钢锅 D、塑料桶(3)、同学们在食堂外就闻到了菜香,用粒子观点解释其原因 .(4)、加钙牛奶可补充钙(填“单质”或“元素”),身体中一旦缺钙,可能患有的疾病是(填“骨质疏松”或“贫血”).(5)、我们常用洗涤剂清洗餐具上的油污,这是因为洗涤剂具有功能.11. 如图是元素周期表部分内容,请根据表中信息完成相关问题
(2)、下列食堂中的常见用品,其主要材料属于合成材料的是 (填字母).A、棉布围裙 B、陶瓷碗 C、不锈钢锅 D、塑料桶(3)、同学们在食堂外就闻到了菜香,用粒子观点解释其原因 .(4)、加钙牛奶可补充钙(填“单质”或“元素”),身体中一旦缺钙,可能患有的疾病是(填“骨质疏松”或“贫血”).(5)、我们常用洗涤剂清洗餐具上的油污,这是因为洗涤剂具有功能.11. 如图是元素周期表部分内容,请根据表中信息完成相关问题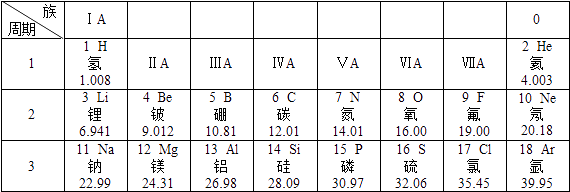 (1)、不同种元素最本质的区别是 .(2)、原子序数为1、6、8的三种元素形成的常见化合物的化学式为 , 其中6号元素的化合价是 .12. 请同学们搭乘“化学地铁”一起畅游物质世界吧!如图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站.“2﹣5号站”各站的对应物质属于不同类别的纯净物.
(1)、不同种元素最本质的区别是 .(2)、原子序数为1、6、8的三种元素形成的常见化合物的化学式为 , 其中6号元素的化合价是 .12. 请同学们搭乘“化学地铁”一起畅游物质世界吧!如图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站.“2﹣5号站”各站的对应物质属于不同类别的纯净物.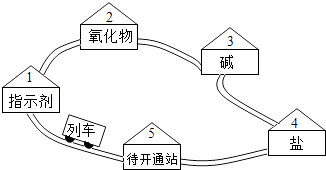 (1)、若列车上的物质为“碳酸钠溶液”.
(1)、若列车上的物质为“碳酸钠溶液”.①列车途径“1号站”时,若指示剂为紫色石蕊溶液,溶液变色.
②列车途经“2号站”时,若氧化物为二氧化碳,二氧化碳与碳酸钠溶液反应生成碳酸氢钠的化学方程式为 .
③列车途经“3号站”时,反应的化学方程式为(写一个).
(2)、“碳酸钠溶液”列车抵达“4号站”时,将列车上的物质更换为“稀盐酸”后出发.“稀盐酸”列车途经“5号站”时,反应的化学方程式为(写一个).
三、解答题
-
13. 下列图示装置常用于实验室制取气体,请根据如图回答问题.
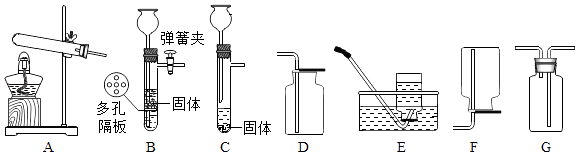 (1)、用高锰酸钾制取氧气,反应的化学方程式为 , 发生装置应选择
(1)、用高锰酸钾制取氧气,反应的化学方程式为 , 发生装置应选择(填代号).
(2)、欲制取CO2 , B装置相对C装置的优点是;收集CO2应选择装置(从A﹣F中选择)验满的方法是 , 欲干燥CO2 , 应将气体通过G装置,G种应加入的药品是 .14. 将一小块银白色的金属钠放置在空气中会发生下列变化:钠(Na) 钠的氧化物 氢氧化钠溶液 白色固体
[提出问题]:常温下钠与氧气反应,产物有哪些?
[查阅资料]:(1)钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,其反应的方程式如下:
Na2O+H2O=2NaOH;2Na2O2+2H2O=4NaOH+O2↑(2)CaCl2溶液呈中性
(1)、[作出猜想]:常温下钠与氧气反应的产物可能为.猜想1:① 猜想2:Na2O2 , 猜想3:Na2O2和NaOH
(2)、[实验探究一]:实验操作
实验现象
实验结论
取少量钠的氧化物加入足量蒸馏水
②
猜想1正确
(3)、[继续探究]:钠在空气中放置较长时间发生反应生成的白色固体[作出猜想]生成的白色固体可能是1是:Na2CO3 2是:Na2CO3和NaOH
[实验探究二]:
实验操作
实验现象
实验结论
取少量白色固体配成溶液,加入适量CaCl2溶液
③
白色固体成分为Na2CO3和NaOH
将上述反应后的溶液过滤,取少量滤液滴加④
⑤
(4)、[反思拓展]①也可以用稀盐酸区别Na2O与Na2O2 , Na2O2与稀盐酸的化学反应方程式为:2Na2O2+4HCl=4NaCl+2H2O+X↑,X的化学式为⑥ .
②实验结束后,废液缸中溶液显碱性,请你设计一个实验方案处理废液⑦ .
四、解答题
-
15. 某氢氧化钠样品中提有氯化钠,为测定样品中氢氧化钠的质量分数,称取5g样品,加入27g水完全溶解后,缓慢加入稀盐酸,同时测定溶液的pH=7时,刚好用去10%的稀盐酸36.5g,试计算:(1)、将100g质量分数为38%的浓盐酸稀释成10%的稀盐酸,需加水的质量为g.(2)、样品中氢氧化钠的质量分数.(3)、反应后所得溶液中溶质的质量分数.