山西省吕梁市交城县2019-2020学年九年级上学期化学期中考试试卷
试卷更新日期:2019-11-22 类型:期中考试
一、单选题
-
1. 下列变化中只涉及物理变化的是( )A、野火烧不尽,春风吹又生 B、春蚕到死丝方尽,蜡炬成灰泪始干 C、只要功夫深,铁杵磨成针 D、爆竹声中一岁除,春风送暖入屠苏2. 下列物质中属于纯净物的是( )A、冰水混合物 B、稀有气体 C、人呼出的气体 D、净化后的空气3. 地壳中含量最多的金属元素与含量最多的非金属元素形成的化合物为( )A、Fe2O3 B、SiO2 C、CaO D、Al2O34. 近几年全国环境质量总体上有好转趋势,但仍有56%的城市未达到二级标准。造成这些城市污染的原因之一可能是( )A、大量燃烧含硫煤 B、植物的光合作用 C、人和动物的呼吸 D、利用太阳能烧水5. 某学生用托盘天平称量2.5克药品时,发现指针向右偏转,此时应该()A、加砝码 B、加药品 C、减少药品 D、调节左右螺母6. 下列物质含有氢分子的是()A、H2 B、H2O2 C、H2CO3 D、H2O7. 下列各图中“○”“●”分别表示两种不同元素的原子,其中表示混合物的是( )A、
 B、
B、 C、
C、 D、
D、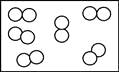 8. 吗啡的化学式是C17H19NO3 ,下列说法中正确的是( )A、吗啡属于氧化物 B、各元素中碳元素的质量分数最大 C、吗啡分子由40个原子 D、碳、氢、氮、氧四种元素的质量比为17:19:1:39. 下列物质按照带横线元素的化合价由低到高的顺序排列的是()A、KIO3、I2、KI B、HClO3、HCl、Cl2 C、MnO2、K2MnO4、KMnO4 D、NaNO3、NH4Cl、NO210. 科学家研制出一种新型催化剂,可用于去除装修残留的甲醛(化学式为 CH2O),该反应过程的微观示意图如下。下列说法正确的是( )
8. 吗啡的化学式是C17H19NO3 ,下列说法中正确的是( )A、吗啡属于氧化物 B、各元素中碳元素的质量分数最大 C、吗啡分子由40个原子 D、碳、氢、氮、氧四种元素的质量比为17:19:1:39. 下列物质按照带横线元素的化合价由低到高的顺序排列的是()A、KIO3、I2、KI B、HClO3、HCl、Cl2 C、MnO2、K2MnO4、KMnO4 D、NaNO3、NH4Cl、NO210. 科学家研制出一种新型催化剂,可用于去除装修残留的甲醛(化学式为 CH2O),该反应过程的微观示意图如下。下列说法正确的是( )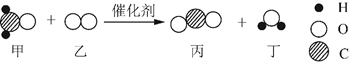 A、物质甲为甲醛,其分子由碳原子和水分子构成 B、物质乙中氧元素的化合价为-2价 C、该反应前后原子种类和数目均发生改变 D、该反应消耗物质甲和生成物质丁的质量比为5﹕3
A、物质甲为甲醛,其分子由碳原子和水分子构成 B、物质乙中氧元素的化合价为-2价 C、该反应前后原子种类和数目均发生改变 D、该反应消耗物质甲和生成物质丁的质量比为5﹕3二、填空题
-
11. 化学与生活息息相关。
请将下列短文中加点的文字转化为恰当的化学符号,填在旁边的横线上:刚玉是宝石的一种,它的主要成分是氧化铝 (氧化铝中铝元素显+3价 ),其硬度仅次于金刚石 ,一些刚玉由于混有少量亚铁离子 等杂质而显蓝色,俗称蓝宝石。
12. “见著知微,见微知著”是化学思维方法。 (1)、从宏观知微观
(1)、从宏观知微观水与50mL乙醇混合后,溶液体积小于100mL,微观解释为;
气体X在氧气中燃烧生成氮气和水,X分子中一定含有的原子是和 填符号 。
(2)、从微观知宏观微粒A最外层电子数是 , 在化学反应中容易 填“得”或“失” 电子;
微粒A,B,C,D,E中,对应单质化学性质最稳定的是 填编号,下同 ,属于同一种元素的是和。
13. 请阅读以下摘自今年的《苏州日报》,与化学关系密切的信息,并填空.[资讯1]据市环境监测站专家分析:5月4日至7日,由于阳光灿烂,臭氧(O3)也出来“作怪”,连续四天的日平均浓度也均超标.臭氧在常温常压下是淡蓝色气体,稳定性极差,可自行分解为氧气.臭氧在空气中达到一定浓度可刺激呼吸道.大气中臭氧浓度超标的原因是:在静风条件下强烈的阳光就成为氮氧化物的催化剂,从而推高了臭氧浓度,形成污染.
(1)、臭氧“自行分解”的化学方程式为;若氮氧化物假定为二氧化氮,强光条件下促使其分解产生了O3和N2.则该反应的化学方程式为.(2)、[资讯2]吴江某公司研发的一层看似普通的白色薄膜,却有超高防水透气、阻燃、抗菌和耐腐蚀的神奇功能…这种膜的专业术语叫聚四氟乙烯纳米微孔薄膜,由聚四氟乙烯树脂经特殊设备和工艺制作而成,该树脂是一种超高分子量材料.制作这种薄膜的聚四氟乙烯树脂[(CF2CF2)n]的相对分子质量为1×108 , 其n值等于.碳元素的质量分数为.
三、流程题
-
14. 空气是宝贵的自然资源。如图是以空气和其他必要的原料合成氮肥(NH4HCO3)的流程。请按要求回答下列问题:
 (1)、步骤①中得到的“其它气体”中主要成分是。(2)、现代工业常利用氮分子大于氧分子的特性,使用特制的分子筛把空气中的氧气分离出来,此过程属于(选填“物理”、“化学“)变化。(3)、若用下面三幅模型图表示步骤②中反应过程,则从反应开始到完成的排列顺序为(用字母表示)
(1)、步骤①中得到的“其它气体”中主要成分是。(2)、现代工业常利用氮分子大于氧分子的特性,使用特制的分子筛把空气中的氧气分离出来,此过程属于(选填“物理”、“化学“)变化。(3)、若用下面三幅模型图表示步骤②中反应过程,则从反应开始到完成的排列顺序为(用字母表示) (4)、写出步骤③中发生反应的化学方程式:。
(4)、写出步骤③中发生反应的化学方程式:。四、推断题
-
15. 在如图转化关系中,生成物D能使带火星的木条复燃,H能使澄清石灰水变浑浊,在反应②中,B的质量和化学性质均没有改变。
 (1)、图中A是 , 它的颜色为B是 , 它的颜色为D是 , H是(2)、属于化合反应的是(填序号)。
(1)、图中A是 , 它的颜色为B是 , 它的颜色为D是 , H是(2)、属于化合反应的是(填序号)。五、实验题
-
16. 根据下列装置图,结合所学知识,请回答下列问题。
 (1)、图中仪器a的名称是 , b的名称是。(2)、实验室用用高锰酸钾制取氧气,可选择作气体发生装置(填字母代号),该装置的不足之处是 , 此法制取氧气的化学方程式为 , 当用C收集氧气时,当看到时表明气体已收集满。(3)、组装仪器时连接玻璃管和胶皮管的操作时先把玻璃管口 , 然后稍稍用力即可把玻璃管插入胶皮管;17. 小明参观某养鱼池时,好奇的发现农民向养鱼池中撒一种淡黄色固体——过氧化钙,用来增加鱼池中的含氧量。
(1)、图中仪器a的名称是 , b的名称是。(2)、实验室用用高锰酸钾制取氧气,可选择作气体发生装置(填字母代号),该装置的不足之处是 , 此法制取氧气的化学方程式为 , 当用C收集氧气时,当看到时表明气体已收集满。(3)、组装仪器时连接玻璃管和胶皮管的操作时先把玻璃管口 , 然后稍稍用力即可把玻璃管插入胶皮管;17. 小明参观某养鱼池时,好奇的发现农民向养鱼池中撒一种淡黄色固体——过氧化钙,用来增加鱼池中的含氧量。小明刚学完氧气的实验室制法,于是他想可否用过氧化钙制取氧气。
(提出问题)过氧化钙可否用于制取氧气?
(查阅资料)部分内容如下:过氧化钙(CaO2)室温下稳定,在300℃时分解生成氧气,主要用途可做增氧剂、杀菌剂等。
(猜想与验证)
(1)、小明依据资料显示:加热过氧化钙可制取氧气。实验装置
实验主要过程

①检查装置气密性。操作如下:先将导管伸入液面下,用手紧握试管,观察到 , 松开手后,导管口有液面上升。②加入过氧化钙,加热,当 , 开始收集氧气。③收集满一瓶气体,并将集气瓶(填“正放”或“倒放”)在桌上。④停止加热。熄灭酒精灯前,应。⑤检验气体。方法是。
实验结论:加热过氧化钙可制取氧气。
(2)、小明联想到农民用过氧化钙增加鱼池中的含氧量,提出猜想Ⅱ.猜想Ⅱ:过氧化钙与水反应可制取氧气。
实验装置
实验主要过程

①检查装置气密性。
②加入过氧化钙和水后,有少量细小气泡缓慢放出。
③在导管口几乎收集不到气体。
该装置放置到第二天,集气瓶中只收集到极少量气体,振荡试管后仍有少量细小气泡缓慢放出。
实验结论:不能用过氧化钙与水反应制取氧气。
分析与反思:
虽然没有快速收集到大量氧气,但由此实验现象,小明推导出农民用过氧化钙做增氧剂的主要原因是。
(3)、小明希望对此实验进行改进,使该反应加快,你能帮他提出建议吗?你的合理建议:。
这些建议是否可行,还需进一步通过实验验证。
六、计算题
-
18. 把氯酸钾和二氧化锰的混合物共7g放在试管中加热,完全反应后,冷却。称得剩余固体5.08g。
求:
(1)、根据质量守恒定律计算可制得氧气多少克?(2)、剩余固体中含有什么物质?各多少克?
-
-