山东省泰安市高新区2019-2020学年九年级上学期化学期中考试试卷
试卷更新日期:2019-11-22 类型:期中考试
一、单选题
-
1. 把少量生活中的物质分别放入水中,充分搅拌,可以得到溶液的是( )A、面粉 B、牛奶 C、蔗糖 D、植物油2. 安全事故无小事。下图是一种危险化学品警示标记,在运输时应张贴该标记的是( )
 A、食盐 B、纯碱 C、酒精 D、烧碱3. 下列关于溶液的说法中正确的是( )A、一瓶液体长期放置后不出现分层,该液体就是溶液 B、溶液中不能同时存两种溶质 C、外界条件不改变,溶质溶剂不会分离 D、溶液一定是无色、澄清的4. 正确规范的操作是实验成功和人身安全的重要保证。下列实验操作正确的是( )A、
A、食盐 B、纯碱 C、酒精 D、烧碱3. 下列关于溶液的说法中正确的是( )A、一瓶液体长期放置后不出现分层,该液体就是溶液 B、溶液中不能同时存两种溶质 C、外界条件不改变,溶质溶剂不会分离 D、溶液一定是无色、澄清的4. 正确规范的操作是实验成功和人身安全的重要保证。下列实验操作正确的是( )A、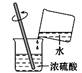 稀释浓硫酸
B、
稀释浓硫酸
B、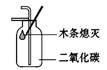 二氧化碳验满
C、
二氧化碳验满
C、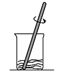 溶解固体
D、
溶解固体
D、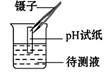 测定pH
5. 下列选项中物质的俗名、化学式、用途完全对应的是( )A、浓硫酸 HCl 生产药品 B、生石灰 CaO 干燥剂 C、食盐 NaCl 除铁锈 D、火碱 NaOH 改良酸性土壤6. 下列数据为常见水果的pH,其中酸性最强的是( )A、
测定pH
5. 下列选项中物质的俗名、化学式、用途完全对应的是( )A、浓硫酸 HCl 生产药品 B、生石灰 CaO 干燥剂 C、食盐 NaCl 除铁锈 D、火碱 NaOH 改良酸性土壤6. 下列数据为常见水果的pH,其中酸性最强的是( )A、 柠檬pH(2~3)
B、
柠檬pH(2~3)
B、 橙子pH(3~4)
C、
橙子pH(3~4)
C、 西红柿pH(4~5)
D、
西红柿pH(4~5)
D、 西瓜pH(5~6)
7. 如图是物质X溶于水中发生解离的微观示意图,其中能说明X是一种酸的是( )A、
西瓜pH(5~6)
7. 如图是物质X溶于水中发生解离的微观示意图,其中能说明X是一种酸的是( )A、 B、
B、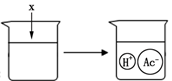 C、
C、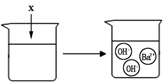 D、
D、 8. 下列洗涤中发生乳化现象的是( )A、用汽油除去衣服上的油污 B、用洗洁精洗净餐具上的油污 C、用水洗去盘子中的水果汁 D、用稀盐酸除去铁锈9. 下列物质不能与氢氧化钙溶液发生化学反应的是( )A、稀硫酸 B、氧化铁 C、紫色石蕊试液 D、碳酸钠溶液10. 下列物质露置于空气中,质量增大且发生化学变化的是( )A、浓硫酸 B、浓盐酸 C、食盐 D、氢氧化钠11. 增大二氧化碳在水中的溶解度的方法( )A、升温增压 B、升温减压 C、降温增压 D、降温减压12. 下列各变化属于物理变化的是( )A、盐酸使指示剂变色 B、用稀盐酸除去金属表面的铁锈 C、浓盐酸在空气里敞口放置瓶口有白雾生成 D、用小木棍蘸取少量浓硫酸,小木棍逐渐变为黑色13. 图3是X、Y两种固体物质的溶解度曲线。下列说法中正确的是( )
8. 下列洗涤中发生乳化现象的是( )A、用汽油除去衣服上的油污 B、用洗洁精洗净餐具上的油污 C、用水洗去盘子中的水果汁 D、用稀盐酸除去铁锈9. 下列物质不能与氢氧化钙溶液发生化学反应的是( )A、稀硫酸 B、氧化铁 C、紫色石蕊试液 D、碳酸钠溶液10. 下列物质露置于空气中,质量增大且发生化学变化的是( )A、浓硫酸 B、浓盐酸 C、食盐 D、氢氧化钠11. 增大二氧化碳在水中的溶解度的方法( )A、升温增压 B、升温减压 C、降温增压 D、降温减压12. 下列各变化属于物理变化的是( )A、盐酸使指示剂变色 B、用稀盐酸除去金属表面的铁锈 C、浓盐酸在空气里敞口放置瓶口有白雾生成 D、用小木棍蘸取少量浓硫酸,小木棍逐渐变为黑色13. 图3是X、Y两种固体物质的溶解度曲线。下列说法中正确的是( ) A、t1℃时X的溶解度大于Y的溶解度 B、t2℃时X的溶解度等于Y的溶解度 C、t3℃时X的饱和溶液降温至t2℃时,变为不饱和溶液 D、t1℃时Y的不饱和溶液升温至t2℃时,变为饱和溶液14. 下列表述正确的是( )A、稀盐酸和稀硫酸化学性质相似的原因是溶液中都含有H+ B、用pH试纸测定某未知溶液的pH为5.5 C、生成盐和水的反应一定是中和反应 D、使酚酞试液变红色的一定是碱15. 在配制一定溶质质量分数的蔗糖溶液时,导致溶液中蔗糖的质量分数偏大的可能原因有( )A、用量筒量取水时俯视读数 B、用来配制溶液的烧杯刚用少量蒸馏水润洗过 C、用托盘天平称取蔗糖时,将蔗糖放在右盘,且称量时使用了游码 D、用了含少量杂质的蔗糖配制溶液16. 化学兴趣小组利用下图所示装置进行实验,打开止水夹,将液体a滴入试管①中与固体b接触,若试管②中的导管口没有气泡产生,则液体a和固体b的组合可能是( )
A、t1℃时X的溶解度大于Y的溶解度 B、t2℃时X的溶解度等于Y的溶解度 C、t3℃时X的饱和溶液降温至t2℃时,变为不饱和溶液 D、t1℃时Y的不饱和溶液升温至t2℃时,变为饱和溶液14. 下列表述正确的是( )A、稀盐酸和稀硫酸化学性质相似的原因是溶液中都含有H+ B、用pH试纸测定某未知溶液的pH为5.5 C、生成盐和水的反应一定是中和反应 D、使酚酞试液变红色的一定是碱15. 在配制一定溶质质量分数的蔗糖溶液时,导致溶液中蔗糖的质量分数偏大的可能原因有( )A、用量筒量取水时俯视读数 B、用来配制溶液的烧杯刚用少量蒸馏水润洗过 C、用托盘天平称取蔗糖时,将蔗糖放在右盘,且称量时使用了游码 D、用了含少量杂质的蔗糖配制溶液16. 化学兴趣小组利用下图所示装置进行实验,打开止水夹,将液体a滴入试管①中与固体b接触,若试管②中的导管口没有气泡产生,则液体a和固体b的组合可能是( ) A、稀盐酸和碳酸钠 B、水和氢氧化钠 C、水和生石灰 D、水和硝酸铵17. 如表所示的概念完全符合如图关系的是( )
A、稀盐酸和碳酸钠 B、水和氢氧化钠 C、水和生石灰 D、水和硝酸铵17. 如表所示的概念完全符合如图关系的是( )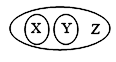
X
Y
Z
A
溶液
溶剂
溶质
B
饱和溶液
不饱和溶液
浓溶液
C
酸
碱
化合物
D
易溶
微溶
可溶
A、A B、B C、C D、D18. 下列关于溶液的说法正确的是( )A、同种固态溶质的饱和溶液的溶质的质量分数一定比不饱和溶液的溶质的质量分数大 B、在某固态物质的饱和溶液里加入其他任何物质都不能溶解 C、某固态物质的饱和溶液,当温度升高时,若溶液质量不变,则溶质的质量分数不变 D、温度升高,KNO3的饱和溶液就变成不饱和溶液,所以溶液的溶质的质量分数也随之而减少19. 下列实验方案设计合理的是( )A、除去氢氧化钠溶液中少量的碳酸钠………加入过量的稀盐酸 B、鉴别稀盐酸和稀硫酸…………分别滴加氯化钡溶液 C、干燥氯化氢气体………………将气体通过氢氧化钠固体 D、除去氯化钠固体中的硝酸钾……溶解成较高温度下的饱和溶液,然后降温结晶20. 如图是a、b、c三种固体物质(不含结晶水)的溶解度曲线。下列叙述正确的是( )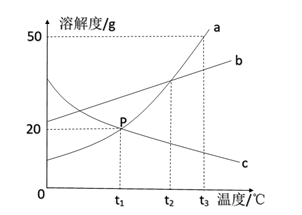 A、t1℃时,a、c两种物质饱和溶液的溶质质量分数为20% B、将接近饱和的c物质的溶液变成饱和溶液,可采用加溶质、降温等方法 C、将a、b、c三种物质的饱和溶液从t2℃降温至t1℃,所得溶液中溶质质量分数的大小关系为b>a=c D、将150g a物质的饱和溶液从t3℃降温至t1℃,可析出30g a物质
A、t1℃时,a、c两种物质饱和溶液的溶质质量分数为20% B、将接近饱和的c物质的溶液变成饱和溶液,可采用加溶质、降温等方法 C、将a、b、c三种物质的饱和溶液从t2℃降温至t1℃,所得溶液中溶质质量分数的大小关系为b>a=c D、将150g a物质的饱和溶液从t3℃降温至t1℃,可析出30g a物质二、填空题
-
21. 下图为“胃酸完全抑制剂”的标签。
 (1)、“胃酸完全抑制剂”主要成分中属于盐的物质是(写化学式)。(2)、服用“胃酸完全抑制剂”后在胃内发生反应的反应方程式是(任写一个),它属于基本反应类型中的。22. 宏观和微观相联系是化学独特的思维方式,微观探析化学反应的规律是化学科学的核心任务。根据下列微观示意图回答问题。
(1)、“胃酸完全抑制剂”主要成分中属于盐的物质是(写化学式)。(2)、服用“胃酸完全抑制剂”后在胃内发生反应的反应方程式是(任写一个),它属于基本反应类型中的。22. 宏观和微观相联系是化学独特的思维方式,微观探析化学反应的规律是化学科学的核心任务。根据下列微观示意图回答问题。 (1)、从微观的角度说明图示反应的实质是;(2)、该反应的化学方程式是。(3)、若反应中NaOH稍过量,则反应后,溶液中存在的微观粒子有。23. 已知A,B,C三种物质的溶解度曲线如图所示。
(1)、从微观的角度说明图示反应的实质是;(2)、该反应的化学方程式是。(3)、若反应中NaOH稍过量,则反应后,溶液中存在的微观粒子有。23. 已知A,B,C三种物质的溶解度曲线如图所示。 (1)、在阴影区域部分,处于不饱和状态的是(选填“A,B,C”)。(2)、P点表示的含义为。(3)、向试管中滴入2mL水后,若X中有固体析出,则X为(选填“A,B,C”)。
(1)、在阴影区域部分,处于不饱和状态的是(选填“A,B,C”)。(2)、P点表示的含义为。(3)、向试管中滴入2mL水后,若X中有固体析出,则X为(选填“A,B,C”)。三、简答题
-
24. 归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出盐酸的五条化学性质(如图所示,连线表示相互反应)。
 (1)、为了验证性质①,小红将紫色石蕊溶液加到盐酸中,溶液变色。(2)、盐酸的性质③决定了盐酸可用于清除铁锈,写出该反应的化学方程式: , 该反应的实验现象是。(3)、为验证性质⑤,应选用的物质是(写一种物质的名称)。
(1)、为了验证性质①,小红将紫色石蕊溶液加到盐酸中,溶液变色。(2)、盐酸的性质③决定了盐酸可用于清除铁锈,写出该反应的化学方程式: , 该反应的实验现象是。(3)、为验证性质⑤,应选用的物质是(写一种物质的名称)。四、实验题
-
25. 下图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
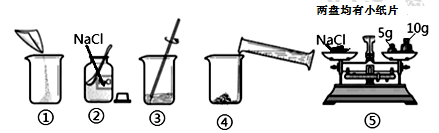 (1)、用上图表示的序号表示配制溶液的正确操作顺序。(2)、图③中玻璃棒的作用是。(3)、称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示数如图,则称取NaCl的实际质量为;若当时药品与砝码放反了,称取药品的质量变为。
(1)、用上图表示的序号表示配制溶液的正确操作顺序。(2)、图③中玻璃棒的作用是。(3)、称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示数如图,则称取NaCl的实际质量为;若当时药品与砝码放反了,称取药品的质量变为。 (4)、根据计算需要量取水的体积是mL(水的密度为1g/mL)。26. 进行化学实验是化学学习和探究的主要途径,根据要求完成下列实验探究。(1)、用控制变量方法探究影响物质溶解性的因素。
(4)、根据计算需要量取水的体积是mL(水的密度为1g/mL)。26. 进行化学实验是化学学习和探究的主要途径,根据要求完成下列实验探究。(1)、用控制变量方法探究影响物质溶解性的因素。实验一
实验二


①实验一目的是探究对硝酸钾溶解性的影响;
②实验二是探究溶剂种类对物质溶解性的影响,该实验中需要控制的变量是温度和。
(2)、某化学兴趣小组在进行酸碱中和反应的实验探究时,向烧杯中的氢氧化钠溶液滴加稀盐酸一会儿后,发现忘记添加酸碱指示剂。某同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到试管中溶液不变色。于是针对此溶液的成分,同学们进行了科学探究。A.猜想与假设:
猜想一:反应后氢氧化钠过量,溶液呈碱性;
猜想二:氢氧化钠与盐酸恰好完全中和,溶液呈中性;
猜想三:反应后稀盐酸过量,溶液显酸性 。
同学们经过讨论后觉得猜想一错误,其理由是:。
B.设计并进行实验:
①化学兴趣小组的同学为了验证自己的猜想,设计了实验方案一:
实验步骤
实验现象
实验结论
用洁净、干燥的玻璃棒蘸取少量反应后的溶液滴在干燥的pH试纸上,观察颜色变化并与标准比色卡对比。
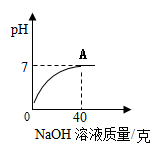
pH7
(填“>”、“=”或“<”)
猜想二不成立,猜想三成立
②请你设计另一个实验方案(与实验方案一不同),验证猜想三成立,并填写下表:
验步骤
实验现象
实验结论
猜想二不成立,猜想三成立
五、计算题
-