江苏省无锡市江阴市四校2019-2020学年高一上学期理综-化学期中考试试卷
试卷更新日期:2019-11-18 类型:期中考试
一、单项选择题(每小题3分,共60分)
-
1. 在日常生活中会接触到许多物质,下列物质中属于碱性氧化物的是( )A、硫酸铵 B、二氧化碳 C、生石灰 D、乙醇2. 下列有关化学用语表示正确的是( )
A、中子数为10的氧原子: B、氯原子的结构示意图: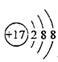 C、硝酸钡的化学式:BaNO3
D、水的摩尔质量为18g
3. 大气污染中,PM2.5是主要污染物之一,PM2.5 是指直径约为2.5微米的颗粒物,也称为可吸入肺颗粒物。根据以上信息你认为下列分散质中分散质粒子直径与PM2.5最接近的是(1微米=10-6 m)( )A、石灰水 B、豆浆 C、蔗糖水 D、泥水4. 相同物质的量的各固体或液体的体积并不相同,其主要原因是( )A、粒子质量不同 B、粒子大小不同 C、粒子间距离不同 D、粒子的数目不同5. 诺贝尔化学奖得主Gerhard Ertl对金属Pt(78号元素)表面催化CO氧化反应的模型进行了深入研究。下列关于202Pt和198Pt的说法正确的是( )A、202 Pt和198Pt的质子数相同,互称为同位素 B、202 Pt和198Pt的中子数相同,互称为同位素 C、202Pt和198Pt的核外电子数相同,是同一种核素 D、 202 Pt和198Pt的质量数不同,不能互称为同位素6. 如果你家里的食用花生油不小心混入了大量的水,利用你所学的知识,最简便的分离方法是( )A、
C、硝酸钡的化学式:BaNO3
D、水的摩尔质量为18g
3. 大气污染中,PM2.5是主要污染物之一,PM2.5 是指直径约为2.5微米的颗粒物,也称为可吸入肺颗粒物。根据以上信息你认为下列分散质中分散质粒子直径与PM2.5最接近的是(1微米=10-6 m)( )A、石灰水 B、豆浆 C、蔗糖水 D、泥水4. 相同物质的量的各固体或液体的体积并不相同,其主要原因是( )A、粒子质量不同 B、粒子大小不同 C、粒子间距离不同 D、粒子的数目不同5. 诺贝尔化学奖得主Gerhard Ertl对金属Pt(78号元素)表面催化CO氧化反应的模型进行了深入研究。下列关于202Pt和198Pt的说法正确的是( )A、202 Pt和198Pt的质子数相同,互称为同位素 B、202 Pt和198Pt的中子数相同,互称为同位素 C、202Pt和198Pt的核外电子数相同,是同一种核素 D、 202 Pt和198Pt的质量数不同,不能互称为同位素6. 如果你家里的食用花生油不小心混入了大量的水,利用你所学的知识,最简便的分离方法是( )A、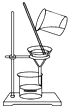 B、
B、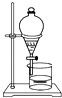 C、
C、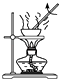 D、
D、 7. 化学与生活、社会发展息息相关,下列说法不正确的是( )A、“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 B、“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应 C、“春蚕到死丝方尽,蜡炬成灰泪始干” 诗句中涉及氧化还原反应 D、屠呦呦提取青蒿素加入乙醚萃取,此过程属于化学变化8. 目前市场上有一种专门为婴幼儿设计的电解质饮料,适合在婴幼儿感冒、发烧时快速补充体内流失的电解质成分。下列物质可用作该饮料中的电解质的是( )A、Fe B、葡萄糖 C、MgSO4 D、CO29. 小张最近去医院做了体检,得到的血液化验单中标有葡萄糖5.9 ×10-3mol·L-1 , 正常值为3.9~6.1×10-3mol·L-1表示该体检指标的物理量是( )A、溶解度(S) B、物质的量浓度( C ) C、质量分数(W) D、摩尔质量(M)10. 下列溶液中的c (Cl-) 与50mL 1mol·L-1 氯化铝溶液中的c (Cl-)相等的是( )A、150mL 3mol·L-1 氯化钾溶液 B、75mL 2mol·L-1 氯化铵溶液 C、150mL1mol·L-1 氯化钠溶液 D、75mL 1mol·L-1 氯化钡溶液11. 用NaCl固体配制100 mL 1.00 mol·L-1 NaCl溶液,不需要用到的仪器是( )A、100 mL容量瓶 B、胶头滴管 C、玻璃棒 D、试管12. 人们常用“84”消毒液对环境进行消毒。该消毒液无色,对某些有色物质有漂白作用,对该溶液进行焰色反应,呈黄色。你认为它可能的有效成分是( )A、NaOH B、NaClO C、KMnO4 D、Na2CO313. 下列氯化物中,既能由金属和氯气直接反应制得,又能由金属和盐酸反应制得的是( )A、CuCl2 B、FeCl2 C、AlCl3 D、FeCl314. 下列反应既是化合反应,又是氧化还原反应的是( )A、 B、 C、 D、15. 常温常压下,用等质量的He、CH4、O2、SO2分别吹出四个气球,其中气体为He的是( )A、
7. 化学与生活、社会发展息息相关,下列说法不正确的是( )A、“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 B、“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应 C、“春蚕到死丝方尽,蜡炬成灰泪始干” 诗句中涉及氧化还原反应 D、屠呦呦提取青蒿素加入乙醚萃取,此过程属于化学变化8. 目前市场上有一种专门为婴幼儿设计的电解质饮料,适合在婴幼儿感冒、发烧时快速补充体内流失的电解质成分。下列物质可用作该饮料中的电解质的是( )A、Fe B、葡萄糖 C、MgSO4 D、CO29. 小张最近去医院做了体检,得到的血液化验单中标有葡萄糖5.9 ×10-3mol·L-1 , 正常值为3.9~6.1×10-3mol·L-1表示该体检指标的物理量是( )A、溶解度(S) B、物质的量浓度( C ) C、质量分数(W) D、摩尔质量(M)10. 下列溶液中的c (Cl-) 与50mL 1mol·L-1 氯化铝溶液中的c (Cl-)相等的是( )A、150mL 3mol·L-1 氯化钾溶液 B、75mL 2mol·L-1 氯化铵溶液 C、150mL1mol·L-1 氯化钠溶液 D、75mL 1mol·L-1 氯化钡溶液11. 用NaCl固体配制100 mL 1.00 mol·L-1 NaCl溶液,不需要用到的仪器是( )A、100 mL容量瓶 B、胶头滴管 C、玻璃棒 D、试管12. 人们常用“84”消毒液对环境进行消毒。该消毒液无色,对某些有色物质有漂白作用,对该溶液进行焰色反应,呈黄色。你认为它可能的有效成分是( )A、NaOH B、NaClO C、KMnO4 D、Na2CO313. 下列氯化物中,既能由金属和氯气直接反应制得,又能由金属和盐酸反应制得的是( )A、CuCl2 B、FeCl2 C、AlCl3 D、FeCl314. 下列反应既是化合反应,又是氧化还原反应的是( )A、 B、 C、 D、15. 常温常压下,用等质量的He、CH4、O2、SO2分别吹出四个气球,其中气体为He的是( )A、 B、
B、 C、
C、 D、
D、 16. 用 表示阿伏加德罗常数的值,下列判断正确的是( )A、28g 含有的氮原子数目为 B、常温常压下, 含有的分子数目为 C、 溶液中含有的钾离子数目为 D、在标准状况下, LCO和 的混合物的物质的量为1mol17. 某一化学兴趣小组的同学在家中进行实验,按照图甲连接好线路,发现灯泡不亮,按图乙连接好线路,发现灯泡亮了。由此得出的以下结论中正确的是( )
16. 用 表示阿伏加德罗常数的值,下列判断正确的是( )A、28g 含有的氮原子数目为 B、常温常压下, 含有的分子数目为 C、 溶液中含有的钾离子数目为 D、在标准状况下, LCO和 的混合物的物质的量为1mol17. 某一化学兴趣小组的同学在家中进行实验,按照图甲连接好线路,发现灯泡不亮,按图乙连接好线路,发现灯泡亮了。由此得出的以下结论中正确的是( )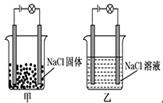 A、NaCl固体是非电解质 B、NaCl在水溶液中电离出了可以自由移动的离子 C、NaCl溶液是电解质 D、在NaCl溶液中,水电离出了大量的离子18. 某试管中盛有碘的水溶液,加入少量的CCl4 , 充分振荡,静置片刻后( )A、整个溶液变蓝色 B、整个溶液显紫红色 C、上层无色,下层紫红色 D、上层紫红色,下层无色19. 下列关于氧化剂与还原剂的判断正确的是( )A、反应CH4+2O2 CO2+2H2O中,O2是氧化剂,CH4是还原剂 B、反应Cl2+2NaOH=NaCl+NaClO+H2O中,Cl2是氧化剂,NaOH是还原剂 C、反应MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O中,HCl是氧化剂,MnO2是还原剂 D、反应2Na+2H2O=2NaOH+H2↑中,H2O既是氧化剂又是还原剂20. 检验溶液中是否含有某种离子,下列操作方法正确的是 ( )A、向某溶液中加AgNO3溶液产生白色沉淀,证明有Cl- B、向某溶液中加稀 HCl,无明显现象,再加入BaCl2 溶液产生白色沉淀,证明有SO42- C、向某溶液中加入稀 HCl,放出能使澄清的石灰水变浑浊的气体,证明有CO32- D、向某溶液中加入浓氢氧化钠溶液后加热,产生使湿润蓝色石蕊试纸变红的气体,证明含有NH4+21.(1)、绿色植物是空气天然的“净化器”,在家里科学选种一些绿色植物,可以达到净化空气、吸收有害物质的作用。科学研究发现,1公顷柳杉每月可以吸收160 kg SO2 , 则1公顷柳杉每月吸收的SO2的物质的量为。(2)、铅笔芯的主要成分是石墨和黏土,这些物质按照不同的比例加以混合、压制,就可以制成不同型号的铅笔芯。如果某铅笔芯质量的一半成分是石墨,且用铅笔写一个字消耗的质量约为1 mg。那么一个铅笔字含有的碳原子数约为。(3)、吸食“摇头丸”会严重破坏人体的中枢神经,“摇头丸”的化学式为C9H13N,请计算:
A、NaCl固体是非电解质 B、NaCl在水溶液中电离出了可以自由移动的离子 C、NaCl溶液是电解质 D、在NaCl溶液中,水电离出了大量的离子18. 某试管中盛有碘的水溶液,加入少量的CCl4 , 充分振荡,静置片刻后( )A、整个溶液变蓝色 B、整个溶液显紫红色 C、上层无色,下层紫红色 D、上层紫红色,下层无色19. 下列关于氧化剂与还原剂的判断正确的是( )A、反应CH4+2O2 CO2+2H2O中,O2是氧化剂,CH4是还原剂 B、反应Cl2+2NaOH=NaCl+NaClO+H2O中,Cl2是氧化剂,NaOH是还原剂 C、反应MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O中,HCl是氧化剂,MnO2是还原剂 D、反应2Na+2H2O=2NaOH+H2↑中,H2O既是氧化剂又是还原剂20. 检验溶液中是否含有某种离子,下列操作方法正确的是 ( )A、向某溶液中加AgNO3溶液产生白色沉淀,证明有Cl- B、向某溶液中加稀 HCl,无明显现象,再加入BaCl2 溶液产生白色沉淀,证明有SO42- C、向某溶液中加入稀 HCl,放出能使澄清的石灰水变浑浊的气体,证明有CO32- D、向某溶液中加入浓氢氧化钠溶液后加热,产生使湿润蓝色石蕊试纸变红的气体,证明含有NH4+21.(1)、绿色植物是空气天然的“净化器”,在家里科学选种一些绿色植物,可以达到净化空气、吸收有害物质的作用。科学研究发现,1公顷柳杉每月可以吸收160 kg SO2 , 则1公顷柳杉每月吸收的SO2的物质的量为。(2)、铅笔芯的主要成分是石墨和黏土,这些物质按照不同的比例加以混合、压制,就可以制成不同型号的铅笔芯。如果某铅笔芯质量的一半成分是石墨,且用铅笔写一个字消耗的质量约为1 mg。那么一个铅笔字含有的碳原子数约为。(3)、吸食“摇头丸”会严重破坏人体的中枢神经,“摇头丸”的化学式为C9H13N,请计算:①“摇头丸”的摩尔质量为;
②某毒枭被查获带有270 g“摇头丸”,该毒枭所带的“摇头丸”的物质的量为。
(4)、将14.3 g Na2CO3·10H2O固体溶于水配成250 mL溶液,则所得溶液物质的量浓度是。22. 化学实验是化学学习的重要内容。根据你掌握的知识,完成下面内容。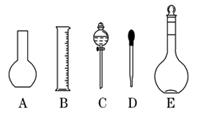 (1)、实验室需要0.1 mol/L NaOH溶液480 mL, 根据溶液的配制情况回答下列问题:
(1)、实验室需要0.1 mol/L NaOH溶液480 mL, 根据溶液的配制情况回答下列问题:①如图所示的仪器中配制溶液肯定不需要的是(填序号);
②由计算得知,应选择mL的容量瓶,
用托盘天平称取g NaOH。
③在配制NaOH溶液实验中,其他操作均正确。
若定容时仰视刻度线, 则所配制溶液浓度0.1 mol/L
(填“大于”“等于”或“小于”,下同);溶解NaOH后的溶液需冷却到室温后方能转移入容量瓶中。若趁热转移会使所配制溶液浓度0.1 mol/L。
(2)、选择下列实验方法分离物质,将分离方法的序号填在横线上。萃取分液 升华 蒸发结晶 过滤 蒸馏 分液
除去洗菜水里的菜叶子和泥土;
从食盐水里获得食盐固体;
从碘和沙子混合物中获得碘;
从溴水中获得溴;
分离 沸点为 和甲苯沸点为 的混合物。
23. 实验题:(1)、实验一如图所示为实验室制取蒸馏水的装置示意图。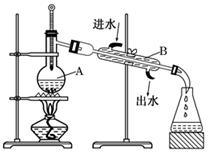
根据图示回答下列问题:
图中两处明显错误是:
①;
②。
(2)、A仪器的名称是 ,B仪器的名称是。
(3)、实验时,A中除加入少量自来水外,还需要加入少量的 , 其作用是。
(4)、实验二:碘是人体不可缺乏的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4 , 该小组先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和KI溶液,转移到分液漏斗中,再加入一定量的苯,振荡。
分液漏斗使用前应先 , 振荡后上层液体为(填有机层、水层)。
(5)、萃取碘水中的I2单质时要用到萃取剂,下列关于所加萃取剂的说法正确的是(______)A、不与碘反应 B、碘在其中的溶解度远大于在水中的溶解度 C、该萃取剂与水不互溶且密度比水大 D、可以选用CCl4、酒精做萃取剂.(6)、某学生在一次分液操作中发现上下层溶液都是无色液体,无法知道分液漏斗中的液体哪一层是有机层,哪一层是水层,请你用简单的方法帮他鉴别出来,写出有关步骤及判断方法24. 在实验室里,用足量的浓盐酸与一定量的高锰酸钾反应(不加热),来制取氯气。反应:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
(1)、“双线桥法”标出电子转移情况 。(2)、若生成2.24L标准状况时的氯气,请计算(写出必要的计算过程):①论上需要多少克KMnO4参加反应?
②被氧化的HCl的物质的量为多少?