2017年广西来宾市中考化学试卷
试卷更新日期:2017-07-17 类型:中考真卷
一、选择题
-
1. 某成年人长期不吃瘦肉、鱼、蛋等食物,结果出现脸色苍白、头晕等症状.该成年人缺少的营养素最可能是( )A、糖类 B、油脂 C、无机盐 D、蛋白质2. 下列物质属于化石燃料的是( )A、煤 B、酒精 C、木材 D、一氧化碳3. ①水的沸腾②胆矾研碎③铁丝燃烧④食物腐败等四个变化”中,属于化学变化的是( )A、①② B、①③ C、②③ D、③④4. 为了减少空气污染,下列措施不正确的是( )A、使用清洁能源 B、加强大气质量监测 C、积极植树造林 D、加高烟囱将工厂废气排放到大气中5. 下列图标与燃烧、爆炸无关的是( )A、

 B、
B、
 C、
C、
 D、
D、
 6. 下列仪器与其用途的对应关系,正确的是( )A、量筒﹣﹣配制溶液 B、烧杯﹣﹣贮存气体 C、长颈漏斗﹣﹣过滤 D、胶头滴管﹣﹣滴加少量液体7. 下列各种粒子,带负电荷的是( )A、电子 B、中子 C、质子 D、原子核8. 20℃时氯化钾的溶解度为34g.下列是四位同学在20℃时配制的氯化钾溶液,其中一定达到饱和的是( )A、
6. 下列仪器与其用途的对应关系,正确的是( )A、量筒﹣﹣配制溶液 B、烧杯﹣﹣贮存气体 C、长颈漏斗﹣﹣过滤 D、胶头滴管﹣﹣滴加少量液体7. 下列各种粒子,带负电荷的是( )A、电子 B、中子 C、质子 D、原子核8. 20℃时氯化钾的溶解度为34g.下列是四位同学在20℃时配制的氯化钾溶液,其中一定达到饱和的是( )A、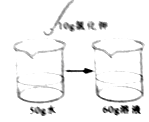
 B、
B、
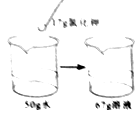 C、
C、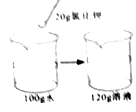
 D、
D、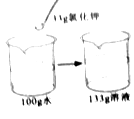
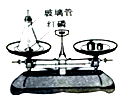
 9. 下列属于人体必需微量元素的是( )A、铁 B、汞 C、镉 D、铅10. 有关氧气的说法,正确的是( )A、氧气可作燃料 B、实验室可用分离液态空气的方法制氧气 C、通常状况下,氧气无色无味、不易溶于水 D、氧气化学性质比较活泼,可跟任何物质反应11. 下列化学方程式书写正确的是( )A、2KClO3=2KCl+3O2 B、H2SO4+Ca(OH)2=CaSO4+H2O C、2Fe+6HCl=2FeCl3+3H2↑ D、Cu(NO3)2+2NaOH=Cu(OH)2↓+2NaNO312. 下列属于氧化物的是( )A、H2O2 B、O3 C、C6H12O6 D、KMnO413. 关于2H2+O2 2H2O的读法不正确的是( )A、氢气与氧气在点燃的条件下生成水 B、每2个氢分子与1个氧分子完全反应,生成2个水分子 C、常温下,每2体积的氧气与l体积的氧气完全反应,生成2体积的水 D、每4份质量的氧气与32份质量的氧气完全反应,生成36份质量的水14. 下列有关金属的叙述,正确的是( )A、钢中含碳量低于生铁中的含碳量 B、合金的硬度比其纯金属的硬度小 C、铝、铁、铜都是银白色金属 D、铝能制成铝箔是因为铝有很好的抗腐蚀性15. 分别向甲、乙、丙三种无色溶液中滴加紫色石蕊试液、观察到甲溶液变红色,乙溶液变蓝色,丙溶液变紫色.则它们的pH由小到大的排列是( )A、甲、乙、丙 B、甲、丙、乙 C、乙、甲、丙 D、丙、甲、乙16. 关于分子、原子、离子的说法,正确的是( )A、分子的质量一定比原子大 B、原子是不能再分的粒子 C、原子得失电子后形成离子 D、分子、原子能构成物质,离子不能17. 关于金刚石、石墨、C60的叙述,正确的是( )A、都属于碳单质 B、都由碳原子构成 C、都具有导电性 D、完全燃烧产物不同18. 下列实验现象的描述,正确的是( )A、硫在空气中燃烧,产生明亮的蓝紫色火焰 B、打开浓盐酸的试剂瓶,瓶口会出现白雾 C、一氧化碳还原氧化铁,固体由黑色变红色 D、把铁钉放入硫酸铜溶液中,有铜析出19. 在粗盐难溶性杂质去除实验中,操作错误的是( )A、称量时,在托盘天平左右两盘垫上相同质量的纸片 B、溶解时,用玻璃棒搅拌加快粗盐溶解 C、过滤时,用玻璃棒搅拌漏斗内的液体加快过滤 D、蒸发时,当蒸发皿中出现较多固体时停止加热20. 乙醇在一定条件下可氧化为乙醛:2CH3CH2OH+O2 2CH3CHO(乙醛)+2H2O.实际是发生了如下两个反应:反应一:2Cu+O2 2CuO,反应二:CH3CH2OH+CuO CH3CHO+H2O+Cu.下列说法错误的是( )A、Cu在反应一中是反应物 B、Cu在反应前后化学性质改变 C、Cu在反应二中是生成物 D、Cu在反应中起到催化作用21. 下列实验能够用于直接验证质量守恒定律的是( )A、
9. 下列属于人体必需微量元素的是( )A、铁 B、汞 C、镉 D、铅10. 有关氧气的说法,正确的是( )A、氧气可作燃料 B、实验室可用分离液态空气的方法制氧气 C、通常状况下,氧气无色无味、不易溶于水 D、氧气化学性质比较活泼,可跟任何物质反应11. 下列化学方程式书写正确的是( )A、2KClO3=2KCl+3O2 B、H2SO4+Ca(OH)2=CaSO4+H2O C、2Fe+6HCl=2FeCl3+3H2↑ D、Cu(NO3)2+2NaOH=Cu(OH)2↓+2NaNO312. 下列属于氧化物的是( )A、H2O2 B、O3 C、C6H12O6 D、KMnO413. 关于2H2+O2 2H2O的读法不正确的是( )A、氢气与氧气在点燃的条件下生成水 B、每2个氢分子与1个氧分子完全反应,生成2个水分子 C、常温下,每2体积的氧气与l体积的氧气完全反应,生成2体积的水 D、每4份质量的氧气与32份质量的氧气完全反应,生成36份质量的水14. 下列有关金属的叙述,正确的是( )A、钢中含碳量低于生铁中的含碳量 B、合金的硬度比其纯金属的硬度小 C、铝、铁、铜都是银白色金属 D、铝能制成铝箔是因为铝有很好的抗腐蚀性15. 分别向甲、乙、丙三种无色溶液中滴加紫色石蕊试液、观察到甲溶液变红色,乙溶液变蓝色,丙溶液变紫色.则它们的pH由小到大的排列是( )A、甲、乙、丙 B、甲、丙、乙 C、乙、甲、丙 D、丙、甲、乙16. 关于分子、原子、离子的说法,正确的是( )A、分子的质量一定比原子大 B、原子是不能再分的粒子 C、原子得失电子后形成离子 D、分子、原子能构成物质,离子不能17. 关于金刚石、石墨、C60的叙述,正确的是( )A、都属于碳单质 B、都由碳原子构成 C、都具有导电性 D、完全燃烧产物不同18. 下列实验现象的描述,正确的是( )A、硫在空气中燃烧,产生明亮的蓝紫色火焰 B、打开浓盐酸的试剂瓶,瓶口会出现白雾 C、一氧化碳还原氧化铁,固体由黑色变红色 D、把铁钉放入硫酸铜溶液中,有铜析出19. 在粗盐难溶性杂质去除实验中,操作错误的是( )A、称量时,在托盘天平左右两盘垫上相同质量的纸片 B、溶解时,用玻璃棒搅拌加快粗盐溶解 C、过滤时,用玻璃棒搅拌漏斗内的液体加快过滤 D、蒸发时,当蒸发皿中出现较多固体时停止加热20. 乙醇在一定条件下可氧化为乙醛:2CH3CH2OH+O2 2CH3CHO(乙醛)+2H2O.实际是发生了如下两个反应:反应一:2Cu+O2 2CuO,反应二:CH3CH2OH+CuO CH3CHO+H2O+Cu.下列说法错误的是( )A、Cu在反应一中是反应物 B、Cu在反应前后化学性质改变 C、Cu在反应二中是生成物 D、Cu在反应中起到催化作用21. 下列实验能够用于直接验证质量守恒定律的是( )A、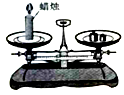
 B、
B、
 C、
C、
 D、
D、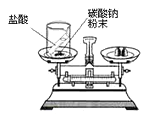
 22. 下列物质的用途,正确的是( )A、食盐可作发酵粉 B、石灰石可作建筑材料 C、碳酸氢钠可制玻璃 D、氢氧化钠可改良酸性土壤23. 为了探究镁、锌、铜三种金属的活动性强弱,将形状、大小相同的三种金属分别放入装有X溶液的试管中,通过观察现象即能得出实验结论.则X溶液是( )A、稀硫酸 B、硝酸银溶液 C、氯化铜溶液 D、氯化镁溶液24. 下列各组物质鉴别方案的描述,正确的是( )A、H2、CO、CH4三种气体,直接点燃气体就能够鉴别 B、Fe2O3、CuO、Zn、Cu四种固体,加一种试剂无法鉴别 C、MgCl2、KOH、HCl、Na2SO4四种溶液,不加任何试剂就可以鉴别 D、NaOH、KOH、NaCl、H2SO4四种溶液,加入酚酞溶液就可以鉴别25.
22. 下列物质的用途,正确的是( )A、食盐可作发酵粉 B、石灰石可作建筑材料 C、碳酸氢钠可制玻璃 D、氢氧化钠可改良酸性土壤23. 为了探究镁、锌、铜三种金属的活动性强弱,将形状、大小相同的三种金属分别放入装有X溶液的试管中,通过观察现象即能得出实验结论.则X溶液是( )A、稀硫酸 B、硝酸银溶液 C、氯化铜溶液 D、氯化镁溶液24. 下列各组物质鉴别方案的描述,正确的是( )A、H2、CO、CH4三种气体,直接点燃气体就能够鉴别 B、Fe2O3、CuO、Zn、Cu四种固体,加一种试剂无法鉴别 C、MgCl2、KOH、HCl、Na2SO4四种溶液,不加任何试剂就可以鉴别 D、NaOH、KOH、NaCl、H2SO4四种溶液,加入酚酞溶液就可以鉴别25.现有盐酸和CaCl2的混合溶液,向其中逐滴滴入Na2CO3溶液,生成沉淀质量与滴入Na2CO3溶液质量的变化关系如右图所示.下列说法正确的是( )
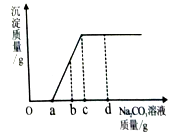
 A、滴至a克时,溶液中反应为CaCl2+Na2CO3=2NaCl+CaCO3↓ B、滴至b克时,溶液中含HCl、NaCl两种溶质 C、滴至c克时,溶液中溶质质量比原混合溶液中溶质质量大 D、滴至d克时,溶液呈中性
A、滴至a克时,溶液中反应为CaCl2+Na2CO3=2NaCl+CaCO3↓ B、滴至b克时,溶液中含HCl、NaCl两种溶质 C、滴至c克时,溶液中溶质质量比原混合溶液中溶质质量大 D、滴至d克时,溶液呈中性二、填空题
-
26. 请完成以下填空:
镁是由构成;CO2中“2”表示的意义是;由N、H、Cl三种元素组成的一种盐的化学式是
27. 化学与我们的生活息息相关.①小琼买了纯棉毛巾、真丝围巾、羊毛衫、塑料拖鞋等物品,这些物品中属于合成材料制品的是;小琼还买了一瓶矿泉水,标签上注明的主要矿物成分及含量(单位mg/L):Ca﹣20、K﹣3、Zn﹣0.06、F﹣0.02等,这里的Ca、K、Zn、F是指 .
②从分子的角度分析,做饭时闻到饭菜的香味,是因为;油锅着火了,用锅盖盖灭,其原理是 .
28.如图是水的电解实验装置图,请回答下列问题:
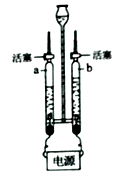
①该反应是将电能转化能.
②检验b管内气体的方法是 .
③若a管收集到8mL气体,则在相同条件下b管应收集到的气体是 mL.
 29.
29.根据如图图示回答下列问题:
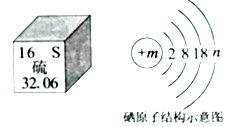

①从图中不能直接获取的信息是 .
A.硫属于非金属元素 B.硫的核外电子数为16
C.硫的相对原子质量为32.06 D.硫元素形成的单质有还原性
②根据硫原子的最外层电子数,推出硫元素的最低化合价为﹣2价,则硫元素的最高化合价为价.
③元素周期表中同一主族的元素具有相似的化学性质,例如硒(Se)和S有相似的化学性质,则图中m= .
30.如图是X、Y两种固体物质的溶解度曲线图.请据图回答:
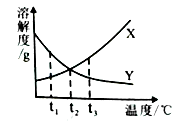
①t3℃时,将澄清的饱和溶液X、Y降温到t2℃,有固体析出的是溶液.
②Y溶液的溶质可能是(填序号).
A.NaCl B.KNO3 C.Ca(OH)2
③t3℃时,保持温度不变,将X、Y饱和溶液蒸发一定量的水,则蒸发水后两溶液的溶质质量分数XY(填“>”、“<”或“=”).

三、简答题
-
31.
空气中氧气含量的测定如图所示:
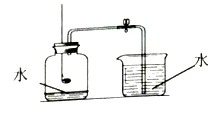
 (1)、燃烧匙内盛放的药品是 .(2)、集气瓶内水面上升不到 的原因可能是(答一条即可).32. 自来水厂的生活用水常用氯气来杀菌消毒.氯气是一种黄绿色有刺激性气味的气体,把氯气通入水中生成两种酸,其中一种酸有强氧化性,可杀菌消毒,该酸性质不稳定,见光分解产产生O2 .(1)、根据上述信息写出氯气的一种物理性质: .(2)、Cl2+H2O=HCl+X,X的化学式为 .33.
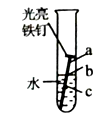
(1)、燃烧匙内盛放的药品是 .(2)、集气瓶内水面上升不到 的原因可能是(答一条即可).32. 自来水厂的生活用水常用氯气来杀菌消毒.氯气是一种黄绿色有刺激性气味的气体,把氯气通入水中生成两种酸,其中一种酸有强氧化性,可杀菌消毒,该酸性质不稳定,见光分解产产生O2 .(1)、根据上述信息写出氯气的一种物理性质: .(2)、Cl2+H2O=HCl+X,X的化学式为 .33.如图所示,铁钉最容易生锈的是处(填“a”、“b”或“c”),常用稀硫酸除去铁锈,写出该反应的化学方程式: .
 34. 某pH=13的溶液中可能含有Cu2+、Na+、SO42﹣、CO32﹣、NO3﹣等离子中的一种或几种,为了检验该溶液中含有的离子,进行如下实验并分析:(1)、该溶液pH=13,证明不存在的离子是 .(2)、取少量该溶液于试管中,滴加适最BaCl2溶液,产生白色沉淀,再加入过量的稀盐酸,沉淀部分溶解.写出沉淀溶解的化学方程式: .(3)、该溶液中一定存在的离子是 , 可能存在的离子是 .
34. 某pH=13的溶液中可能含有Cu2+、Na+、SO42﹣、CO32﹣、NO3﹣等离子中的一种或几种,为了检验该溶液中含有的离子,进行如下实验并分析:(1)、该溶液pH=13,证明不存在的离子是 .(2)、取少量该溶液于试管中,滴加适最BaCl2溶液,产生白色沉淀,再加入过量的稀盐酸,沉淀部分溶解.写出沉淀溶解的化学方程式: .(3)、该溶液中一定存在的离子是 , 可能存在的离子是 .四、实验探究题
-
35.
如图是实验室制取纯净、干燥的二氧化碳气体,并探究其某些性质的实验装置.据图回答下列问题:
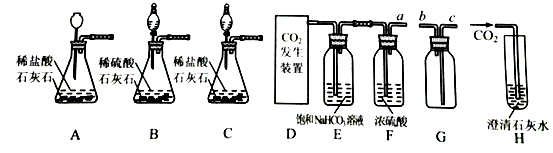
 (1)、D处应连接装置(填“A”、“B”或“C”).(2)、E装置的作用是;用G装置收集二氧化碳气体,a端应连接G装置端(填“b”或“c”).(3)、写出H装置中发生反应的化学方程式: .36.
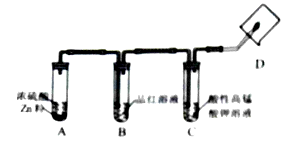
(1)、D处应连接装置(填“A”、“B”或“C”).(2)、E装置的作用是;用G装置收集二氧化碳气体,a端应连接G装置端(填“b”或“c”).(3)、写出H装置中发生反应的化学方程式: .36.某兴趣小组做了锌粒与稀硫酸反应的实验后,用浓硫酸代替稀硫酸与锌粒进行实验,有刺激性气味气体产生.为了验证该气体的成分,该小组通过查阅资料得知:浓硫酸有强氧化性,能与多种物质反应;SO2能使品红溶液褪色,可被酸性KMnO4吸收.并进行如下实验:
 (1)、实验事实与结论:
(1)、实验事实与结论:①反应进行不久,观察到B处 , D处无明显现象,证明产生的气体是SO2 . 写出有关反应的化学方程式 .
②反应继续进行一段时间后,D处气体能燃烧,干燥烧杯内壁有水雾,证明产生的气体是H2 , 产生该气体的原因是 .
(2)、反思与评价:小明认为,工业上可用锌粒和浓硫酸反应大量制取硫酸锌溶液.小红认为不适宜,她的理由是
五、计算题
-
37.
取MgCl2和NaCl的固体混合物10g做如下实验.请根据图中实验及数据进行计算.
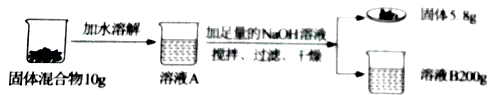
 (1)、MgCl2中镁元素和氯元素的质量比为(2)、计算溶液B中NaCl的质量分数(写出计算过程).(3)、要配制与溶液B相同质量分数的NaCl溶液200g,需要质量分数为24.4%的NaCl溶液的质量是多少?(写出计算过程)
(1)、MgCl2中镁元素和氯元素的质量比为(2)、计算溶液B中NaCl的质量分数(写出计算过程).(3)、要配制与溶液B相同质量分数的NaCl溶液200g,需要质量分数为24.4%的NaCl溶液的质量是多少?(写出计算过程)