专题24:烷烃、烯烃、炔烃
试卷更新日期:2019-11-06 类型:一轮复习
一、单选题
-
1. 下列说法中错误的是( )A、烷烃的通式是CnH2n+2 , 所以符合此通式的烃一定是烷烃 B、碳原子数相同的烯烃和烷烃是同分异构体 C、烯烃中碳的质量分数一定大于烷烃中碳的质量分数 D、烯烃易发生加成反应,烷烃能发生取代反应2. 利用下列反应不能制得括号中纯净物质的是( )A、乙烯与氯气加成(1,2 二氯乙烷) B、氯气与苯用氯化铁作催化剂反应(氯苯) C、等物质的量的氯气与乙烷在光照条件下反应(氯乙烷) D、乙烯与水加成(乙醇)3. 有关烷烃的叙述:①大都是易燃物;②特征反应是取代反应;③相邻两个烷烃在分子组成上相差一个甲基,其中正确的是( )A、①和③ B、②和③ C、只有① D、①和②4. 下列物质中,能通过化学反应使溴的四氯化碳溶液褪色的是()A、CH4 B、CH2=CH2 C、CH3CH2OH D、苯5. 下列实验现象与实验操作不相匹配的是( )
实验操作
实验现象
A
向盛有高锰酸钾酸性溶液的试管中通入足量的乙烯后静置
溶液的紫色逐渐褪去,静置后溶液分层
B
将镁条点燃后迅速伸入集满 的集气瓶
集气瓶中产生浓烟并有黑色颗粒产生
C
向盛有饱和硫代硫酸钠溶液的试管中滴加稀盐酸
有刺激性气味气体产生,溶液变浑浊
D
向盛有 溶液的试管中加过量铁粉,充分振荡后加1滴KSCN溶液
黄色逐渐消失,加KSCN后溶液颜色不变
A、A B、B C、C D、D6. 欲制取较纯净的1,2-二氯乙烷,可采取的方法是( )A、乙烯与HCl加成 B、乙烯与Cl2加成 C、乙烷与Cl2按1:2的体积比在光照条件下反应 D、乙烯先与HCl加成,再与等物质的量的Cl2在光照下反应7. 下列关于乙烯与苯的说法正确的是( )A、分子中均含有碳碳双键 B、常温常压下,它们均呈气态 C、都能使酸性KMnO4溶液褪色 D、分子中所有原子均处于同一平面8. 实验室制取乙烯的发生装置如图所示。下列说法正确的是() A、烧瓶中加入乙醇、浓硫酸和碎瓷片 B、反应温度控制在140℃ C、导出的气体能使溴水褪色,可以证明反应生成乙烯 D、可用向上排气法收集乙烯9. 催化加氢可生成2-甲基戊烷的是( )A、CH2=CHC(CH3)2CH2CH3 B、CH2=CHCH(CH3)C≡CH C、(CH3)2C=C(CH3)2 D、(CH3)2CHCH2C≡CH10. 下列关于乙烷、乙烯、乙炔的说法正确的是( )
A、烧瓶中加入乙醇、浓硫酸和碎瓷片 B、反应温度控制在140℃ C、导出的气体能使溴水褪色,可以证明反应生成乙烯 D、可用向上排气法收集乙烯9. 催化加氢可生成2-甲基戊烷的是( )A、CH2=CHC(CH3)2CH2CH3 B、CH2=CHCH(CH3)C≡CH C、(CH3)2C=C(CH3)2 D、(CH3)2CHCH2C≡CH10. 下列关于乙烷、乙烯、乙炔的说法正确的是( )①它们既不是同系物,也不是同分异构体
②乙烷是饱和烃,乙烯、乙炔是不饱和烃
③乙烯、乙炔能使溴水褪色,乙烷不能使溴水褪色
④它们都能燃烧,乙炔燃烧火焰最明亮,有浓烟
⑤它们都能使酸性KMnO4溶液褪色
A、①③④ B、①②③⑤ C、②③④⑤ D、①②③④11. 下列实验操作或装置能达到目的的是( )A
B
C
D
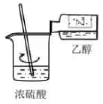
混合浓硫酸和乙醇
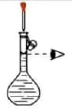
配制一定浓度的溶液
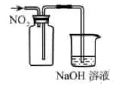
收集 气体
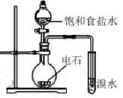
证明乙炔可使溴水褪色
A、A B、B C、C D、D12. 与H2反应生成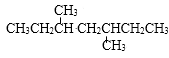 的单炔烃有( ) A、1种 B、2种 C、4种 D、8种13. 0.5mol 气态烃A 最多和1 mol HCl加成,生成氯代烷B,1mol B与4 mol Cl2 发生取代反应,生成只含碳、氯两种元素的化合物C,则A的分子式为( )A、C2H4 B、C2H2 C、C3H4 D、C4H614. 交联聚合物P的结构片段如图所示。下列说法不正确的是(图中
的单炔烃有( ) A、1种 B、2种 C、4种 D、8种13. 0.5mol 气态烃A 最多和1 mol HCl加成,生成氯代烷B,1mol B与4 mol Cl2 发生取代反应,生成只含碳、氯两种元素的化合物C,则A的分子式为( )A、C2H4 B、C2H2 C、C3H4 D、C4H614. 交联聚合物P的结构片段如图所示。下列说法不正确的是(图中 表示链延长)( )
表示链延长)( )  A、聚合物P中有酯基,能水解 B、聚合物P的合成反应为缩聚反应 C、聚合物P的原料之一丙三醇可由油脂水解获得 D、邻苯二甲酸和乙二醇在聚合过程中也可形成类似聚合物P的交联结构15. 对
A、聚合物P中有酯基,能水解 B、聚合物P的合成反应为缩聚反应 C、聚合物P的原料之一丙三醇可由油脂水解获得 D、邻苯二甲酸和乙二醇在聚合过程中也可形成类似聚合物P的交联结构15. 对 认识正确的是( ) A、名称为3-甲基丁烷 B、所有碳原子在同一平面上 C、难溶于水 D、不能发生分解、加成、消去反应16. 下列化合物中,能发生氧化、还原、加成、消去四种反应的是()A、
认识正确的是( ) A、名称为3-甲基丁烷 B、所有碳原子在同一平面上 C、难溶于水 D、不能发生分解、加成、消去反应16. 下列化合物中,能发生氧化、还原、加成、消去四种反应的是()A、 B、
B、 C、CH3CH2CH2CHO
D、
C、CH3CH2CH2CHO
D、
二、实验探究题
-
17.(1)、某同学将等体积的甲烷与氯气混合于一试管中,倒扣在盛饱和食盐水的水槽里,然后置于光亮处。一段时间后的现象正确的是:;
 (2)、反应后试管中所得有机产物化学式为;(有几种写几种)(3)、写出甲烷与氯气反应第一步的化学方程式;(4)、在同温同压下,甲烷的同系物A的蒸汽密度是甲烷密度的4.5倍,其分子式__;(5)、A有种同分异构体;写出其有三个甲基的同分异构体的结构简式;(6)、A的某同分异构体只有一种一氯代物,请用系统命名法为该同分异构体命名。18. 环己烯是重要的化工原料。其实验室制备流程如下:
(2)、反应后试管中所得有机产物化学式为;(有几种写几种)(3)、写出甲烷与氯气反应第一步的化学方程式;(4)、在同温同压下,甲烷的同系物A的蒸汽密度是甲烷密度的4.5倍,其分子式__;(5)、A有种同分异构体;写出其有三个甲基的同分异构体的结构简式;(6)、A的某同分异构体只有一种一氯代物,请用系统命名法为该同分异构体命名。18. 环己烯是重要的化工原料。其实验室制备流程如下: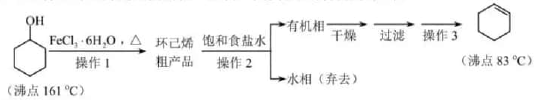
回答下列问题:
(1)、Ⅰ.环己烯的制备与提纯原料环己醇中若含苯酚杂质,检验试剂为 , 现象为。
(2)、操作1的装置如图所示(加热和夹持装置已略去)。
①烧瓶A中进行的可逆反应化学方程式为 , 浓硫酸也可作该反应的催化剂,选择 而不用浓硫酸的原因为(填序号)。
a.浓硫酸易使原料碳化并产生
b. 污染小、可循环使用,符合绿色化学理念
c.同等条件下,用 比浓硫酸的平衡转化率高
②仪器B的作用为。
(3)、操作2用到的玻璃仪器是。(4)、将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石, , 弃去前馏分,收集83℃的馏分。(5)、Ⅱ.环己烯含量的测定在一定条件下,向 环己烯样品中加入定量制得的 ,与环己烯充分反应后,剩余的 与足量 作用生成 ,用 的 标准溶液滴定,终点时消耗 标准溶液 (以上数据均已扣除干扰因素)。
测定过程中,发生的反应如下:
①

②
③
滴定所用指示剂为。样品中环己烯的质量分数为(用字母表示)。
(6)、下列情况会导致测定结果偏低的是(填序号)。a.样品中含有苯酚杂质
b.在测定过程中部分环己烯挥发
c. 标准溶液部分被氧化
19. 某同学设计实验探究工业制乙烯的原理和乙烯的主要化学性质,实验装置如图所示(已知烃类都不与碱反应)。请回答下列问题 (1)、工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。例如,石油分馏产物之一的十六烷烃发生反应:C16H34 C8H18+甲,甲 △4乙,则甲的分子式为 , 乙的结构简式为。(2)、B装置中的实验现象可能是 ,写出反应的化学方程式: , 其反应类型是。(3)、C装置中可观察到的现象是 , 反应类型是。(4)、查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置 (填字母)中的实验现象可判断该资料是否真实。为了探究溴与乙烯反应是加成反应而不是取代反应,可以测定装置B中溶液在反应前后的酸碱性,简述其理由: 。(5)、通过上述实验探究,检验甲烷和乙烯的方法是(选填字母,下同);除去甲烷中乙烯的方法是 。
(1)、工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。例如,石油分馏产物之一的十六烷烃发生反应:C16H34 C8H18+甲,甲 △4乙,则甲的分子式为 , 乙的结构简式为。(2)、B装置中的实验现象可能是 ,写出反应的化学方程式: , 其反应类型是。(3)、C装置中可观察到的现象是 , 反应类型是。(4)、查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置 (填字母)中的实验现象可判断该资料是否真实。为了探究溴与乙烯反应是加成反应而不是取代反应,可以测定装置B中溶液在反应前后的酸碱性,简述其理由: 。(5)、通过上述实验探究,检验甲烷和乙烯的方法是(选填字母,下同);除去甲烷中乙烯的方法是 。A.气体通入水中
B.气体通过盛溴水的洗气瓶
C.气体通过盛酸性高锰酸钾溶液的洗气瓶
D.气体通过氢氧化钠溶液
(6)、分别燃烧乙烯和甲烷,甲烷火焰明亮而乙烯产生少量黑烟,原因是 。20. 实验室常用乙醇与浓硫酸的混合液加热的方法制取乙烯。反应中常因温度而发生副反应。请选用下列装置(装置可以使用多次)完成相关实验并回答有关问题: (1)、制备乙烯时,常在A装置的烧瓶中加入碎瓷片,其目的是;加热时要使溶液的温度迅速上升到140℃以上,因为在140℃左右易生成乙醚,该有机物的结构简式为;生成乙烯的化学方程式为。(2)、乙醇与浓硫酸加热制取乙烯时,乙烯气体中常混有SO2和CO2 , 为验证有副产物SO2和CO2气体存在,上述仪器的连接顺序为a→。(3)、某同学设计制备1,2-二溴乙烷的装置连接顺序为A→E→C→D。已知1,2-二溴乙烷的主要物理性质有:难溶于水、熔点9℃、沸点132℃、密度2.2g·cm-3。
(1)、制备乙烯时,常在A装置的烧瓶中加入碎瓷片,其目的是;加热时要使溶液的温度迅速上升到140℃以上,因为在140℃左右易生成乙醚,该有机物的结构简式为;生成乙烯的化学方程式为。(2)、乙醇与浓硫酸加热制取乙烯时,乙烯气体中常混有SO2和CO2 , 为验证有副产物SO2和CO2气体存在,上述仪器的连接顺序为a→。(3)、某同学设计制备1,2-二溴乙烷的装置连接顺序为A→E→C→D。已知1,2-二溴乙烷的主要物理性质有:难溶于水、熔点9℃、沸点132℃、密度2.2g·cm-3。①E装置的作用。
②分离D装置中1,2-二溴乙烷的操作方法是加入试剂 , 充分反应后进行操作。
③反应过程中,应将D装置放在10℃的水浴中,温度不宜过低、过高的原因是。
三、综合题
-
21. 按要求写出下列反应方程式(请注明反应条件),并按要求填空(1)、实验室制备乙烯 , 反应类型是 .(2)、乙酸与乙醇的反应 , 反应的无机产物中氧元素的来源是。(3)、溴乙烷与氢氧化钠水溶液共热 , 此反应将卤代烃类物质转化为类物质.(4)、苯与浓硫酸、浓硝酸的混合酸在加热时发生反应 , 反应类型是 .22. 煤的综合利用备受关注。有如下的转化关系,CO与H2不同比例可以分别合成A、B,已知烃A对氢气的相对密度是14,B能发生银镜反应,C为常见的酸味剂。
 (1)、有机物C中含有的官能团的名称是。(2)、反应⑤的反应类型为。(3)、写出③的反应方程式 。(4)、下列说法正确的是______________。(填字母)A、第①步是煤的液化,为煤的综合利用的一种方法 B、有机物B和C都可以与新制氢氧化铜发生反应 C、有机物C和D的水溶液都具有杀菌消毒作用 D、乙酸乙酯与有机物D混合物的分离,可以用氢氧化钠溶液振荡、静置分液的方法23. 下图中A、B、C、D、E、F、G均为有机化合物。
(1)、有机物C中含有的官能团的名称是。(2)、反应⑤的反应类型为。(3)、写出③的反应方程式 。(4)、下列说法正确的是______________。(填字母)A、第①步是煤的液化,为煤的综合利用的一种方法 B、有机物B和C都可以与新制氢氧化铜发生反应 C、有机物C和D的水溶液都具有杀菌消毒作用 D、乙酸乙酯与有机物D混合物的分离,可以用氢氧化钠溶液振荡、静置分液的方法23. 下图中A、B、C、D、E、F、G均为有机化合物。
根据上图回答问题:
(1)、D的化学名称是。(2)、反应③的化学方程式是(有机物须用结构简式表示)(3)、B的分子式是。A的结构简式是。反应①的反应类型是。
(4)、符合下列3个条件的B的同分异构体的数目有个。①含有邻二取代苯环结构;②与B有相同官能团;③不与FeCl3溶液发生显色反应。写出其中任意一个同分异构体的结构简式。
(5)、G是重要的工业原料,用化学方程式表示G的一种重要的工业用途24. 以苯和乙炔为原料合成化工原料E的路线如下: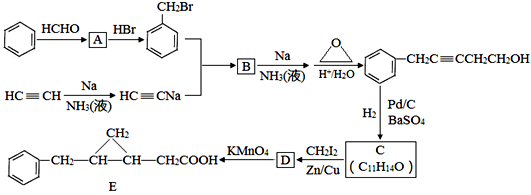
回答下列问题:
(1)、以下有关苯和乙炔的认识正确的是。a.苯和乙炔都能使溴水褪色,前者为化学变化,后者为物理变化
b.苯和乙炔在空气中燃烧都有浓烟产生
c.苯与浓硝酸混合,水浴加热55~60℃,生成硝基苯
d.聚乙炔是一种有导电特性的高分子化合物
(2)、A的名称。(3)、生成B的化学方程式为 , 反应类型是。(4)、C的结构简式为 , C的分子中一定共面的碳原子最多有个。(5)、与D同类别且有二个六元环结构(环与环之间用单键连接)的同分异构体有4种,请写出其中2种同分异构体的结构简式:。(6)、参照上述合成路线,设计一条以乙炔和必要试剂合成环丙烷的路线:。四、推断题
-
25. 烃A标准状况下的密度为1.16 g·L-1 , 以A为原料在一定条件下可获得有机物B、C、D、E、F,其相互转化关系如图。F为有浓郁香味,不易溶于水的油状液体。
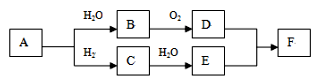
请回答:
(1)、A的结构简式。(2)、D+E→F的反应类型是。(3)、有机物A转化为B的化学方程式是。(4)、下列说法正确的是_________。A、有机物E与金属钠反应比水与金属钠反应要剧烈。 B、有机物E与金属钠反应的产物可以与水反应重新生成E。 C、有机物D,E,F可用饱和Na2CO3溶液鉴别。 D、上述转化关系图中共涉及3次加成反应。