四川省达州市达川区2018-2019学年九年级上学期化学期末考试试卷
试卷更新日期:2019-11-05 类型:期末考试
一、单选题
-
1. 下列变化中,一定属于化学变化的是( )A、爆炸 B、工业制氧 C、木材燃烧 D、汽油挥发2. 下列关于实验现象的描述正确的是( )A、镁条在空气中剧烈反应,发出耀眼的强光,生成白色固体 B、细铁丝在空气中剧烈燃烧,火星四射,放热,生成一种黑色固体 C、水在通电的条件下发生分解反应生成氢气和氧气 D、木炭在空气中燃烧,放热,发出红光,生成二氧化碳3. 如图是某化学反应的微观示意图,其中不同的小球代表不同的原子.

下列说法错误的是()
A、该图说明了化学反应中分子可以再分原子不能再分 B、该图示中共有4种物质 C、该化学反应,前后各元素的化合价均没有变化 D、该化学反应中,反应物分子个数比为1:14. 在高温条件下,A、B两种物质可以发生化学反应生成C和 反应前后分子种类变化的微观示意图如图所示 在这个化学反应中,以下叙述正确的是() A、该反应是化合反应 B、物质B的相对分子质量是16 C、生成C和D的微粒个数比1:1 D、生成C和D的质量比是14:35. “归纳与比较”是化学学习的重要方法,下列有关CO2与CO的知识归纳错误的是( )
A、该反应是化合反应 B、物质B的相对分子质量是16 C、生成C和D的微粒个数比1:1 D、生成C和D的质量比是14:35. “归纳与比较”是化学学习的重要方法,下列有关CO2与CO的知识归纳错误的是( )A
组成
一氧化碳和二氧化碳都是由碳元素和氧元素组成的.
B
性质
都是无色无味的气体;都能溶于水,水溶液显酸性;都能与石灰水反应;都能燃烧等.
C
用途
CO2可用于光合作用、灭火、化工产品的原料和气体肥料,“干冰”可用于人工降雨等;CO可用作气体燃料、冶炼金属的还原剂等.
D
危害
CO2会造成“温室效应”;CO极易与血液中的血红蛋白结合引起中毒
A、A B、B C、C D、D6. 下列实验结论错误的是( )选项
A
B
C
D
实验




实验现象
热水中未燃烧的白磷在通入氧气后燃烧
带火星的木条伸入氧气中复燃
紫色石蕊试液在通入二氧化碳后变红
燃烧的蜡烛由低到高依次熄灭
实验结论
燃烧需要氧气
氧气浓度越大,燃烧越剧烈
使石蕊变红的是二氧化碳
二氧化碳密度比空气大
A、A B、B C、C D、D7. 下列图象能正确反映实验室制取氧气有关量变化的是( )A、 高锰酸钾制氧气时固体剩余物质量与加热时间的关系
B、
高锰酸钾制氧气时固体剩余物质量与加热时间的关系
B、 高锰酸钾制氧气时二氧化锰的质量与反应时间的关系
C、
高锰酸钾制氧气时二氧化锰的质量与反应时间的关系
C、 一定量的双氧水制氧气时氧气质量与反应时间的关系
D、
一定量的双氧水制氧气时氧气质量与反应时间的关系
D、 双氧水制氧气时氧气质量与双氧水用量的关系
双氧水制氧气时氧气质量与双氧水用量的关系
二、填空题
-
8. 用化学用语回答:(1)、氦气;(2)、氧化铁中的铁元素的化合价;(3)、三个镁离子;(4)、二个氢氧根离子。9. 根据下列粒子结构示意图,回答问题。
 (1)、图A,B,C,D四种粒子共表示种元素。(2)、D原子在化学反应中易填(“得到”或“失去”)电子,元素A位于元素周期表的第周期。(3)、如图从A至F中达到相对稳定结构的是。(4)、E粒子带1个单位负电荷,则X。10. 根据所学知识回答下列问题:(1)、金牌中的金是(填“金属”或“非金属”)元素;(2)、“风过泸州带酒香”,请从微观角度解释诗句中的现象;(3)、某有机物在空气中燃烧生成二氧化碳和水,该有机物的组成肯定有、元素。(4)、水通入直流电后可分解,以下图片是水分解过程中微粒变化的部分示意图,请按它们在化学变化过程中出现的顺序排列(用图中的字母表示),写出反应的文字表达式。
(1)、图A,B,C,D四种粒子共表示种元素。(2)、D原子在化学反应中易填(“得到”或“失去”)电子,元素A位于元素周期表的第周期。(3)、如图从A至F中达到相对稳定结构的是。(4)、E粒子带1个单位负电荷,则X。10. 根据所学知识回答下列问题:(1)、金牌中的金是(填“金属”或“非金属”)元素;(2)、“风过泸州带酒香”,请从微观角度解释诗句中的现象;(3)、某有机物在空气中燃烧生成二氧化碳和水,该有机物的组成肯定有、元素。(4)、水通入直流电后可分解,以下图片是水分解过程中微粒变化的部分示意图,请按它们在化学变化过程中出现的顺序排列(用图中的字母表示),写出反应的文字表达式。 11. 室温下,分别向四个装有等质量的水的烧杯中加入NanRO2n﹣1固体,且所加固体的质量由A到D依次减少,充分溶解后如图所示,请回答下列问题。
11. 室温下,分别向四个装有等质量的水的烧杯中加入NanRO2n﹣1固体,且所加固体的质量由A到D依次减少,充分溶解后如图所示,请回答下列问题。 (1)、中盛的一定是饱和溶液;中盛的可能是饱和溶液(以上均填序号);(2)、若对A、B两烧杯进行加热,先变成不饱和溶液的是(填序号);(3)、当将一定量NanRO2n﹣1的饱和溶液变为不饱和溶液时,下列说法错误的是______A、溶质质量分数一定变小 B、溶剂质量可能不变 C、溶液质量一定增大 D、溶质质量可能不变(4)、化合物NanRO2n﹣1中R元素的化合价为。12. 我国2016年纪念“世界水日”和“中国水周”活动的宣传主题为“落实五大发展理念,推进最严格水资源管理”,请回答下列与水有关的问题:(1)、通过电解水的实验,得出了水的组成,电解水的化学方程式为 .(2)、爱护水资源,人人有责.你认为下列做法不利于防治水体污染的是______.A、依照法规加强水资源的监测和管理 B、生活污水任意排放 C、合理使用化肥和农药 D、工业废水处理达标后排放(3)、洗碗时,用洗涤剂清洗油污是利用洗涤剂的作用.(4)、在生活中,当水的硬度大或者病菌过多,可以采取的方法降低水的硬度和杀灭病菌,ClO2是一种饮用水消毒剂,其生产的化学方程式为 2NaClO2+X═2ClO2+2NaCl,据此式可以推断出X的化学式为 .
(1)、中盛的一定是饱和溶液;中盛的可能是饱和溶液(以上均填序号);(2)、若对A、B两烧杯进行加热,先变成不饱和溶液的是(填序号);(3)、当将一定量NanRO2n﹣1的饱和溶液变为不饱和溶液时,下列说法错误的是______A、溶质质量分数一定变小 B、溶剂质量可能不变 C、溶液质量一定增大 D、溶质质量可能不变(4)、化合物NanRO2n﹣1中R元素的化合价为。12. 我国2016年纪念“世界水日”和“中国水周”活动的宣传主题为“落实五大发展理念,推进最严格水资源管理”,请回答下列与水有关的问题:(1)、通过电解水的实验,得出了水的组成,电解水的化学方程式为 .(2)、爱护水资源,人人有责.你认为下列做法不利于防治水体污染的是______.A、依照法规加强水资源的监测和管理 B、生活污水任意排放 C、合理使用化肥和农药 D、工业废水处理达标后排放(3)、洗碗时,用洗涤剂清洗油污是利用洗涤剂的作用.(4)、在生活中,当水的硬度大或者病菌过多,可以采取的方法降低水的硬度和杀灭病菌,ClO2是一种饮用水消毒剂,其生产的化学方程式为 2NaClO2+X═2ClO2+2NaCl,据此式可以推断出X的化学式为 .三、推断题
-
13. 已知A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,B为氧化物;D、E、F三种物质含有同种非金属元素,其中F是单质,E是易与血液中血红蛋白结合的有毒气体。它们之间的转化关系如图所示(有些转换关系,反应条件等略去)。试回答:
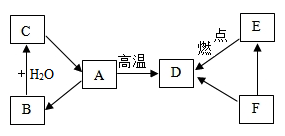 (1)、写出F的化学式:;(2)、写出D物质的一种用途。(3)、用化学方程式表示以下转换关系:A→D , 该反应的反应类型。(4)、E→D反应过程热量(填“放出”或“吸收”)。
(1)、写出F的化学式:;(2)、写出D物质的一种用途。(3)、用化学方程式表示以下转换关系:A→D , 该反应的反应类型。(4)、E→D反应过程热量(填“放出”或“吸收”)。四、实验题
-
14. 小明要配制100g溶质质量分数为18.5%的氯化钠溶液,如图是他配制该溶液的示意图.
 (1)、图中共有处错误(说明:天平的两个托盘上都垫有纸).(2)、量取所需要的水应选择(选填“10mL”、“50mL”或“100mL”)量筒.(3)、用图示的序号表示配制溶液的操作顺序: .(4)、下列因素会使所配溶液溶质质量分数偏小的是(填序号)
(1)、图中共有处错误(说明:天平的两个托盘上都垫有纸).(2)、量取所需要的水应选择(选填“10mL”、“50mL”或“100mL”)量筒.(3)、用图示的序号表示配制溶液的操作顺序: .(4)、下列因素会使所配溶液溶质质量分数偏小的是(填序号)①药品和砝码放错了盘 ②量取水时仰视量筒刻度 ③所用烧杯内事先残留少量蒸馏水 ④将所配溶液转入试剂瓶时,不慎洒到外面少量.⑤使用粗盐代替氯化钠进行配制.
15. 如图是初中化学常见的仪器和装置,请回答下列问题。 (1)、A装置收集某气体应具备的物理性质是。(2)、实验室制取二氧化碳的反应原理:(用化学方程式表示),你认为CO2能否使干燥的紫色石蕊纸花变红色?(选填“能”或“不能”)若某同学用一定质量分数的盐酸与石灰石反应,将制得的CO2通入到澄清的石灰水中,观察未变浑浊,其原因可能是。(3)、若实验室用大理石和稀盐酸制取和收集一瓶干燥的二氧化碳气体,同时检验二氧化碳,若气流按从左到右方向,用仪器接口字母表示连接顺序为:b→h→i﹣→→→j(选填小写字母)。(4)、实验室常用加热氯化铵和氢氧化钙的固体混合物来制取氨气,应选用的发生装置是(填字母)。16. 实验室常用如图装置测定空气中氧气的含量。
(1)、A装置收集某气体应具备的物理性质是。(2)、实验室制取二氧化碳的反应原理:(用化学方程式表示),你认为CO2能否使干燥的紫色石蕊纸花变红色?(选填“能”或“不能”)若某同学用一定质量分数的盐酸与石灰石反应,将制得的CO2通入到澄清的石灰水中,观察未变浑浊,其原因可能是。(3)、若实验室用大理石和稀盐酸制取和收集一瓶干燥的二氧化碳气体,同时检验二氧化碳,若气流按从左到右方向,用仪器接口字母表示连接顺序为:b→h→i﹣→→→j(选填小写字母)。(4)、实验室常用加热氯化铵和氢氧化钙的固体混合物来制取氨气,应选用的发生装置是(填字母)。16. 实验室常用如图装置测定空气中氧气的含量。 (1)、(实验原理)该实验反应的原理是(用文字表达式表示)。(2)、(实验步骤)具体实验步骤有:
(1)、(实验原理)该实验反应的原理是(用文字表达式表示)。(2)、(实验步骤)具体实验步骤有:①在硬质玻璃管中装入铜粉,两端塞上带导管的橡皮塞,其中一端用气球密封;
②测量出实验所用硬质玻璃管的容积;
③停止加热后,待试管冷却至室温,注射器活塞稳定后,记录注射器中气体的体积;
④酒精灯在铜粉部位加热,加热时不断推拉注射器:
⑤移动注射器活塞,在注射器中留下一定体积的气体,记录体积后与硬质玻璃管另一端密封连接,并将硬质玻璃管固定在铁架台上。
a.正确的操作步骤为(填数字序号);
b.在实验加热过程中,硬质玻璃管中观察到的现象是;缓慢推拉注射器活塞 的目的是;
(3)、(实验记录)如表是甲、乙、丙三组同学记录的实验数据:实验小组
硬质玻璃管 的容积/mL
反应前注射器中气体体积/mL
反应后注射器中气体体积/mL
反应消耗的氧气体积/mL
空气中氧气的体积分数(%)
甲
45
15
4
11
18.3
乙
40
18
5
13
22.4
丙
50
20
6
填写上表中空白,帮助丙组同学完成实验数据的统计;
(实验分析)从上述数据中可知,该实验存在一定误差,导致该实验数据比21%小的原因不可能是(填数字序号)。
①没有缓缓推拉注射器活塞;
②读数时没有冷却至室温;
③加入铜丝量太多;
④反应后读数时小气球中气体未全部挤出
五、计算题
-
17. 化学兴趣小组用一瓶久置的过氧化氢溶液制取氧气并测量过氧化氢的质量分数。现称量68g 过氧化氢溶液和 0.1g 二氧化锰进行实验,反应前后质量随时间变化关系如图.

计算:
(1)、制得氧气的质量是__g;(2)、过氧化氢质量分数是?
-