陕西省汉中市2019-2020学年高三上学期化学第五次质量检测试卷
试卷更新日期:2019-10-30 类型:月考试卷
一、选择题:本题共14个小题,每小题3分.共42分
-
1. 下列表示正确的是( )A、中子数为20的Ar原子: B、硝基苯的结构简式:
 C、次氯酸的电了式:
C、次氯酸的电了式:  D、CH4的比例模型:
D、CH4的比例模型:  2. 下列有关叙述正确的是( )A、据悉中国在建的第二艘航母中使用了素有“现代工业的骨骼”之称的碳纤维.碳纤维是一种新型的有机高分子材料 B、离子交换膜在工业上应用广泛,如氯碱工业使用阴离子交换膜 C、获得2015年诺贝尔生理学或医学奖屠呦呦女士用乙醚从黄花蒿中提取出青蒿素,该技术应用了萃取原理 D、酸碱指示剂变色,煤的液化、蛋白质的颜色反应、海水提取溴、焰色反应都涉及化学变化3. 设NA为阿伏加德罗常数的值,下列说法正确的是( )A、标准状况下,2.24 L Cl2通入NaOH溶液中反应转移的电子致为0.2NA B、常温下,1 L pH=11的NaOH溶液中由水电离出的H+的数目为10-11NA C、273 K、101 kPa 下.22.4 L由NO和O2组成的混合气体中所含分子总数为NA D、100 g 34%双氧水中含有H—O键的数目为2NA4. X、Y、Z、R、W是5种短周期元素,原子序数依次增大:它们可组成离子化合物Z2Y和其价化合物RY2、XW4;已知Y、R同主族,Z、R、W同周期。下列说法错误的是( )A、原子半径:Z>R>W B、气态氢化物稳定性:HmW>HnR C、XW4分子中各原子均满足8电子结构 D、Y、Z、R三种元素组成的化合物水溶液一定显碱性5. 二氧化氯(ClO2)是国际上公认的安全、无毒的绿色消毒剂,对酸性污水中的Mn2+也有明显的去除效果,其反应原理为:ClO2+Mn2+→MnO2↓+Cl-(部分反应物和产物省略、未配平),下列有关该反应的说法正确的是( )
2. 下列有关叙述正确的是( )A、据悉中国在建的第二艘航母中使用了素有“现代工业的骨骼”之称的碳纤维.碳纤维是一种新型的有机高分子材料 B、离子交换膜在工业上应用广泛,如氯碱工业使用阴离子交换膜 C、获得2015年诺贝尔生理学或医学奖屠呦呦女士用乙醚从黄花蒿中提取出青蒿素,该技术应用了萃取原理 D、酸碱指示剂变色,煤的液化、蛋白质的颜色反应、海水提取溴、焰色反应都涉及化学变化3. 设NA为阿伏加德罗常数的值,下列说法正确的是( )A、标准状况下,2.24 L Cl2通入NaOH溶液中反应转移的电子致为0.2NA B、常温下,1 L pH=11的NaOH溶液中由水电离出的H+的数目为10-11NA C、273 K、101 kPa 下.22.4 L由NO和O2组成的混合气体中所含分子总数为NA D、100 g 34%双氧水中含有H—O键的数目为2NA4. X、Y、Z、R、W是5种短周期元素,原子序数依次增大:它们可组成离子化合物Z2Y和其价化合物RY2、XW4;已知Y、R同主族,Z、R、W同周期。下列说法错误的是( )A、原子半径:Z>R>W B、气态氢化物稳定性:HmW>HnR C、XW4分子中各原子均满足8电子结构 D、Y、Z、R三种元素组成的化合物水溶液一定显碱性5. 二氧化氯(ClO2)是国际上公认的安全、无毒的绿色消毒剂,对酸性污水中的Mn2+也有明显的去除效果,其反应原理为:ClO2+Mn2+→MnO2↓+Cl-(部分反应物和产物省略、未配平),下列有关该反应的说法正确的是( )
A、工业上可用更为廉价的Cl2来代替ClO2 B、利用该原理处理含Mn2+的污水后溶液的pH升高 C、该反应中氧化产物和还原产物的物质的量之比为2:5 D、理论上处理含1 mol Mn2+的污水,需要标准状况下的ClO28.96L6. 能正确表达下列反应的离子方程式为( )A、用醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O B、硫化亚铁与浓硫酸混合加热:2H++FeS=H2S↑+Fe2+ C、向硫酸铝溶液中滴加碳酸钠溶液:2Al3++3CO32-=Al2(CO3)3↓ D、用氢氧化钠溶液吸收工业废气中的NO2:2NO2+2OH-=NO3-+NO2-+H2O7. 研究表明,大气中氮氧化物和碳氢化合物受紫外线作用可产生二次污染物—光化学烟雾,其中某些反应过程如图所示。下列说法不正确的是( ) A、整个过程中O3作催化剂 B、反应Ⅲ的方程式为O2+O=O3 C、光化学烟雾中含甲醛、乙醛等刺激性物质 D、反应Ⅰ、反应Ⅱ均属于氧化还原反应8. 中美元首G20峰会确定携手采取积极行动管制芬太尼。芬太尼为一种麻醉、镇痛药物,超剂量使用该药物会导致严重后果,其结构简式如图所示。下列说法正确的是( )
A、整个过程中O3作催化剂 B、反应Ⅲ的方程式为O2+O=O3 C、光化学烟雾中含甲醛、乙醛等刺激性物质 D、反应Ⅰ、反应Ⅱ均属于氧化还原反应8. 中美元首G20峰会确定携手采取积极行动管制芬太尼。芬太尼为一种麻醉、镇痛药物,超剂量使用该药物会导致严重后果,其结构简式如图所示。下列说法正确的是( ) A、芬太尼分子中含有碳碳双键官能团 B、芬太尼分子中所有的碳原子可能共平面 C、芬太尼的一氯取代物有13种 D、芬太尼的分子式为C22H22N2O9. 下列化学实验事实及其解释正确的是( )A、将饱和氯水滴到淀粉碘化钾试纸上,如果试纸先变蓝后变白,说明氯气具有氧化性和漂白性 B、向Na2S2O3稀溶液中加入稀硫酸,发生如下反应:S2O32-+2H+=SO2↑+S↓+H2O,利用产生浑浊的快慢或产生气泡的快慢可以测定该反应在不同条件下的反应速率 C、乙酸乙酯中少量乙醇杂质可加水除去,其原理与溴水中加四氯化碳萃取溴类似 D、将SO2通入品红溶液中,品红溶液褪色,加热褪色后的溶液,恢复红色,说明亚硫酸不稳定10. 如图为某二次电池充电时的工作原理示意图,该过程可实现盐溶液的淡化。下列说法错误的是( )
A、芬太尼分子中含有碳碳双键官能团 B、芬太尼分子中所有的碳原子可能共平面 C、芬太尼的一氯取代物有13种 D、芬太尼的分子式为C22H22N2O9. 下列化学实验事实及其解释正确的是( )A、将饱和氯水滴到淀粉碘化钾试纸上,如果试纸先变蓝后变白,说明氯气具有氧化性和漂白性 B、向Na2S2O3稀溶液中加入稀硫酸,发生如下反应:S2O32-+2H+=SO2↑+S↓+H2O,利用产生浑浊的快慢或产生气泡的快慢可以测定该反应在不同条件下的反应速率 C、乙酸乙酯中少量乙醇杂质可加水除去,其原理与溴水中加四氯化碳萃取溴类似 D、将SO2通入品红溶液中,品红溶液褪色,加热褪色后的溶液,恢复红色,说明亚硫酸不稳定10. 如图为某二次电池充电时的工作原理示意图,该过程可实现盐溶液的淡化。下列说法错误的是( ) A、充电时,a为电源正极 B、充电时,Cl-向Bi电极移动,Na+向NaTi2(PO4)3电极移动 C、放电时,正极的电极反应为BiOCl+2H++3e-=Bi+Cl-+H2O D、充电时,新增入电极中的物质:n(Na+):n(Cl-)=1:311. 高纯度氧化铝有广泛的用途,某研究小组用以下流程制取高纯度氧化铝:
A、充电时,a为电源正极 B、充电时,Cl-向Bi电极移动,Na+向NaTi2(PO4)3电极移动 C、放电时,正极的电极反应为BiOCl+2H++3e-=Bi+Cl-+H2O D、充电时,新增入电极中的物质:n(Na+):n(Cl-)=1:311. 高纯度氧化铝有广泛的用途,某研究小组用以下流程制取高纯度氧化铝:
以下说法不合理的是( )
A、“除杂”操作是加入过氧化氢后,用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+ . 发生的主要反应的离子方程式为2Fe2++H2O2+4NH3·H2O=2Fe(OH)3 ↓+4NH4+ B、配制硫酸铝溶液时,需用硫酸酸化的目的是抑制Al3+水解 C、“结晶”这步操作中,母液需要蒸干后才能获得铵明矾晶体(含结晶水) D、“分离”操作的名称是过滤12. 下列图示与对应的叙述相符的是( ) A、图甲表示常温下稀释pH=11的NaOH溶液和氨水时溶液pH的变化,曲线Ⅱ表示氨水 B、图乙表示常温下,0.1000mol·L-1NaOH溶液滴定20.00mL 0.1000mol·L-1醋酸溶液的滴定曲线 C、图丙表示某可逆反应的反应速率随时间的变化,t0时刻改变的条件一定是使用了催化剂 D、图丁表示反应4CO(g)+2NO2(g) N2(g)+4CO2(g),在其他条件不变的情况下改变起始CO的物质的量,平衡时N2的体积分数变化情况,由图可知NO2的转化率c>b>a13. 下列设计的实验方案能达到相应实验目的的是( )
A、图甲表示常温下稀释pH=11的NaOH溶液和氨水时溶液pH的变化,曲线Ⅱ表示氨水 B、图乙表示常温下,0.1000mol·L-1NaOH溶液滴定20.00mL 0.1000mol·L-1醋酸溶液的滴定曲线 C、图丙表示某可逆反应的反应速率随时间的变化,t0时刻改变的条件一定是使用了催化剂 D、图丁表示反应4CO(g)+2NO2(g) N2(g)+4CO2(g),在其他条件不变的情况下改变起始CO的物质的量,平衡时N2的体积分数变化情况,由图可知NO2的转化率c>b>a13. 下列设计的实验方案能达到相应实验目的的是( )选项
实验目的
实验方案
A
探究化学反应的限度
取5mL0.1mol/LKI溶液滴加0.1 molL FeCl3溶液5~6滴,充分反应,可根据溶液中既含l2又含I-的实验事实判断该反应是可逆反应
B
探究浓度对化学反应速率的影响
用两支试管各取5mL0.1mol/L的KMnO4溶液,分别加入2mL0.1mol/L和0.2mol/L的H2C2O4(草酸)溶液,记录溶液褪色所需的时间
C
证明海带中含有碘元素
将海带剪碎、加蒸馏水浸泡,取滤液加几滴稀硫酸和1mLH2O2 , 再加入几滴淀粉溶液,溶液变蓝
D
验证 CH3COONa溶液中存在水解平衡
取 CH3COONa:溶液于试管中并加入几滴酚酞试剂,再加入醋酸铵固体(其水溶液呈中性),观察溶液颜色变化
A、A B、B C、C D、D14. 25℃时,体积均为20mL、浓度均为0.1mol·L-1的两种酸HX、HY分别与0.1mol·L-1的NaOH溶液反应,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是( ) A、a点c(X-)>b点c(Y-) B、HX发生反应的离子方程式为HX+OH-=X+H2O C、Ka(HY)的数量级约为10-3 D、pH=7时,两种反应后的溶液中c(Y-)>c(X-)
A、a点c(X-)>b点c(Y-) B、HX发生反应的离子方程式为HX+OH-=X+H2O C、Ka(HY)的数量级约为10-3 D、pH=7时,两种反应后的溶液中c(Y-)>c(X-)二、非选择题:本卷包括5道题,满分58分,考生根据要求作答。
-
15. 铅精矿可用于冶炼金属铅,其主要成分为PbS。
Ⅰ.火法炼铅将铅精矿在空气中焙烧,生成PbO和SO2。
(1)、用铅精矿火法炼铅的反应的化学方程式为。(2)、火法炼铅的废气中含低浓度SO2 , 可将废气通入过量氨水中进行处理,反应的离子方程式为。(3)、Ⅱ.湿法炼铅在制备金属铅的同时,还可制得硫磺,相对于火法炼铅更为环保。湿法炼铅的工艺流程如下:
已知:①不同温度下PbCl2的溶解度如下表所示。
温度(℃)
20
40
60
80
100
溶解度(g)
1.00
1.42
1.94
2.88
3.20
②PbCl2为能溶于水的弱电解质,在Cl-浓度较大的溶液中,存在平衡
PbCl2(aq)+ 2Cl- (aq) PbCl42-(aq)
浸取液中FeCl3的作用是。
(4)、操作a为加适量水稀释并冷却,该操作有利于滤液1中PbCl2的析出,分析可能的原因是 。(5)、将溶液3和滤液2分别置于右图所示电解装置的两个极室中,可制取金属铅并使浸取液中的FeCl3再生。
①溶液3应置于(填“阴极室”或“阳极室”)中。
②简述滤液2电解后再生为FeCl3的原理:。
③若铅精矿的质量为ag,铅浸出率为b,当电解池中通过cmol电子时,金属铅全部析出,铅精矿中PbS的质量分数的计算式为 。
16. 某小组设计不同实验方案比较Cu2+、Ag+的氧化性。(1)、方案1:通过置换反应比较:向酸化的AgNO3溶液插入铜丝,析出黑色固体,溶液变蓝。反应的离子方程式是 , 说明氧化性Ag+>Cu2+。(2)、方案2:通过Cu2+、Ag+分别与同一物质反应进行比较实验
试剂
编号及现象
试管
滴管

1.0mol·L-1 KI溶液
1.0mol·L-1AgNO3溶液
Ⅰ.产生黄色沉淀,溶液无色
1.0mol·L-1 CuSO4溶液
Ⅱ.产生白色沉淀A,溶液变黄
①经检验, Ⅰ中溶液不含I2 , 黄色沉淀是。
②经检验,Ⅱ中溶液含I2。推测Cu2+做氧化剂,白色沉淀A是Cul,确认A的实验如下:

a.检验滤液无I2。溶液呈蓝色说明溶液含有 (填离子符号)。
b.白色沉淀B是 。
c.白色沉淀A与AgNO3溶液反应的离子方程式是。说明氧化性Ag+>Cu2+。
(3)、分析方案2中Ag+未能氧化I- , 但Cu2+氧化了的原因,设计实验如下:编号
实验1
实验2
实验3
实验



现象
无明显变化
a中溶液较快变棕黄色,b中电上折出银;电流计指针偏转
C中溶液较慢变浅黄色;电流计指针偏转
(电极均为石墨,溶液浓度均为1mol/L,b、d中溶液pH≈4)
①a中溶液呈棕黄色的原因是 (用电极反应式表示)。
②“实验3”不能说明Cu2+氧化了I-。依据是空气中的氧气也有氧化作用,设计实验证实了该依据,实验方案及现象是 。
③方案2中,Cu2+能氧化I- , 而Ag+未能氧化I-的原因。
(资料:Ag++I-=AgI↓ K1=1.2×1016;2Ag++2I-=2Ag↓+I2 K2=8.7×108)
17. 工业上可通过煤的液化合成甲醇,主反应为:CO(g)+2H2(g) CH3OH(I)△ H=x kJ/mol。(1)、已知常温下CH3OH、H2和CO的燃烧热分别为726.5kJ/mol、285.5kJ/mol、283.0 kJ/mol,则x=;为提高合成甲醇反应的选择性,关键因素是。(2)、温度在TK下,容积为1.00L的某密闭容器中进行上述反应,相关数据如图一。①该化学反应0-10min的平均速率v(H2)= ;M和N点的逆反应速率较大的是(填“va(M)”、“vb(N)”或“不能确定”)
②10min时容器内CO的体积分数为 。

③对于气相反应,常用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)表示平衡常数(以KP表示),其中,pB-p总×B的体积分数,若在TK下平衡气体总压强为xatm,则该反应Kp=(计算表达式)。实验测得不同温度下的1nK化学平衡常数K的自然对数)如图二,请分析1nK随T呈现上述变化趋势的原因是 。
(3)、干燥的甲醇可用于制造燃料电池。研究人员发现利用NaOH干燥甲醇时,温度控制不当会有甲酸盐和H2生成,其反应方程式为。三、选考题:考生需从18题和19题中选择一题作答,两题都答者按第一题计分
-
18. 【化学一选修3:物质结构与性质】
硒化锌是一种半导体材料,回答下列问题
(1)、锌在周期表中的位置;Se基态原子价电子排布图为。元素锌、硫和硒第一电离能较大的是 (填元素符号)。(2)、Na2SeO3分子中Se原子的杂化类型为;H2SeO4的酸性比H2SeO3强,原因是 。(3)、气态SeO3分子的立体构型为; 与SeO3互为等电子体的有(填序号)。A CO32- B NO3- C. NCl3 D.SO32-
(4)、硒化锌的晶胞结构如图所示,图中X和Y点所堆积的原子均为(填元素符号):该晶胞中硒原子所处空隙类型为(填“立方体”、“正四面体”或“正八面体”),该种空隙的填充率为;若该晶胞密度为pg·cm3 , 硒化锌的摩尔质量为 Mg.mol-1。用NA代表阿伏加德罗常数的数值,则晶胞参数a为 nm。 19. 【化学一选修5:有机化学基础】具有抗菌作用的白头翁素衍生物M的合成路线如下图所示:
19. 【化学一选修5:有机化学基础】具有抗菌作用的白头翁素衍生物M的合成路线如下图所示: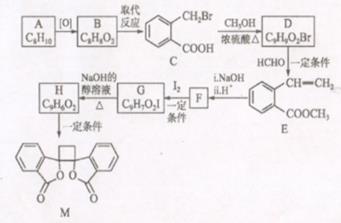
已知:i.RCH2Br R-HC=CH-R‘
ii.R-HC=CH-R'
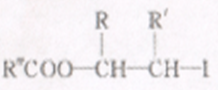
iii.R-HC=CH-R’
 (以上R、R'、R"代表氢、烷基或芳基等)(1)、D中官能团名称为 , A的化学名称为 。(2)、F的结构简式 为 ,则与F具有相同官能团的同分异构体共种(考虑顺反异构,不包含F)(3)、由G生成H的化学方程式为 ,反应类型为 。(4)、下列说法不正确的是 (选填字母序号)。A、可用硝酸银溶液鉴别B,C两种物质 B、由H生成M的反应是加成反应 C、1molE最多可以与4molH2发生加成反应 D、1molM与足量NaOH溶液反应,消耗4 mol NaOH(5)、以乙烯为起始原料,结合已知信息选用必要的无机试剂,写出合成
(以上R、R'、R"代表氢、烷基或芳基等)(1)、D中官能团名称为 , A的化学名称为 。(2)、F的结构简式 为 ,则与F具有相同官能团的同分异构体共种(考虑顺反异构,不包含F)(3)、由G生成H的化学方程式为 ,反应类型为 。(4)、下列说法不正确的是 (选填字母序号)。A、可用硝酸银溶液鉴别B,C两种物质 B、由H生成M的反应是加成反应 C、1molE最多可以与4molH2发生加成反应 D、1molM与足量NaOH溶液反应,消耗4 mol NaOH(5)、以乙烯为起始原料,结合已知信息选用必要的无机试剂,写出合成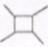 的路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
的路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)