2017年四川省达州市渠县九校联考中考化三模试卷
试卷更新日期:2017-07-11 类型:中考模拟
一、选择题
-
1. 自然界的下列过程或现象中,伴随着化学变化的是( )A、北极冰川融化 B、高原水土流失 C、地下煤炭形成 D、天上雨雪转换2. 下列物质的用途,利用其物理性质的是( )A、氮气填充在灯泡中作保护气 B、还原性铁粉在月饼盒内作除氧剂 C、干冰在舞台制雾时作致冷剂 D、生石灰在某些食品袋内作干燥剂3. 下列对某一主题的知识归纳,有错误的一组是( )
A.化学常识
B.化学与食品
空气的主要成分﹣﹣氮气和氧气
除 暖 瓶 水 垢﹣﹣可用食醋浸泡
甲 醛﹣﹣浸泡肉类食品,以防变质
工业盐﹣﹣用来腌制凉果、酸菜等食物
C.化学与生活
D.化学与能源
NaOH溶液、澄清石灰水﹣﹣用Na2CO3溶液来鉴别
化纤织物、纯毛织物﹣﹣用灼烧闻气味来鉴别
沼气、酒精﹣﹣生物能源,可再生能源
石油、煤﹣﹣化石能源,不可再生能源
A、A B、B C、C D、D4. 物质存放在烧杯中一段时间后,质量变大且变质的是( )①浓盐酸 ②浓硫酸 ③烧碱 ④食盐 ⑤生石灰 ⑥稀硫酸.
A、①⑥ B、②③⑤ C、③⑤ D、②③④5. 能共存于pH=13且溶液颜色为无色透明的溶液的离子组是( )A、H+、Cl﹣、NO3﹣、Ba2+ B、Na+、Cu2+、Cl﹣、NO3﹣ C、Ba2+、NO3﹣、Na+、Cl﹣ D、Fe3+、K+、Cl﹣、SO42﹣6. 类推是一种重要的学习方法,但如果不具体问题具体分析就会产生错误的结论.下列类推结论错误的是( )①CO能与Fe2O3反应生成Fe,CO也能与CuO反应生成Cu
②NaOH溶液能使无色酚酞试液变红色,Cu(OH)2也能使无色酚酞试液变红色
③有机化合物含碳元素,则含碳元素的化合物一定是有机化合物
④溶液是均一稳定的,则均一稳定的液体一定是溶液
⑤碱溶液呈碱性,能使无色酚酞变红,则呈碱性的溶液一定是碱溶液.
A、②③④⑤ B、①②⑤ C、①⑤ D、③④⑤7. 欲除去不纯物质中的杂质(括号内杂质),所用试剂和方法均正确的是( )选项
待提纯物质
选用试剂
操作方法
A
CO2(H2O)
生石灰
气体通过盛有生石灰的干燥管
B
Cu(Fe)
稀硫酸
搅拌、过滤、洗涤、干燥
C
CuSO4溶液(硫酸)
氧化铜
蒸发、洗涤
D
NaCl(Na2CO3)
氯化钡
加过量氯化钡溶液后过滤
A、A B、B C、C D、D8. 下列四个图象能正确反映实验变化关系的有( )A
B
C
D
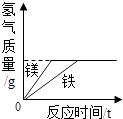

常温下,足量的镁、铁分别同时放入少量等质量、等质量分数的稀盐酸中
敞口放置于空气中的浓硫酸或稀盐酸
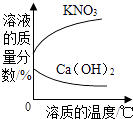
加热KNO3、Ca(OH)2的饱和溶液(不考虑溶剂的蒸发)
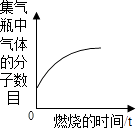
少量的碳在密闭的集气瓶中与氧气完全燃烧
A、A B、B C、C D、D二、填空题
-
9. 用化学用语表示:
①相对分子质量最小的氧化物
②2个铁离子 .
③小苏打中碳元素的化合价
④地壳中含量最多的金属元素 .
10. 化学与我们的生活密切相关:(1)、人们误食重金属盐(如:硫酸铜、氯化钡等)可通过喝大量豆浆的方法解毒.由此可知喝下列物质中的也可以达到同样的目的.①牛奶 ②果汁 ③蛋清 ④矿泉水 ⑤食盐水
(2)、无人驾驶汽车处理系统的核心材料是高纯度的硅.工业制硅的反应之一如下:2X+SiCl4=Si+4HCl.该反应中,X的化学式是 .(3)、化学电池在放电时发生化学变化,由能转化为能.(4)、煤燃烧产生的某种气体是形成酸雨的主要原因,在煤中加入可以减少其的排放.11. 甲、乙两组同学分别设计了如下实验,图中试剂混合前后物质的总质量分别表示为M(前)、M(后).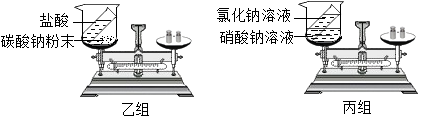
请根据图示回答:
(1)、甲组实验中,M(前)>M(后),原因是;若所用试剂不变,改进的方法是;(2)、乙组实验中,M(前)=M(后),丙组同学认为该实验不能验证质量守恒定律,原因是 .(3)、丁组同学研究了物质W的组成.一定条件下,W在密闭容器内发生反应前后各物质的质量如下图所示: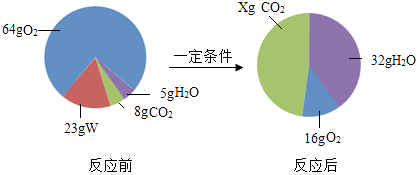
其中,x=g,W的化学式是 . (按碳、氢、氧元素顺序书写)
12. 现有一固体混合物A的成分,已知其中可能含有NH4Cl、Na2SO4、CuCl2、NaCl、AgCl几种物质中的两种或多种.按如图所示进行实验,出现的现象如图中所述(设过程中所有可能发生的反应均恰好完全反应).
试根据实验过程和发生的现象填写以下空白(均填写相应的化学符号):
(1)、混合物A中,一定不存在的物质是 , 可能存在的物质是(2)、气体B是 , 现象X为(3)、滤液C中,存在的金属阳离子是(4)、滤渣D是 .(5)、写出实验过程③中发生的化学反应的化学方程式 .13. 金属在日常生活、工农业生产和科学研究方面应用广泛.(1)、铜可用来制作导线,是因为其具有良好的延展性和 .(2)、在空气中,铝表面生成一层致密的氧化膜,氧化膜的主要成分是 .(3)、小明将一包铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到滤渣和滤液.①锌和硝酸银溶液反应的化学方程式是 .
②若滤液为蓝色,则滤液中一定含有的金属离子是(写离子符号)
三、探究题
-
14. 如图是某学校化学课外学习小组设计的探究工业炼铁原理及产物验证的实验.实验 中所用氧化铁的质量为10g,硬质玻璃管的质量为50g.
 (1)、B装置中反应的化学方程式是;E装置中反应的化学方程式是 , 该反应是(选填“吸”或“放”)热反应.(2)、从实验安全的角度考虑D瓶中应盛放的试剂是 .(3)、F装置的作用是、 .(4)、为探究E装置中黑色粉末的成分是什么,同学们将反应后的黑色固体研细后,用磁铁吸引,发现黑色粉末全部能被吸引.当装置冷却后称得E装置中玻璃管和固体的总质量为59g.则剩余黑色固体中铁元素质量为 . 根据上述实验数据处理得出产物中黑色因体的成分是 .15. 众所周知,二氧化碳能使澄清的石灰水变浑浊(生成白色沉淀).但是,在分组实验中,向石灰水中通入二氧化碳(如图1所示),出现了意想不到的现象:有的石灰水未变浑浊;有的出现浑浊后又变澄清(沉淀消失).
(1)、B装置中反应的化学方程式是;E装置中反应的化学方程式是 , 该反应是(选填“吸”或“放”)热反应.(2)、从实验安全的角度考虑D瓶中应盛放的试剂是 .(3)、F装置的作用是、 .(4)、为探究E装置中黑色粉末的成分是什么,同学们将反应后的黑色固体研细后,用磁铁吸引,发现黑色粉末全部能被吸引.当装置冷却后称得E装置中玻璃管和固体的总质量为59g.则剩余黑色固体中铁元素质量为 . 根据上述实验数据处理得出产物中黑色因体的成分是 .15. 众所周知,二氧化碳能使澄清的石灰水变浑浊(生成白色沉淀).但是,在分组实验中,向石灰水中通入二氧化碳(如图1所示),出现了意想不到的现象:有的石灰水未变浑浊;有的出现浑浊后又变澄清(沉淀消失).
【提出问题】分组实验中,出现意想不到现象的原因是什么呢?
(1)、【猜想与假设】I.石灰水未变浑浊,是因为二氧化碳中混有少量氯化氢气体.
Ⅱ.石灰水未变浑浊,是因为 .
Ⅲ.石灰水出现浑浊后又变澄清,与石灰水的浓度、通入二氧化碳的时间有关.
(2)、【进行实验】实验装置如图2所示.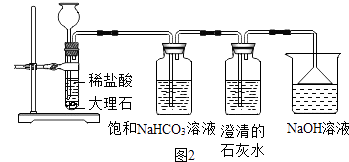
提示:①实验中所用盐酸与分组实验所用盐酸相同;
②CO2在饱和NaHCO3溶液中的溶解度非常小.
步骤1:分别取一定体积的饱和澄清石灰水与一定体积的蒸馏水混合配制成50mL溶液.
步骤2:分别向50mL溶液中通入一段时间的二氧化碳,记录现象.
实验序号
V饱和石灰水/mL
V蒸馏水
/mL
出现现象所需时间/s
开始浑浊
明显浑浊
沉淀减少
是否澄清
①
50
0
19
56
366
持续通入CO28min以上,沉淀不能完全消失
②
40
10
24
51
245
③
30
20
25
44
128
④
20
30
27
35
67
89s后完全澄清
⑤
10
40
通3min以上,均无明显现象
【解释与结论】
(1 )实验中,所用石灰水为饱和溶液的是(填序号).
(2 )二氧化碳使澄清石灰水变浑浊原因是(用化学方程式表示).
(3 )饱和NaHCO3溶液的作用是 .
(4 )通过实验分析,猜想 I(填“成立”或“不成立”),猜想Ⅱ、Ⅲ成立.
(3)、【反思与评价】向澄清的石灰水中通入二氧化碳,为避免出现“意想不到的现象”,你的建议是 .
四、计算题
-
16. 现有含HCl和CuCl2的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图所示.
 (1)、当加入NaOH溶液质量为ag时,溶液中的溶质有;(2)、求混合溶液中CuCl2的质量分数.(3)、求恰好完全反应时,消耗NaOH溶液的总质量.
(1)、当加入NaOH溶液质量为ag时,溶液中的溶质有;(2)、求混合溶液中CuCl2的质量分数.(3)、求恰好完全反应时,消耗NaOH溶液的总质量.