2016-2017学年安徽省宣城市六校联考高二下学期期中化学试卷
试卷更新日期:2017-07-03 类型:期中考试
一、选择题
-
1. 化学与生产和生活密切相关,下列说法正确的是( )A、乙烯是化学物质,不可用作水果的催熟剂 B、煤经过气化和液化等物理变化可转化为清洁燃料 C、石油是混合物,经分馏后得到汽油、煤油和柴油等纯净物 D、汽油与水互不相溶,但不可以用裂化汽油萃取溴水中的溴2. 设NA为阿伏加德罗常数的值,下列说法中不正确的是( )A、1molC2H4Cl2中含有共用电子对数目为7NA B、标准状况下,44.8 L丙三醇与足量金属钠反应,生成气体的分子数为3NA C、20℃时,1 mol己烷完全燃烧后恢复至原状态,生成气态物质分子数为6NA D、15g甲基正离子(CH3+)所含有的电子数是8NA3. 下列物质的沸点按由高到低顺序排列正确的是( )
①丙三醇
②丁烷
③乙二醇
④乙醇.
A、①②③④ B、④③②① C、②①③④ D、①③④②4. 下列实验能达到预期目的是( )A、用溴水检验汽油中是否含有不饱和脂肪烃 B、除去苯中混有的苯酚,加入浓溴水,过滤 C、除去乙醇中混有的水,加入金属钠,蒸馏 D、乙烷气体中混有乙烯,通入酸性高锰酸钾溶液,洗气5. 二甲醚和乙醇是同分异构体,其鉴别可采用化学方法及物理方法,下列鉴别方法中不能对二者进行鉴别的是( )A、利用金属钠或者金属钾 B、利用质谱法 C、利用红外光谱法 D、利用核磁共振氢谱6. 某一溴代烷水解后的产物在红热铜丝催化下,最多可被空气氧化生成4种不同的醛,该一溴代烷的分子式可能是( )A、C4H9Br B、C5H11Br C、C6H13Br D、C7H15Br7. 化合物丙由如下反应制得:C4H10O C4H8 C4H8Br2(丙),丙的结构简式不可能是( )A、CH3CH2CHBrCH2Br B、CH3CH(CH2Br)2 C、CH3CHBrCHBrCH3 D、(CH3)2CBrCH2Br8. 天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )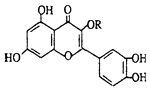 A、可溶于有机溶剂 B、分子中有三个苯环 C、1mol维生素P可以和6molBr2反应 D、1mol维生素P可以和4molNaOH反应9.
A、可溶于有机溶剂 B、分子中有三个苯环 C、1mol维生素P可以和6molBr2反应 D、1mol维生素P可以和4molNaOH反应9.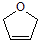 是一种有机烯醚,可由链烃A通过下列路线制得,下列说法正确的是( )
是一种有机烯醚,可由链烃A通过下列路线制得,下列说法正确的是( ) A B C
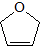 A、B中含有的官能团有溴原子、碳碳双键 B、A的结构简式是CH2═CHCH2CH3 C、该有机烯醚不能发生加聚反应 D、①②③的反应类型分别为加成反应、取代反应、消去反应10. 一种气态烷烃和一种气态烯烃的混合物共10g,平均相对分子质量为25.使混合气通过足量溴水,溴水增重8.4g,则混合气中的烃分别是( )A、甲烷和乙烯 B、甲烷和丙烯 C、乙烷和乙烯 D、乙烷和丙烯11. 实验室制取的乙炔气体中常混有少量H2S、CO2和水蒸气,为了得到干燥纯净的乙炔气体,选择最简便的实验方案有( )A、通过NaOH后,通过浓H2SO4 , 再通过石灰水 B、通过CuSO4溶液后再通过石灰水 C、通过五氧化磷,再通过无水CaCl2 D、通过足量的碱石灰12. 下列各组物质中,相互间一定互为同系物的是( )A、邻二甲苯和对二甲苯 B、C4H8O2和C3H6O2 C、C4H10和C20H42 D、C6H5﹣OH和C6H5﹣CH2﹣OH13. 中国科学家屠呦呦因创制新型抗疟药﹣﹣青蒿素和双氢青蒿素获得2015年诺贝尔生理学或医学奖.青蒿素和双氢青蒿素的结构式如图.从青蒿中提取青蒿素主要采用有机溶剂提取的方法.下列有关说法不正确的是( )
A、B中含有的官能团有溴原子、碳碳双键 B、A的结构简式是CH2═CHCH2CH3 C、该有机烯醚不能发生加聚反应 D、①②③的反应类型分别为加成反应、取代反应、消去反应10. 一种气态烷烃和一种气态烯烃的混合物共10g,平均相对分子质量为25.使混合气通过足量溴水,溴水增重8.4g,则混合气中的烃分别是( )A、甲烷和乙烯 B、甲烷和丙烯 C、乙烷和乙烯 D、乙烷和丙烯11. 实验室制取的乙炔气体中常混有少量H2S、CO2和水蒸气,为了得到干燥纯净的乙炔气体,选择最简便的实验方案有( )A、通过NaOH后,通过浓H2SO4 , 再通过石灰水 B、通过CuSO4溶液后再通过石灰水 C、通过五氧化磷,再通过无水CaCl2 D、通过足量的碱石灰12. 下列各组物质中,相互间一定互为同系物的是( )A、邻二甲苯和对二甲苯 B、C4H8O2和C3H6O2 C、C4H10和C20H42 D、C6H5﹣OH和C6H5﹣CH2﹣OH13. 中国科学家屠呦呦因创制新型抗疟药﹣﹣青蒿素和双氢青蒿素获得2015年诺贝尔生理学或医学奖.青蒿素和双氢青蒿素的结构式如图.从青蒿中提取青蒿素主要采用有机溶剂提取的方法.下列有关说法不正确的是( )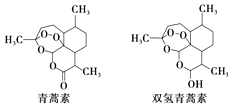 A、青蒿素的分子式为C15H22O5 B、青蒿素通过还原反应可制得双氢青蒿素 C、青蒿素有青蒿的芳香气味,是芳香族化合物 D、用有机溶剂乙醚从青蒿中提取青蒿素,主要采用萃取的方法14.
A、青蒿素的分子式为C15H22O5 B、青蒿素通过还原反应可制得双氢青蒿素 C、青蒿素有青蒿的芳香气味,是芳香族化合物 D、用有机溶剂乙醚从青蒿中提取青蒿素,主要采用萃取的方法14.柠檬烯是一种常用香料,其结构简式如图.
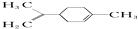 有关柠檬烯的分析正确的是( )
有关柠檬烯的分析正确的是( )
A、A.它的一氯代物有6种 B、它和丁基苯(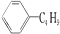 )互为同分异构体
C、它的分子中所有的碳原子一定在同一平面上
D、一定条件下,它分别可以发生加成、取代、氧化、还原等反应
15. 科学研究发现,具有高度对称性的有机分子具有致密性高,稳定性强,张力能大等特点,因此这些分子成为2014年化学界关注的热点,下面是几种常见高度对称烷烃的分子碳架结构,这三种烷烃的二氯取代产物的同分异构体数目分别是( )
)互为同分异构体
C、它的分子中所有的碳原子一定在同一平面上
D、一定条件下,它分别可以发生加成、取代、氧化、还原等反应
15. 科学研究发现,具有高度对称性的有机分子具有致密性高,稳定性强,张力能大等特点,因此这些分子成为2014年化学界关注的热点,下面是几种常见高度对称烷烃的分子碳架结构,这三种烷烃的二氯取代产物的同分异构体数目分别是( ) A、2种,4种,8种 B、2种,4种,6种 C、1种,3种,6种 D、1种,3种,8种16. 有机化合物的结构可用键线式表示,如CH2═CHCH2Br可表示为
A、2种,4种,8种 B、2种,4种,6种 C、1种,3种,6种 D、1种,3种,8种16. 有机化合物的结构可用键线式表示,如CH2═CHCH2Br可表示为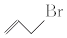 .则关于有机物
.则关于有机物  的说法正确的有( ) A、与苯互为同分异构体 B、其二氯代物有3种 (不考虑立体异构) C、分子中所有的碳原子在同一平面上 D、属于烯烃,是乙烯的同系物17. x、y、z三种物质的分子组成分别符合烷烃、烯烃、炔烃的通式,若在一定条件下VL的x、y、z的混合气体可与V L的H2发生加成反应,则混合气体中x、y、z的体积比可能是( )A、1:1:1 B、1:2:3 C、1:4:2 D、3:2:118. 25℃和101kPa时,乙烷、乙炔和丙烯组成的混合烃32mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了72mL,原混合烃中乙炔的体积分数为( )A、12.5% B、25% C、50% D、75%
的说法正确的有( ) A、与苯互为同分异构体 B、其二氯代物有3种 (不考虑立体异构) C、分子中所有的碳原子在同一平面上 D、属于烯烃,是乙烯的同系物17. x、y、z三种物质的分子组成分别符合烷烃、烯烃、炔烃的通式,若在一定条件下VL的x、y、z的混合气体可与V L的H2发生加成反应,则混合气体中x、y、z的体积比可能是( )A、1:1:1 B、1:2:3 C、1:4:2 D、3:2:118. 25℃和101kPa时,乙烷、乙炔和丙烯组成的混合烃32mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了72mL,原混合烃中乙炔的体积分数为( )A、12.5% B、25% C、50% D、75%二、非选择题
-
19. 下列八种物质:①丙烯、②聚乙烯、③1﹣溴丁烷、④苯、⑤甲苯、⑥1﹣丁醇、⑦苯酚、⑧乙醚(1)、既能与酸性高锰酸钾溶液反应,又能与溴水反应的是(填序号,下同)(2)、互为同系物的有(3)、互为同分异构体的有(4)、写出③与NaOH醇溶液反应的化学方程式(5)、写出⑥在铜催化下被氧化的化学方程式 .20. 0.1mol某烃在足量的氧气中完全燃烧,生成CO2和水各0.6mol,则该烃的分子式为 . 若该烃不能使溴水或高锰酸钾溶液褪色,但在一定条件下,可以和溴蒸气发生取代反应,其一溴取代物只有一种,则此烃结构简式为 , 名称是 . 若该烃能使溴水褪色,且能在催化剂作用下与H2发生加成反应,生成2,2﹣二甲基丁烷,则此烃结构简式为 , 名称是 , 与溴发生加成反应的化学方程式为 .21. 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图:

 +H2O,
+H2O, 
可能用到的有关数据如表:
相对分子质量
密度/(g•cm﹣3)
沸点/℃
溶解性
环己醇
100
0.961 8
161
微溶于水
环己烯
82
0.810 2
83
难溶于水
合成反应:
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓H2SO4 , b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯12g.
回答下列问题:
(1)、装置b的名称是 .(2)、本实验中最容易产生的副产物的结构简式为 , 生成该物质的反应类型是(3)、分液漏斗在使用前须清洗干净并 , 在本实验分离过程中,产物应该从分液漏斗的(填“上口倒出”或“下口倒出”).(4)、在环己烯粗产物蒸馏过程中,不可能用到的仪器有 (填正确答案标号).A、蒸馏烧瓶 B、温度计 C、分液漏斗 D、锥形瓶 E、蒸发皿(5)、本实验所得到的环己烯产率是 .22. 为测定某有机物A的结构,进行如下实验.[分子式的确定]
(1)、将有机物A置于氧气流中充分燃烧,实验测得:生成9.0g H2O和17.6g CO2 , 消耗氧气13.44L(标准状况下).则该物质的最简式是 , 能否据此确定该有机物的分子式(若能则写出其分子式,若不能请说明理由)(2)、根据价键理论,预测A可能的结构种(不考虑立体异构).(3)、[结构式的确定]经测定,有机物A分子内有2种不同环境的氢原子,且A能与金属钠反应放出气体,则A的结构简式为 .
(4)、[性质实验]A在一定条件下脱水可生成B,B可发生加聚反应生成C,请写出A转化为B的化学反应方程式: .
(5)、体育比赛中当运动员肌肉扭伤时,队医随即用氯乙烷(沸点为12.27℃)对受伤部位进行局部冷冻麻醉.请选用B的某同系物和其他试剂及合适的方法制备氯乙烷,要求原子利用率为100%,写出制备反应方程式: .