2017年广东省东莞市中堂六校联考中考化学三模试卷
试卷更新日期:2017-06-28 类型:中考模拟
一、选择题
-
1. 生活中常见的下列现象,属于化学变化的是( )A、冰棒融化 B、米饭变馊 C、瓷碗破碎 D、湿衣晾干2. 下列属于复分解反应的是( )A、3Fe+2O2 Fe3O4 B、CaCO3 CaO+CO2↑ C、CuSO4+2NaOH═Cu(OH)2↓+Na2SO4 D、C+2CuO 2Cu+CO2↑3. 钚可用于核电,还可用于制造核武器,钚(Pu)的原子序数为94,该元素一种原子的质子数和中子数之和为239,下列关于该原子的说法不正确的是( )A、中子数为145 B、核外电子数为94 C、核电荷数为239 D、质子数为944. 有关化学与健康的说法不正确的是( )A、新鲜的水果蔬菜中富含维生素 B、用甲醛水溶液浸泡的海产品可以放心食用 C、人体缺少铁元素会引起贫血 D、葡萄糖在人体内可以转化成CO2和水并放出能量5. 下列基本实验操作正确的是( )A、
 检查气密性
B、
检查气密性
B、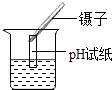 测量溶液的pH
C、
测量溶液的pH
C、 取固体药品
D、
取固体药品
D、 熄灭酒精灯
6. 我国成功发射的“嫦娥三号”使用长三丙运载火箭 其中火箭燃料用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作常规推进剂,当两者完全反应生成三种新物质,反应的化学方程式为 C2H8N2+2N2O4 3X+2CO2+4H2O,下列有关说法错误的是( )A、反应前后氮元素的化合价没有发生变化 B、X的化学式为N2 C、N2O4属于氧化物,在反应中做助燃剂 D、该反应属于放热反应7. 小明设计了如图装置探究“微粒是不断运动的”,一段时间后,可观察到的紫色石蕊变红,则物质A是( )
熄灭酒精灯
6. 我国成功发射的“嫦娥三号”使用长三丙运载火箭 其中火箭燃料用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作常规推进剂,当两者完全反应生成三种新物质,反应的化学方程式为 C2H8N2+2N2O4 3X+2CO2+4H2O,下列有关说法错误的是( )A、反应前后氮元素的化合价没有发生变化 B、X的化学式为N2 C、N2O4属于氧化物,在反应中做助燃剂 D、该反应属于放热反应7. 小明设计了如图装置探究“微粒是不断运动的”,一段时间后,可观察到的紫色石蕊变红,则物质A是( ) A、浓氨水 B、浓硫酸 C、生石灰 D、浓盐酸8. “分类”可以使人们有序的研究物质,以下分类正确的是( )A、合金:生铁、锰钢、青铜 B、碱:纯碱、烧碱、消石灰 C、盐:氯化银、氯化钠、氯化氢 D、合成材料:塑料、合成纤维、铝合金9. 下列化肥中能增强农作物抗病虫害和抗倒伏能力的是( )A、尿素[CO(NH2)2] B、氯化钾(KCl) C、硫酸铵[(NH4)2 SO4] D、磷矿粉[Ca3(PO4)2]10. 我国最近已研究出新型水处理剂ClO2的新制法,其反应的微观过程如图所示.下列说法不正确的是( )
A、浓氨水 B、浓硫酸 C、生石灰 D、浓盐酸8. “分类”可以使人们有序的研究物质,以下分类正确的是( )A、合金:生铁、锰钢、青铜 B、碱:纯碱、烧碱、消石灰 C、盐:氯化银、氯化钠、氯化氢 D、合成材料:塑料、合成纤维、铝合金9. 下列化肥中能增强农作物抗病虫害和抗倒伏能力的是( )A、尿素[CO(NH2)2] B、氯化钾(KCl) C、硫酸铵[(NH4)2 SO4] D、磷矿粉[Ca3(PO4)2]10. 我国最近已研究出新型水处理剂ClO2的新制法,其反应的微观过程如图所示.下列说法不正确的是( )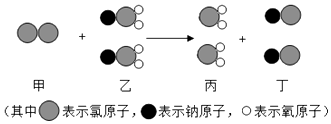 A、乙中氯元素的化合价为+3价 B、该反应前后分子的个数不变 C、该反应的本质是原子的重新组合 D、丙属于氧化物11. 把X、Y、Z三种金属分别放入稀硫酸中,X溶解并放出氢气,Y无明显变化,把Y放入Z的硫酸盐溶液中,过一会儿,表面有Z析出,则X、Y、Z的活动性顺序由弱到强的是( )A、X、Y、Z B、Y、Z、X C、Z、Y、X D、Z、X、Y12. 小明同学取生活中的四种物质,测得其pH如下表所示,其中酸性最强的是( )
A、乙中氯元素的化合价为+3价 B、该反应前后分子的个数不变 C、该反应的本质是原子的重新组合 D、丙属于氧化物11. 把X、Y、Z三种金属分别放入稀硫酸中,X溶解并放出氢气,Y无明显变化,把Y放入Z的硫酸盐溶液中,过一会儿,表面有Z析出,则X、Y、Z的活动性顺序由弱到强的是( )A、X、Y、Z B、Y、Z、X C、Z、Y、X D、Z、X、Y12. 小明同学取生活中的四种物质,测得其pH如下表所示,其中酸性最强的是( )物质
矿泉水
雨水
橙汁
蔗糖水
pH
7.3
5.8
3.6
7.0
A、矿泉水 B、雨水 C、蔗糖水 D、橙汁13. 如图是探究铁锈蚀条件的装置.调节L端与R端的液面高度一致,塞紧木塞,一周后观察.下列推断错误的是( ) A、b管中铁钉不会锈蚀 B、L端与R端液面高度仍然保持一致 C、该实验说明铁锈蚀与空气、水有关 D、若将a管中的水改为食盐水能加快铁的锈蚀14. 下列图象能正确反映其对应操作中各量变化关系的是( )A、
A、b管中铁钉不会锈蚀 B、L端与R端液面高度仍然保持一致 C、该实验说明铁锈蚀与空气、水有关 D、若将a管中的水改为食盐水能加快铁的锈蚀14. 下列图象能正确反映其对应操作中各量变化关系的是( )A、 用一定质量的高锰酸钾加热制氧气
B、
用一定质量的高锰酸钾加热制氧气
B、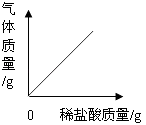 向一定质量的石灰石中加入过量的稀盐酸
C、
向一定质量的石灰石中加入过量的稀盐酸
C、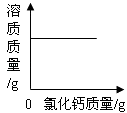 向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体
D、
向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体
D、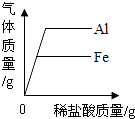 分别向等质量的铝和铁中加入溶质质量分数相同的稀盐酸至过量
分别向等质量的铝和铁中加入溶质质量分数相同的稀盐酸至过量
二、填空题
-
15. 用元素符号或化学式填空:(1)、2个氢氧根离子;(2)、2个氢原子:;(3)、氯化铝中氯元素显﹣1价;(4)、食盐水中的溶质 .16. 图中的①、②是氧元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图.

请你回答下列问题.
(1)、氧元素的原子序数为 , 钙元素的相对原子质量为 .(2)、B粒子属于(填“原子”、“阴离子”或“阳离子”);若D为原子,X= .(3)、A、B、C、D中属于同种元素的粒子是(填序号).17. 根据问题填空:(1)、通过图1可以说明燃烧条件之一是 , 但这个实验不能在酒精灯上加热时间过长原因是 .
 (2)、
(2)、图2中A、B对比说明燃烧需要的条件是 , 若B、C同样证明此条件,并且时间短现象明显,可以向烧杯C中最好加入固体、液体为(填序号)
①Na2CO3(粉末) HCl(稀) ②NaOH(粉末) HCl(稀)
③大理石(块状) HCl(稀) ④大理石(块状) H2SO4(稀)
 18. 如图是a、b、c三种物质的溶解度曲线:
18. 如图是a、b、c三种物质的溶解度曲线:
①P点的意义是;
②t2℃时,将50g a物质放入50g水中充分溶解,得到a的溶液的质量为 g(a物质不含结晶水);
③t2℃时,a、b、c三种物质的溶解度由大到小的顺序为:;将t2℃时a、b、c三种物质的饱和溶液降温至t1℃时,所得溶液的溶质质量分数关系是;
④t2℃时,将c的饱和溶液变为不饱和溶液,可采用的方法.
19. 随着经济的发展,能源与环境问题日益受到人们的关注和重视.(1)、目前,人类以化石燃料为主要能源.化石燃料有煤、和天然气,它们都属于(填“可再生”或“不可再生”)能源.甲烷完全燃烧的化学方程式为 .(2)、三大化石燃料的大量使用,会产生和二氧化氮等气体污染物,这些气体或气体在空气中发生反应后的生成物溶于雨水,会形成酸雨.防治酸雨产生的措施是 . (写出两点)三、综合题
-
20. 已知:A是红色粉末,B、C是氧化物,D、I是常见金属,E为胃酸的主要成分,G为单质.它们之间的转化关系如下:

请回答:
(1)、写出物质的化学式:A、C .(2)、上述转化①②③中,属于置换反应的有(填序号).(3)、为了安全,点燃G气体之前要 .(4)、写出与上述转化①、③有关反应的化学方程式:① , ③ .21. 由于地震和海啸,日本福岛第一核电站发生严重的核辐射泄漏,日本政府向福岛核电站附近居民发放碘片(主要成分是碘化钾KI),以降低放射性碘﹣131对人体的伤害.某兴趣小组为了测定某未知碘片中碘化钾的含量,进行了如图实验:
(查阅资料知:碘化钾易溶于水,而碘化银是不溶于水的黄色沉淀)
 (1)、上述步骤③中“物质M”的化学式为 , 其与碘化钾反应的化学方程式是 .(2)、步骤③中“X操作”是;该操作与步骤①中的操作都要用到除烧杯外的另一种玻璃仪器,它是 , 它在步骤②中的作用是 .
(1)、上述步骤③中“物质M”的化学式为 , 其与碘化钾反应的化学方程式是 .(2)、步骤③中“X操作”是;该操作与步骤①中的操作都要用到除烧杯外的另一种玻璃仪器,它是 , 它在步骤②中的作用是 .四、实验题
-
22. 现有下列实验装置示意图,结合实验装置图回答有关问题.
 (1)、A装置中a仪器的名称是 .(2)、选用A或B装置都能制备的气体是 , 用A装置制取该气体的化学反应方程式是 , 收集该气体可选用的装置为(填序号,答出一种即可) .(3)、用B装置还可以制取气体,制取该气体时,在锥形瓶加入的是 , 在分液漏斗中加入;检验D装置收集满该气体的方法是 .(4)、现有如下资料:
(1)、A装置中a仪器的名称是 .(2)、选用A或B装置都能制备的气体是 , 用A装置制取该气体的化学反应方程式是 , 收集该气体可选用的装置为(填序号,答出一种即可) .(3)、用B装置还可以制取气体,制取该气体时,在锥形瓶加入的是 , 在分液漏斗中加入;检验D装置收集满该气体的方法是 .(4)、现有如下资料:通常状况下,NO2是一种密度比空气大的有毒气体,能与水发生反应;NO2能与碱溶液反应生成盐和水.实验室制取少量NO2气体的方法:废铜和浓硝酸反应,生成硝酸铜、水和NO2气体.制取NO2的反应方程式为 .
①制取NO2的发生装置是(填编号);
②若用F装置来收集NO2 , 气体应从接口(填序号,下同)处进入集气瓶,从环保的角度考虑,在制取NO2时你认为在装置F后连接的装置是 .
23. 同学们在学习碱的化学性质时,做了如图所示的甲乙两个实验. (1)、写出乙实验的化学反应方程式: , 反应过程中产生的现象是 .(2)、实验结束后,甲、乙两个同学将废液倒入实验室的废液缸,结果发现废液浑
(1)、写出乙实验的化学反应方程式: , 反应过程中产生的现象是 .(2)、实验结束后,甲、乙两个同学将废液倒入实验室的废液缸,结果发现废液浑浊并呈红色,他们产生了疑问.
【提出问题】废液中含有哪些物质?
【交流讨论】废液中一定含有的碳酸钙、指示剂水和氯化钠,此外还含有能使废液呈碱性的物质能使废液呈碱性的物质是什么?同学们有如下猜想:
小云认为:只有碳酸钠;
小红认为:只有氢氧化钙;
小林认为:是氢氧化钠和碳酸钠.
你认为还可能是 . (写一种猜想)
(3)、【实验设计】小方想用氯化钙溶液来验证小云、小红、小林的猜想.查阅资料获悉氯化钙溶液呈中性,设计如下实验.请你将小方的实验设计补充完整.实验内容
预计现象
预计结论
取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置.
①有白色沉淀,溶液呈红色.
的猜想正确.
②
小云的猜想正确.
③
小红的猜想正确.
【反思拓展】在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑 .
五、综合计算
-
24. 苹果酸(化学式为C4H6O5)是苹果醋中的主要成分,具有解毒、降脂等药效.请问:(1)、苹果酸由种元素组成,苹果酸中元素的质量分数最大.(2)、苹果酸属于(选填“有机物”或“无机物”).(3)、苹果酸的相对分子质量是 .25. 某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.(1)、配制溶液:
①配制200g 8%的氢氧化钠溶液,需水的体积为 mL(水的密度近似看作1g/cm3).
②称量时先调节托盘天平平衡,将一只烧杯放在托盘天平的盘,称量其质量.然后(按操作的先后顺序选填字母),直至天平平衡.
A.将氢氧化钠固体加入烧杯中 B.按需要添加砝码、移动游码
③加水充分溶解,并冷却至室温(约20℃).
(2)、如图表示用上述配制的氢氧化钠溶液与20g某稀盐酸发生反应过程中,使用数字传感仪测得溶液温度变化的曲线.①当加入15g氢氧化钠溶液时,所得溶液中的溶质为(用化学式表示).
②加入 g氢氧化钠溶液,恰好完全中和.
③试计算此盐酸的溶质质量分数.(写出计算过程)
