江苏省扬州市江都区2017-2018学年九年级上学期化学期末考试试卷
试卷更新日期:2019-09-27 类型:期末考试
一、单选题
-
1. 十九大报告提出建设“美丽中国”。下列做法中不符合此主题的是()A、支付宝蚂蚁森林,在沙漠植树 B、关闭所有化工厂,减少环境污染 C、城市出行骑共享单车,节能减排 D、垃圾分类处理,变废为宝2. 下列物质属于纯净物的是()A、液氮 B、青铜 C、盐水 D、磁铁矿3. 地壳中含量最多的金属元素的是()A、Fe B、Si C、O D、Al4. 下列为“节约用水”标志的是()A、
 B、
B、 C、
C、 D、
D、 5. 下列物质由分子构成的是()A、石墨 B、氯化钠 C、蒸馏水 D、镁6. 煤油中含有噻吩(用X表示),噻吩令人不愉快的气味,其燃烧时发生反应的化学方程式表示为:X+6O2 4CO2+SO2+2H2O,则噻吩的化学式为()A、C4H6S B、C4H4S C、C4H4S2 D、C8H8S7. 下列生活中常见物质与水混合,能形成溶液的是( )A、牙膏 B、蔗糖 C、面粉 D、豆油8. 下列实验操作中,正确的是( )A、
5. 下列物质由分子构成的是()A、石墨 B、氯化钠 C、蒸馏水 D、镁6. 煤油中含有噻吩(用X表示),噻吩令人不愉快的气味,其燃烧时发生反应的化学方程式表示为:X+6O2 4CO2+SO2+2H2O,则噻吩的化学式为()A、C4H6S B、C4H4S C、C4H4S2 D、C8H8S7. 下列生活中常见物质与水混合,能形成溶液的是( )A、牙膏 B、蔗糖 C、面粉 D、豆油8. 下列实验操作中,正确的是( )A、 滴加试剂
B、
滴加试剂
B、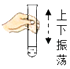 振荡试管
C、
振荡试管
C、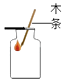 氧气验满
D、
氧气验满
D、 测酸碱度
9. 下列有关实验现象的描述,正确的是()A、镁条在空气中燃烧发出耀眼的白光,生成白色的氧化镁 B、红磷在空气中燃烧产生大量白雾 C、二氧化碳遇到湿润的蓝色石蕊试纸,试纸变红 D、铁与稀硫酸反应有气泡产生,溶液由无色变为黄色10. 已知部分农作物适宜生长的pH如表所示:
测酸碱度
9. 下列有关实验现象的描述,正确的是()A、镁条在空气中燃烧发出耀眼的白光,生成白色的氧化镁 B、红磷在空气中燃烧产生大量白雾 C、二氧化碳遇到湿润的蓝色石蕊试纸,试纸变红 D、铁与稀硫酸反应有气泡产生,溶液由无色变为黄色10. 已知部分农作物适宜生长的pH如表所示:农作物
油菜
水稻
茶树
甘草
适宜生长的pH
5.8﹣6.7
6.0﹣7.0
5.0﹣5.5
7.2﹣8.5
经检测,邵阳地区的土壤呈弱酸性,在邵阳地区不适宜种植的农作物是( )
A、油菜 B、水稻 C、茶树 D、甘草11. 全球近140个国家将在2020年前禁止生产和出口含汞产品,如荧光灯、化妆品、血压计等。关于汞元素的相关信息正确的是()
 A、汞是非金属元素 B、汞的相对原子质量为200.6g C、汞原子的质子数是80 D、汞元素是人体必需微量元素12. 下列实验事实不能作为相应观点的证据是()
A、汞是非金属元素 B、汞的相对原子质量为200.6g C、汞原子的质子数是80 D、汞元素是人体必需微量元素12. 下列实验事实不能作为相应观点的证据是()选项
实验事实
观点
A
电解水生成氢气和氧气
水由氢元素、氧元素组成
B
洗洁精洗去餐具上的油污
乳化作用
C
少量白糖加入水中,不久“消失”
微粒是不断运动的
D
“干冰升华”
分子的体积增大
A、A B、B C、C D、D13. 目前,许多烧烤店都改用机制炭作燃料,引燃机制炭可以使用固体酒精,盖灭机制炭可以使用炭灰,下列有关说法错误的是() A、酒精的燃烧会升高机制炭的着火点 B、炭灰可以隔绝空气而使机制炭熄灭 C、酒精的着火点低于机制炭 D、机制炭做成空心可以增大与空气的接触面积14. 下列说法中正确的是()A、铁制品在潮湿的空气中不易生锈 B、“真金不怕火炼”说明黄金的熔点高 C、铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀 D、生铁和钢的性能不同主要是因为二者含碳量不同15. 医院输液常用溶质质量分数为 5%的葡萄糖(C6H12O6)溶液为病人补充能量。 下列说法正确的是()A、葡萄糖由碳原子、氢原子和氧原子构成 B、葡萄糖由C,H,O 三种元素组成 C、葡萄糖中碳元素质量分数大于氧元素 D、葡萄糖中碳、氢和氧三种元素的质量比为 6:12:616. 下列化学方程式书写完全正确的是()A、C+O2=CO2 B、NaOH+CuSO4=Cu(OH)2↓+Na2SO4 C、2H2O 2H2↑+O2↑ D、Al+O2=Al2O317. 下表列出了除去物质中所含少量杂质的方法,其中正确的是()
A、酒精的燃烧会升高机制炭的着火点 B、炭灰可以隔绝空气而使机制炭熄灭 C、酒精的着火点低于机制炭 D、机制炭做成空心可以增大与空气的接触面积14. 下列说法中正确的是()A、铁制品在潮湿的空气中不易生锈 B、“真金不怕火炼”说明黄金的熔点高 C、铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀 D、生铁和钢的性能不同主要是因为二者含碳量不同15. 医院输液常用溶质质量分数为 5%的葡萄糖(C6H12O6)溶液为病人补充能量。 下列说法正确的是()A、葡萄糖由碳原子、氢原子和氧原子构成 B、葡萄糖由C,H,O 三种元素组成 C、葡萄糖中碳元素质量分数大于氧元素 D、葡萄糖中碳、氢和氧三种元素的质量比为 6:12:616. 下列化学方程式书写完全正确的是()A、C+O2=CO2 B、NaOH+CuSO4=Cu(OH)2↓+Na2SO4 C、2H2O 2H2↑+O2↑ D、Al+O2=Al2O317. 下表列出了除去物质中所含少量杂质的方法,其中正确的是()选项
物质
所含杂质
除去杂质的方法
A
MnO2
KCl
加水溶解、过滤、蒸发结晶
B
CO2
CO
将混合气体点燃
C
Cu
C
在氧气中灼烧
D
FeCl2溶液
CuCl2
加入过量的铁粉,过滤
A、A B、B C、C D、D18. 下图为实验室模拟炼铁,现将agFe2O3在高温下与足量CO反应,实验结束后测得B中产生6.00g白色沉淀,下列说法正确的是() A、实验开始应该先打开弹簧夹① B、该实验过程中共消耗1.68gCO C、氧化铁质量为3.2g D、硬质玻璃管中固体由黑色变为红色
A、实验开始应该先打开弹簧夹① B、该实验过程中共消耗1.68gCO C、氧化铁质量为3.2g D、硬质玻璃管中固体由黑色变为红色二、多选题
-
19. 在点燃条件下,A和B反应生成C和D。反应前后分子变化的微观示意图如下所示。下列说法中正确的是()
 A、该反应前后原子和分子种类均不变 B、该反应属于置换反应 C、A中氮元素的化合价为-3价 D、参加反应的A和B的质量比为17∶3220. 按如图所示装置,将液体x注入装有固体y的试管中,会导致U形管中右端液面升高。则x、y可能是()
A、该反应前后原子和分子种类均不变 B、该反应属于置换反应 C、A中氮元素的化合价为-3价 D、参加反应的A和B的质量比为17∶3220. 按如图所示装置,将液体x注入装有固体y的试管中,会导致U形管中右端液面升高。则x、y可能是() A、稀盐酸 镁 B、水 硝酸铵 C、水 氯化钠 D、水 氢氧化钠
A、稀盐酸 镁 B、水 硝酸铵 C、水 氯化钠 D、水 氢氧化钠三、填空题
-
21. 化学语言包括文字语言、符号语言等:(1)、用相应的化学符号填空:
①2个铜原子; ②氨气分子;
③二氧化氮; ④人体缺少元素,会导致甲状腺疾病;
⑤碳酸根离子; ⑥氧化镁中镁元素的化合价;
(2)、写出下列反应的化学方程式:①红磷燃烧; ②有水参与的化合反应。
22. 化学就在我们身边,它能改善我们的生活。请从“A.二氧化碳 B.碳酸氢铵 C. 武德合金 D.氢气 E.金刚石 ”中选择相应物质的字母填空。(1)、可制作保险丝的物质是;(2)、植物光合作用的原料之一;(3)、农业上用作化肥的是;(4)、能作为绿色能源的单质是;(5)、自然界中最硬的物质是。23. 化学与我们的生活息息相关。 (1)、为延长食品保质期,常采用真空包装或者充气包装,其目的主要是让食品与隔绝。充入食品包装袋中的气体最可能是下列气体中的。
(1)、为延长食品保质期,常采用真空包装或者充气包装,其目的主要是让食品与隔绝。充入食品包装袋中的气体最可能是下列气体中的。A.氢气
B.氮气
C.一氧化碳
D.氨气
(2)、生活中,常用鉴别硬水和软水,活性炭在净水器中能起到过滤和的作用。(3)、目前,广泛使用的手机锂电池负极材料大多采用石墨材料,利用其性。正极方面多是钴酸锂(LiCoO2),钴酸锂中锂元素的化合价为+1,则钴元素的化合价为。(4)、“共享汽车”是指许多人合用一辆车。
①“共享汽车”的行李箱盖是镁铝合金,现将镁铝合金与铝片相互刻画,在铝片表面留下明显划痕,说明镁铝合金的硬度铝的硬度(填“大于”或“小于”)
②相较于私家车而言,使用“共享汽车”出行的好处有(填序号)
A.降低出行成本
B.减少汽车尾气排放
C.节约能源
D.降低交通压力
③“共享汽车”使用天然气作为燃料,其主要成分是甲烷(CH4),CH4中H的质量分数为 , CH4燃烧的化学方程式是 , 该过程主要是将化学能转化为能。
(5)、图为KNO3 和NaCl两种物质的溶解度曲线图。
①t1℃时,两种物质溶解度的大小关系:NaClKNO3(填“>”或“=”或“<”)。
②t2℃时,将25g氯化钠固体投入50g水中,充分溶解后可得NaCl溶液(填“不饱和”或“饱和”或“不能确定”)。
③将饱和KNO3溶液变为不饱和KNO3溶液,可行的方法之一是添加溶剂(水),还可以是。
④将t2℃时饱和的KNO3溶液100g恒温蒸发10g水,可析出KNO3g,剩下的溶液中溶质的质量分数为(结果保留一位小数)。
四、实验题
-
24. 下图为实验室常用的实验装置,回答问题:
 (1)、标号仪器的名称:①;②。(2)、A、E组合制氧气,制取氧气的化学方程式是 , 氧气收集完毕,应先(填“熄灭酒精灯”或“从水中取出导气管”)。(3)、用B制取二氧化碳的化学反应方程式是。如果用右图所示装置(固定仪器省略)来做发生装置,检查该装置气密性的方法是。实验时,应该将块状石灰石放在仪器中(填字母),该装置的主要优点是。
(1)、标号仪器的名称:①;②。(2)、A、E组合制氧气,制取氧气的化学方程式是 , 氧气收集完毕,应先(填“熄灭酒精灯”或“从水中取出导气管”)。(3)、用B制取二氧化碳的化学反应方程式是。如果用右图所示装置(固定仪器省略)来做发生装置,检查该装置气密性的方法是。实验时,应该将块状石灰石放在仪器中(填字母),该装置的主要优点是。
五、流程题
-
25. 废铁屑的主要成分是铁,同时还有少量铁锈(主要成分是Fe2O3)等杂质,动物饲料硫酸亚铁的生产工艺之一如下图所示:
 (1)、实验室欲用98%的浓硫酸(密度为1.84g/mL)配制200g20%的稀硫酸,有以下实验步骤:a.量取;b.计算;c.稀释;d.装瓶贴标签。正确的顺序是 (填字母),若用量筒量取浓硫酸时俯视读数,其它操作正确,则所得溶液的质量分数20%(填“>”、“<”或“=”)。(2)、在反应器中发生的化学反应①Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;②Fe2(SO4)3+Fe=3FeSO4;③。反应器所在的厂房要严禁烟火、加强通风的原因是。(3)、溶液A中的溶质是(填化学式)。(4)、操作Ⅰ的名称是 , 完成操作Ⅰ的玻璃仪器有:玻璃棒、烧杯和 , 玻璃棒的作用。(5)、经过操作Ⅱ:、降温结晶、过滤、冰水洗涤、低温干燥可得硫酸亚铁晶体(FeSO4•7H2O),用低温干燥说明硫酸亚铁晶体可能具有的性质是。(6)、将无水硫酸亚铁(FeSO4)隔绝空气加强热,生成Fe2O3 和SO2、SO3两种气体,试写出该反应的化学方程式。
(1)、实验室欲用98%的浓硫酸(密度为1.84g/mL)配制200g20%的稀硫酸,有以下实验步骤:a.量取;b.计算;c.稀释;d.装瓶贴标签。正确的顺序是 (填字母),若用量筒量取浓硫酸时俯视读数,其它操作正确,则所得溶液的质量分数20%(填“>”、“<”或“=”)。(2)、在反应器中发生的化学反应①Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;②Fe2(SO4)3+Fe=3FeSO4;③。反应器所在的厂房要严禁烟火、加强通风的原因是。(3)、溶液A中的溶质是(填化学式)。(4)、操作Ⅰ的名称是 , 完成操作Ⅰ的玻璃仪器有:玻璃棒、烧杯和 , 玻璃棒的作用。(5)、经过操作Ⅱ:、降温结晶、过滤、冰水洗涤、低温干燥可得硫酸亚铁晶体(FeSO4•7H2O),用低温干燥说明硫酸亚铁晶体可能具有的性质是。(6)、将无水硫酸亚铁(FeSO4)隔绝空气加强热,生成Fe2O3 和SO2、SO3两种气体,试写出该反应的化学方程式。六、综合题
-
26. 2018年1月11日,广西某地高速公路大桥上用于融冰作业的2包共100公斤含有亚硝酸钠的工业盐遗失,当地迅速组织警力开展搜寻遗失的工业盐,确保不流入市场和家庭。
(资料卡1)亚硝酸钠与食盐氯化钠相似,为白色有咸味的固体,但误食会使人中毒。腌制食品、泡菜等制作过程中会产生亚硝酸钠。
根据以上资料,回答下列问题:
(1)、用盐融冰的原理是 , 该过程主要发生的是(填“物理变化”或“化学变化”)。(2)、下图是用不同浓度盐水腌制泡菜过程中亚硝酸盐含量测定曲线图。据此回答:当盐水浓度为6%时,第天亚硝酸盐含量达到最大值。为了安全,泡菜腌制时盐水浓度最好是并在腌制天后再食用。 (3)、兴趣小组欲测定某工业盐中亚硝酸钠的质量分数
(3)、兴趣小组欲测定某工业盐中亚硝酸钠的质量分数(资料卡2)实验室常用亚硝酸钠与氯化铵溶液反应制取纯净的氮气,其化学方程式为:NaNO2+NH4Cl NaCl+N2↑+2H2O(此反应是放热反应)
(资料卡3)在酸性环境中高锰酸钾能与亚硝酸钠发生如下反应:2KMnO4+5NaNO2+3H2SO4=K2SO4+2MnSO4+5NaNO3+3H2O
(方案一)取1g该工业盐样品与足量氯化铵溶液于如图装置中充分反应(该工业盐中其他成分不与氯化铵溶液反应),实验时加热片刻后,即可移去酒精灯,其原因。最终量筒中收集到300mL水,已知该条件下氮气的密度为1.25g/L,则该工业盐样品中亚硝酸钠的质量分数为(写出计算过程,结果保留一位小数,)。

实验结束后发现测量结果偏大,可能原因是。
(方案二)为更准确地测定该工业盐中亚硝酸钠的含量,称取4.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用含量为15.8g/L的酸性KMnO4溶液进行反应,实验所得数据如下表所示:
实验次序
1
2
3
4
KMnO4溶液体积(mL)
20.60
20.02
20.00
19.98
上述第次实验所得数据明显异常,剔除异常数据后,计算出该工业盐中亚硝酸钠的质量分数为。
-
-