江苏省连云港市2018-2019学年九年级上学期化学期末考试试卷
试卷更新日期:2019-09-27 类型:期末考试
一、单选题
-
1. 下列变化属于化学变化的是()A、粗盐溶解在水中后沉降沙子 B、饱和硝酸钾溶液降温后析出晶体 C、食盐水蒸干后出现固体 D、澄清石灰水在空气中敞口放置后表面形成一层白膜2. 实验结束后,图中仪器的处理方式正确的是( )A、
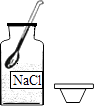 B、
B、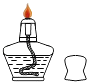 C、
C、 D、
D、 3. 下列对分子、原子的认识,正确的是()A、水降温结冰,水分子运动速率减慢 B、在化学变化中任何粒子都不可分 C、水和氯化钠都是由分子构成的 D、碘升华是因为碘分子的体积随温度的升高而变大4. 科学研究发现:金星大气层的成分之一是三氧化二碳(C2O3),实验证明三氧化二碳的化学性质与一氧化碳相似。下列关于三氧化二碳的说法中,正确的是()A、C2O3能使澄清石灰水变浑浊 B、C2O3在O2中充分燃烧的产物为CO2 C、C2O3在任何条件下都不能还原氧化铜 D、C2O3中碳的化合价为+4价5. “酒驾”已经写入刑法。有人吃荔枝或者榴莲等水果也会被查“酒驾”,因为水果中含糖分,在无氧环境下,水果也会呼吸,这个过程会产生酒精和二氧化碳,人吃了以后短时间内嘴里可能含有酒精余量。交警常用一种“酒精检测仪”检测司机是否酒后驾车。其反应原理为 ,这X的化学式为()A、 B、 C、 D、6. 蜡烛(足量)在密闭容器内燃烧至熄灭,用仪器测出瓶内氧气含量的变化如图乙所示,下列判断正确的是()
3. 下列对分子、原子的认识,正确的是()A、水降温结冰,水分子运动速率减慢 B、在化学变化中任何粒子都不可分 C、水和氯化钠都是由分子构成的 D、碘升华是因为碘分子的体积随温度的升高而变大4. 科学研究发现:金星大气层的成分之一是三氧化二碳(C2O3),实验证明三氧化二碳的化学性质与一氧化碳相似。下列关于三氧化二碳的说法中,正确的是()A、C2O3能使澄清石灰水变浑浊 B、C2O3在O2中充分燃烧的产物为CO2 C、C2O3在任何条件下都不能还原氧化铜 D、C2O3中碳的化合价为+4价5. “酒驾”已经写入刑法。有人吃荔枝或者榴莲等水果也会被查“酒驾”,因为水果中含糖分,在无氧环境下,水果也会呼吸,这个过程会产生酒精和二氧化碳,人吃了以后短时间内嘴里可能含有酒精余量。交警常用一种“酒精检测仪”检测司机是否酒后驾车。其反应原理为 ,这X的化学式为()A、 B、 C、 D、6. 蜡烛(足量)在密闭容器内燃烧至熄灭,用仪器测出瓶内氧气含量的变化如图乙所示,下列判断正确的是()图1
 图2
图2  A、蜡烛燃烧前瓶内只有氧气 B、瓶内物质总质量不断减少 C、蜡烛熄灭后瓶内只剩二氧化碳气体 D、氧气浓度小于一定值时,蜡烛无法燃烧7. 随着工业化进程的深入,大量温室气体的排出,导致全球气温升高、气候发生变化。现在大力提倡“低碳生活”(low﹣carbon life ),下列不属于“低碳生活”方式的是( )A、多使用布制储物袋购物,尽量少使用塑料袋 B、多使用煤炉进行冬季取暖,尽量少用其他方式取暖 C、多步行,骑自行车,尽量选用公共汽车出行,少开车 D、多用永久性的筷子、饭盒,尽量避免使用一次性的餐具8. 把粗铁丝放入 溶液中,铁丝表面覆盖了红色物质,一会儿又有气泡冒出。同学们对“放出气体”这一异常现象进行猜想、实验。其中没有价值的是()A、小赵同学推测气体可能是氢气并检验 B、小钱同学推测气体可能是氨气 并检验 C、小孙同学推测 溶液中可能混有盐酸并测定 D、小李同学推测试剂可能变质或被污染,更换后在实验9. 如图是某反应的微观示意图,下列说法正确的是( )
A、蜡烛燃烧前瓶内只有氧气 B、瓶内物质总质量不断减少 C、蜡烛熄灭后瓶内只剩二氧化碳气体 D、氧气浓度小于一定值时,蜡烛无法燃烧7. 随着工业化进程的深入,大量温室气体的排出,导致全球气温升高、气候发生变化。现在大力提倡“低碳生活”(low﹣carbon life ),下列不属于“低碳生活”方式的是( )A、多使用布制储物袋购物,尽量少使用塑料袋 B、多使用煤炉进行冬季取暖,尽量少用其他方式取暖 C、多步行,骑自行车,尽量选用公共汽车出行,少开车 D、多用永久性的筷子、饭盒,尽量避免使用一次性的餐具8. 把粗铁丝放入 溶液中,铁丝表面覆盖了红色物质,一会儿又有气泡冒出。同学们对“放出气体”这一异常现象进行猜想、实验。其中没有价值的是()A、小赵同学推测气体可能是氢气并检验 B、小钱同学推测气体可能是氨气 并检验 C、小孙同学推测 溶液中可能混有盐酸并测定 D、小李同学推测试剂可能变质或被污染,更换后在实验9. 如图是某反应的微观示意图,下列说法正确的是( ) A、该反应生成物中有单质 B、该反应属于化合反应 C、反应前后分子数目没有发生改变 D、反应前甲、乙两种分子的个数比是1:210. 下列说法符合图中漫画情景的是()
A、该反应生成物中有单质 B、该反应属于化合反应 C、反应前后分子数目没有发生改变 D、反应前甲、乙两种分子的个数比是1:210. 下列说法符合图中漫画情景的是() A、此反应可能是分解反应 B、若金属1是锌,金属2可能是银 C、此反应可能是Cu+2AgCl= 2Ag+CuCl2 D、比较铁和铜的活动性强弱可以用硫酸镁溶液11. 四种物质在一定的条件下充分混合反应,测得反应前后各物质的质量分数如下图所示。则有关说法中错误的()
A、此反应可能是分解反应 B、若金属1是锌,金属2可能是银 C、此反应可能是Cu+2AgCl= 2Ag+CuCl2 D、比较铁和铜的活动性强弱可以用硫酸镁溶液11. 四种物质在一定的条件下充分混合反应,测得反应前后各物质的质量分数如下图所示。则有关说法中错误的() A、丁一定是化合物 B、参加反应的丁的质量一定等于生成甲和丙的质量之和 C、该反应是过氧化氢的分解反应 D、乙可能是这个反应的催化剂12. 进行“一定溶质质量分数的氯化钠溶液的配置”实验活动常出现以下不符合题意操作,其中不影响所配溶液浓度的是()A、称量固体时,氯化钠放在右盘 B、固体转移到烧杯时,氯化钠洒出 C、量取液体时,俯视读数 D、配好的溶液装瓶是,将溶液溅出
A、丁一定是化合物 B、参加反应的丁的质量一定等于生成甲和丙的质量之和 C、该反应是过氧化氢的分解反应 D、乙可能是这个反应的催化剂12. 进行“一定溶质质量分数的氯化钠溶液的配置”实验活动常出现以下不符合题意操作,其中不影响所配溶液浓度的是()A、称量固体时,氯化钠放在右盘 B、固体转移到烧杯时,氯化钠洒出 C、量取液体时,俯视读数 D、配好的溶液装瓶是,将溶液溅出二、填空题
-
13. 用化学符号或化学方程式填空:(1)、2个硝酸根离子;(2)、2个氮气分子;(3)、2个亚铁离子;(4)、+2价的钙元素;(5)、可以做食品袋中干燥剂的物质化学式:;(6)、乙醇(俗称酒精)燃烧的化学方程式:;(7)、有CO2生成的化合反应的化学方程式:;(8)、有CO2生成的置换反应的化学方程式:。14. KNO3和KCl在不同温度时的溶解度如表所示。请回答下列问题:
温度/℃
0
10
20
30
40
50
60
70
KNO3
13.3
20.9
31.6
45.8
63.9
85.5
110
138
KCl
27.6
31.0
34.0
37.0
40.0
42.6
45.5
48.3
(1)、依据上表数据,绘制KNO3和KCl的溶解度曲线,如图1中能表示KNO3溶解度曲线的是(填m或n)。图1
 图2
图2  (2)、小王同学想将80 ℃时的KCl饱和溶液变为不饱和溶液,可以采取的方法是(写出其中一种)。(3)、20℃时,向10 g 水中加入2.5gKNO3充分搅拌得到X,再加入2.5gKNO3充分搅拌得到Y,继续升温至50℃得到Z,则X、Y、Z中为饱和溶液的是。(4)、40℃时,100g水中溶解gKCl恰好饱和;若将该饱和溶液稀释成溶质质量分数为10%的溶液,应加水g。(5)、如图2所示,20℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是下列中的__________(填字母序号)。A、硝酸铵固体 B、生石灰固体 C、冰块
(2)、小王同学想将80 ℃时的KCl饱和溶液变为不饱和溶液,可以采取的方法是(写出其中一种)。(3)、20℃时,向10 g 水中加入2.5gKNO3充分搅拌得到X,再加入2.5gKNO3充分搅拌得到Y,继续升温至50℃得到Z,则X、Y、Z中为饱和溶液的是。(4)、40℃时,100g水中溶解gKCl恰好饱和;若将该饱和溶液稀释成溶质质量分数为10%的溶液,应加水g。(5)、如图2所示,20℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出。加入的物质可能是下列中的__________(填字母序号)。A、硝酸铵固体 B、生石灰固体 C、冰块三、推断题
-
15. 已知A,B,C,D是初中化学常见物质,它们之间的转化关系如图所示。其中B、C是组成元素相同的气体,A是目前世界年产量最高的金属,D是黑色固体,请回答
 (1)、写出A、D的化学式:A , D。(2)、B在工业上常用来冶炼A,写出其反应的化学方程式 , 在这个反应中,发生了反应。
(1)、写出A、D的化学式:A , D。(2)、B在工业上常用来冶炼A,写出其反应的化学方程式 , 在这个反应中,发生了反应。四、实验题
-
16. 小明设计了如下气体制取与性质验证的组合装置。打开分液漏斗活塞,放出一定量过氧化氢溶液,关上活塞,A中出现大量气泡。请看图回答下列问题:
 (1)、A中发生反应的化学方程式为;(2)、B中实验现象是;原因是;(3)、C中实验现象是;(4)、E中实验现象是 , E中发生反应的化学方程式为;(5)、用F装置收集气体的依据是;(6)、若将A与F直接相连,证明F中已集满气体的方法是。
(1)、A中发生反应的化学方程式为;(2)、B中实验现象是;原因是;(3)、C中实验现象是;(4)、E中实验现象是 , E中发生反应的化学方程式为;(5)、用F装置收集气体的依据是;(6)、若将A与F直接相连,证明F中已集满气体的方法是。五、科学探究题
-
17. 空气中氧气含量测定的再认识。
图①
 图②
图② 
(实验回顾)实验室常用红磷燃烧的方法测定空气中氧气的含量。在老师的指导下,小明分别用过量的红磷和白磷进行该实验,用测氧气浓度的传感器测得反应后装置内氧气浓度分别为8.85%和3.21%。请从燃烧条件的角度回答产生上述结果的主要原因:。
(实验探究1)小明根据铁生锈的原理,探究用铁能否准确测定空气中氧气的含量。于是进行了实验(装置如图①)。通过7天测得的数据计算出空气中氧气的含量为19.13%。
(交流与反思)与用红磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点是 .
(实验探究2)为了加快反应速率,小明通过查阅资料,林勇铁粉、碳粉、氯化钠等物质又进行了实验(装置如图②)。8分钟后测得的数据如下表:
测量项目
实验前
实验后
集气瓶(扣除内容物)和导管的容积
烧杯中的水的体积
烧杯中剩余水的体积
体积/mL
126.0
80.0
54.5
请计算出空气中氧气含量(计算结果保留一位小数)。
(结论与反思)通过上述实验探究,选择(填物质名称)进行实验可较为快速地完成实验并减小实验误差。
(拓展延伸)铜也能与空气中氧气、水、二氧化碳反应二锈蚀,生成铜绿(铜绿主要成分为 )。若将图①装置中的粗铁丝换成足量的铜丝进行实验,请判断能否比较准确地测定空气中氧气的含量 , 并说明理由。
六、计算题
-
18. 化学兴趣小组为测定某石灰石样品中碳酸钙的质量分数,取26g石灰石样品放在烧杯中,然后向其中逐渐加入90g稀盐酸,使之与样品充分反应(杂质不参加反应),加入稀盐酸的质量与生成气体的质量关系如图所示请计算:
 (1)、反应生成气体的质量g。(2)、样品中碳酸钙的质量分数。(结果保留到0.1%)。
(1)、反应生成气体的质量g。(2)、样品中碳酸钙的质量分数。(结果保留到0.1%)。
-
-
-