北京市丰台区2018-2019学年高二上学期化学期中考试试卷
试卷更新日期:2019-09-24 类型:期中考试
一、单选题
-
1. 下列有机化合物的分类错误的是( )
A
B
C
D




苯的同系物
芳香化合物
烯烃
醇
A、A B、B C、C D、D2. 可以准确判断有机化合物含有哪些官能团的分析方法是( )A、李比希燃烧法 B、红外光谱法 C、质谱法 D、核磁共振氢谱法3. 下列有关化学用语表示正确的是( )A、乙烷的实验式C2H6 B、乙醇的结构式CH3CH2OH C、羟基电子式 D、1,3-丁二烯的分子式:C4H8
4. 下列各组混合物中能用分液漏斗进行分离的是( )A、乙醇和水 B、苯和甲苯 C、溴乙烷和水 D、乙醇和乙酸5. 下列有机物的命名正确的是( )A、3-甲基2-乙基戊烷 B、2,3,3-三甲基丁烷 C、2-甲基-3-丁炔 D、3, 3 -二甲基 -1- 丁烯6. 四种常见有机物的比例模型如下图。下列说法正确的是( )
D、1,3-丁二烯的分子式:C4H8
4. 下列各组混合物中能用分液漏斗进行分离的是( )A、乙醇和水 B、苯和甲苯 C、溴乙烷和水 D、乙醇和乙酸5. 下列有机物的命名正确的是( )A、3-甲基2-乙基戊烷 B、2,3,3-三甲基丁烷 C、2-甲基-3-丁炔 D、3, 3 -二甲基 -1- 丁烯6. 四种常见有机物的比例模型如下图。下列说法正确的是( ) A、乙可与溴水发生取代反应而使溴水褪色 B、甲能使酸性KMnO4溶液褪色 C、丙中的碳碳键是介于碳碳单键和碳碳双键之间的特殊的键 D、丁为醋酸分子的比例模型7. 含有一个叁键的炔烃,氢化后的结构简式如下,此炔烃可能有的结构式有( )
A、乙可与溴水发生取代反应而使溴水褪色 B、甲能使酸性KMnO4溶液褪色 C、丙中的碳碳键是介于碳碳单键和碳碳双键之间的特殊的键 D、丁为醋酸分子的比例模型7. 含有一个叁键的炔烃,氢化后的结构简式如下,此炔烃可能有的结构式有( ) A、1种 B、2种 C、3种 D、4种8. 下列物质中,沸点最高的是( )A、乙烷 B、乙醇 C、乙二醇 D、丙三醇9. 除去下列物质中的少量杂质(括号内),选用的试剂和分离方法不能达到实验目的的是( )
A、1种 B、2种 C、3种 D、4种8. 下列物质中,沸点最高的是( )A、乙烷 B、乙醇 C、乙二醇 D、丙三醇9. 除去下列物质中的少量杂质(括号内),选用的试剂和分离方法不能达到实验目的的是( )混合物
试剂
分离方法
A
粗苯甲酸(泥沙等)
水
重结晶
B
乙酸乙酯(乙酸)
饱和碳酸钠溶液
分液
C
乙炔(硫化氢)
硫酸铜溶液
洗气
D
苯(苯酚)
溴水
过滤
A、A B、B C、C D、D10. 1 mol某气态烃能与1 mol氯化氢发生加成反应,加成后的产物又可与7 mol氯气发生完全的取代反应,则该烃的结构简式为( )A、CH2=CH2 B、CH3CH=CH2 C、.CH3CH2CH=CH2 D、CH3CH2CH2CH=CH211. 若丙醇中氧原子为18O,它和乙酸反应生成酯的相对分子质量是( )A、100 B、104 C、120 D、12212. 用核磁共振仪对分子式为C3H8O的有机物进行分析,核磁共振氢谱有三个峰,峰面积之比是1:1:6,则该化合物的结构简式为( )A、CH3-O-CH2-CH3 B、CH3CH(OH)CH3 C、CH3CH2CH2OH D、C3H7OH13. 下列烃中,一卤代物的同分异构体的数目最多的是( )A、乙烷 B、2-甲基丙烷 C、2,2-二甲基丙烷 D、2,2-二甲基丁烷14. “绿色化学”对化学反应提出了“原子经济性”(原子节约)的新概念及要求,理想原子经济性反应是原料分子中的原子全部转化成所需要的产物,实现零排放。下列反应类型一定符合这一要求的是( )
(1)(取代反应 (2)加成反应 (3)消去反应 (4)水解反应 (5)酯化反应 (6)氧化反应A、(2) B、(1)(4) C、(3)(5) D、(2)(6)15. 为了鉴定溴乙烷中卤素原子的存在,以下各步实验:①加入AgNO3溶液②加热③用HNO3酸化溶液④加入NaOH水溶液,其中操作顺序合理的是( )A、④②③① B、①②③④ C、④①③② D、④①②③16. 分子式为C4H8的烯烃共有(要考虑顺反异构)( )A、3种 B、4种 C、5种 D、6种17. 十九大报告提出将我国建设成为制造强国,2020年我国“PX”产能将达到3496万吨/年。有机物(烃)“PX”的结构模型如下图,下列说法错误的是( ) A、“PX”的分子式为C8H10 B、“PX”的二氯代物共有6种(不考虑立体异构) C、“PX”分子中,最多有14个原子共面 D、可用酸性KMnO4溶液鉴别“PX”与苯18. 可用于鉴别乙醇、甲酸、乙醛、乙酸4种无色液体的一种试剂是( )A、水 B、新制Cu(OH)2 C、NaOH溶液 D、石蕊试剂19. 下列各物质中既能发生消去反应又能发生催化氧化反应,并且催化氧化的产物为醛的是( )A、
A、“PX”的分子式为C8H10 B、“PX”的二氯代物共有6种(不考虑立体异构) C、“PX”分子中,最多有14个原子共面 D、可用酸性KMnO4溶液鉴别“PX”与苯18. 可用于鉴别乙醇、甲酸、乙醛、乙酸4种无色液体的一种试剂是( )A、水 B、新制Cu(OH)2 C、NaOH溶液 D、石蕊试剂19. 下列各物质中既能发生消去反应又能发生催化氧化反应,并且催化氧化的产物为醛的是( )A、 B、
B、 C、
C、 D、
D、 20. 分子式C4H8O2的有机物与硫酸溶液共热可得有机物A和B.将A氧化最终可得C,且B和C为同系物.若C可发生银镜反应,则原有机物的结构简式为( )A、HCOOCH2CH2CH3 B、CH3COOCH2CH3 C、CH3CH2COOCH3 D、HCOOCH(CH3)221. 下列有关甲苯的实验事实中,能说明侧链对苯环性质有影响的是( )A、甲苯燃烧产生大量黑烟 B、1mol甲苯与3mol H2发生加成反应 C、甲苯能使酸性KMnO4溶液褪色而甲烷不能 D、苯在50~60℃时发生硝化反应而甲苯在30℃时即可22. 用下图所示装置检验乙烯时不需要除杂的是( )
20. 分子式C4H8O2的有机物与硫酸溶液共热可得有机物A和B.将A氧化最终可得C,且B和C为同系物.若C可发生银镜反应,则原有机物的结构简式为( )A、HCOOCH2CH2CH3 B、CH3COOCH2CH3 C、CH3CH2COOCH3 D、HCOOCH(CH3)221. 下列有关甲苯的实验事实中,能说明侧链对苯环性质有影响的是( )A、甲苯燃烧产生大量黑烟 B、1mol甲苯与3mol H2发生加成反应 C、甲苯能使酸性KMnO4溶液褪色而甲烷不能 D、苯在50~60℃时发生硝化反应而甲苯在30℃时即可22. 用下图所示装置检验乙烯时不需要除杂的是( )
选项
乙烯的制备
试剂X
试剂Y
A
CH3CH2Br与NaOH乙醇溶液共热
H2O
KMnO4酸性溶液
B
CH3CH2Br与NaOH乙醇溶液共热
H2O
Br2的CCl4溶液
C
C2H5OH与浓H2SO4加热至170℃
NaOH溶液
KMnO4酸性溶液
D
C2H5OH与浓H2SO4加热至170℃
NaOH溶液
Br2的CCl4溶液
A、A B、B C、C D、D23. 在阿司匹林的结构简式(下式)中①②③④④⑤⑥分别标出了其分子中的不同的键。将阿司匹林与足量NaOH溶液共热,发生反应时断键的位置是( ) A、①④ B、②⑤ C、③④ D、②⑥24. 有一种合成维生素的结构简式为
A、①④ B、②⑤ C、③④ D、②⑥24. 有一种合成维生素的结构简式为 ,对该合成维生素的叙述正确的是( ) A、该合成维生素有三个苯环 B、该合成维生素1mol最多能中和5mol氢氧化钠 C、该合成维生素1mol最多能和含6mol单质溴的溴水反应 D、该合成维生素可用有机溶剂萃取25. 我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如下:
,对该合成维生素的叙述正确的是( ) A、该合成维生素有三个苯环 B、该合成维生素1mol最多能中和5mol氢氧化钠 C、该合成维生素1mol最多能和含6mol单质溴的溴水反应 D、该合成维生素可用有机溶剂萃取25. 我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如下: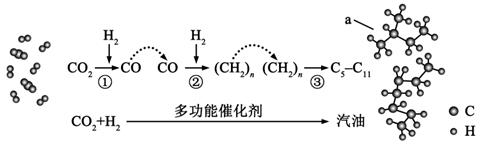
下列说法错误的是( )
A、反应①的产物中含有水 B、反应②中只有碳碳键形成 C、汽油主要是C5~C11的烃类混合物 D、图中a的名称是2-甲基丁烷二、填空题
-
26. 下列几组物质:
①苯和乙苯②CH3COOH和
 ③CH3CH2CH2CH3和
③CH3CH2CH2CH3和 
④ CH3CH2C≡CH和CH3C≡CCH3⑤CH2=CHCH2CH3和
 ⑥
⑥  和
和  (1)、属于同系物的是(填序号,下同);(2)、属于同一物质的是;(3)、由于碳骨架不同而产生的同分异构体是 ;(4)、由于官能团的位置不同而产生的同分异构体是;(5)、具有不同官能团的同分异构体是 。27. 现有下列8种有机物:①乙炔②甲苯③溴乙烷④乙醇⑤苯酚⑥乙醛⑦乙酸⑧乙酸乙酯。请回答:(1)、实验室制备①的反应方程式(2)、能与碳酸氢钠溶液反应产生气体的是(填序号,下同)(3)、在一定条件下能与浓硝酸反应生成TNT的是此反应的化学方程式为(4)、能与银氨溶液发生银镜反应的是此反应的化学方程式为(5)、在一定条件下能与氢氧化钠水溶液反应的是28. 人们对苯及芳香烃的认识有一个不断深化的过程。(1)、已知分子式为C6H6的结构有多种,其中的两种为:
(1)、属于同系物的是(填序号,下同);(2)、属于同一物质的是;(3)、由于碳骨架不同而产生的同分异构体是 ;(4)、由于官能团的位置不同而产生的同分异构体是;(5)、具有不同官能团的同分异构体是 。27. 现有下列8种有机物:①乙炔②甲苯③溴乙烷④乙醇⑤苯酚⑥乙醛⑦乙酸⑧乙酸乙酯。请回答:(1)、实验室制备①的反应方程式(2)、能与碳酸氢钠溶液反应产生气体的是(填序号,下同)(3)、在一定条件下能与浓硝酸反应生成TNT的是此反应的化学方程式为(4)、能与银氨溶液发生银镜反应的是此反应的化学方程式为(5)、在一定条件下能与氢氧化钠水溶液反应的是28. 人们对苯及芳香烃的认识有一个不断深化的过程。(1)、已知分子式为C6H6的结构有多种,其中的两种为:
①这两种结构的区别表现在定性方面(即化学性质方面):Ⅱ能(填入编号,下同),而Ⅰ不能。
A.被酸性高锰酸钾溶液氧化
B.与溴水发生加成反应
C.与溴发生取代反应
D.与氢气发生加成反应
定量方面(即消耗反应物的量的方面):1 mol C6H6与H2加成,Ⅰ需mol,而Ⅱ需mol。
②今发现C6H6还可能有另一种如图所示的立体结构,该结构的二氯代物有种。
 (2)、已知萘的结构简式为
(2)、已知萘的结构简式为 ,该结构简式不能解释萘的下列_______事实(填编号)。 A、萘不能使酸性高锰酸钾溶液褪色 B、萘能与H2发生加成反应 C、萘分子中所有原子在同一平面上 D、一溴代萘(C10H7Br)只有两种同分异构体29. 某有机化合物 A经李比希法测得其中含碳为72.0%、含氢为6.67%,其余为氧。现用下列方法测定该有机化合物的相对分子质量和分子结构。
,该结构简式不能解释萘的下列_______事实(填编号)。 A、萘不能使酸性高锰酸钾溶液褪色 B、萘能与H2发生加成反应 C、萘分子中所有原子在同一平面上 D、一溴代萘(C10H7Br)只有两种同分异构体29. 某有机化合物 A经李比希法测得其中含碳为72.0%、含氢为6.67%,其余为氧。现用下列方法测定该有机化合物的相对分子质量和分子结构。方法一:用质谱法分析得知 A的相对分子质量为150。
方法二:核磁共振仪测出 A的核磁共振氢谱有5个峰,其面积之比为1:2:2:2:3,如下图所示。

方法三:利用红外光谱仪测得 A分子的红外光谱如下图所示。

请填空:
(1)、A的分子式为 。(2)、A的分子中含一个甲基的依据是 。a. A的相对分子质量
b. A的分子式
c. A的核磁共振氢谱图
d. A分子的红外光谱图
(3)、A的结构简式为。三、推断题
-
30. 萜品醇可作为消毒剂、抗氧化剂、医药和溶剂。合成α萜品醇G的路线之一如下:

已知:

请回答下列问题:
(1)、A所含官能团的名称是。(2)、B的分子式为;写出同时满足下列条件的B的链状同分异构体的结构简式:。①核磁共振氢谱有2个吸收峰 ② 能发生银镜反应
(3)、B → C、E → F的反应类型分别为、。(4)、C → D的化学方程式为。(5)、通过常温下的反应,区别E、F和G的试剂是和。四、实验题
-
31. 已知乙醇可以和氯化钙反应生成微溶于水的CaCl2·6C2H5OH。有关的有机试剂的沸点如下:
CH3COOC2H5为77.1℃; C2H5OH为78.3℃;
C2H5OC2H5(乙醚)为34.5℃; CH3COOH为118℃。
实验室合成乙酸乙酯粗产品的步骤如下:在蒸馏烧瓶内将过量的乙醇与少量浓硫酸混合,然后经分液漏斗边滴加醋酸,边加热蒸馏。由上面的实验可得到含有乙醇、乙醚、醋酸和水的乙酸乙酯粗产品。
(1)、制取乙酸乙酯的方程式是。将粗产品经下列步骤精制:
(2)、为除去其中的醋酸,可向产品中加入__________(填字母)。A、无水乙醇 B、碳酸钠粉末 C、无水醋酸钠(3)、再向其中加入饱和氯化钙溶液,振荡,分离,其目的是。(4)、然后再向其中加入无水硫酸铜,振荡,其目的是。最后,将经过上述处理后的液体加入另一干燥的蒸馏瓶内,再蒸馏,弃去低沸点馏分,收集沸点在76℃~78℃之间的馏分即得纯净的乙酸乙酯。
-