初中化学人教版九年级上学期 第五单元测试卷
试卷更新日期:2019-09-19 类型:单元试卷
一、单选题
-
1. 氯酸钾在二氧化锰的催化作用下受热分解制取氧气,其化学方程式书写正确的是( )A、KClO3 KCl+O2↑ B、2KClO3 2KCl+3O2↑ C、2KClO3 2KCl+3O2↑ D、2KClO3 2KCl+3O2↑2. 钠着火不能用二氧化碳灭火。钠在二氧化碳中燃烧生成炭黑和一种白色固体,它可能是()A、碳酸钠 B、硫酸钠 C、碳酸氢钠 D、氢氧化钠3. 某反应的微观示意图如下所示,下列说法错误的是( )
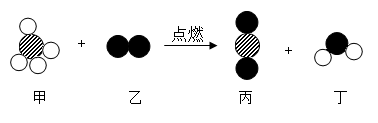 A、反应中甲、乙的分子个数之比为1︰2 B、反应前后分子数目不变 C、反应后丙、丁的分子个数之比为1︰1 D、反应前后原子数目不变4. 2019年5月,华为宣布做好了启动备用芯片的准备,硅是计算机芯片的基体材料。高温下氢气与四氯化硅反成制硅的化学方程式为:2H2+SiCl4 Si+4X,其中X的化学式为( )A、Cl2 B、HCl C、H2O D、SiH45. 对于化学反应2KClO3 2KCl+3O2↑,下列说法错误的是()A、该反应属于分解反应 B、固体减少的质量等于生成O2的质量 C、MnO2加快了该反应速率 D、氯酸钾中K、O元素的质量比是39:166. 甲烷燃烧的微观示意图如下,其中方框中需要补充的是()
A、反应中甲、乙的分子个数之比为1︰2 B、反应前后分子数目不变 C、反应后丙、丁的分子个数之比为1︰1 D、反应前后原子数目不变4. 2019年5月,华为宣布做好了启动备用芯片的准备,硅是计算机芯片的基体材料。高温下氢气与四氯化硅反成制硅的化学方程式为:2H2+SiCl4 Si+4X,其中X的化学式为( )A、Cl2 B、HCl C、H2O D、SiH45. 对于化学反应2KClO3 2KCl+3O2↑,下列说法错误的是()A、该反应属于分解反应 B、固体减少的质量等于生成O2的质量 C、MnO2加快了该反应速率 D、氯酸钾中K、O元素的质量比是39:166. 甲烷燃烧的微观示意图如下,其中方框中需要补充的是()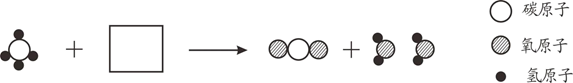 A、
A、 B、
B、 C、
C、 D、
D、 7. 超氧化钾(KO2)常备于急救器和消防队员背包中,能迅速与水反应放出氧气:
7. 超氧化钾(KO2)常备于急救器和消防队员背包中,能迅速与水反应放出氧气:2KO2+2H2O=2KOH+X+O2↑,关于此反应的说法不正确的是 ( )
A、X的化学式为H2O2 B、反应前后元素种类发生变化 C、反应前后氧元素化合价发生变化 D、反应前后物质状态发生变化8. 在化学反应 中,已知 与 恰好完全反应,生成C和D的质量比为 ,又知B的相对分子质量为32,则D的相对分子质量为( )A、9 B、12 C、18 D、369. 在一个密闭容器中,有甲、乙、丙、丁、戊五种物质,在一定条件下发生反应,测得反应前后各物质的质量变化量如图所示(图中正数表示物质质量的增加量,负数表示物质质量的减少是,0表示物质质量不变),下列说法正确的是()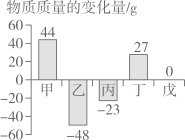 A、该反应一定属于置换反应 B、戊一定是该反应的催化剂 C、参加反应的乙、丙的质量比一定为48:23 D、该反应中甲、丁的相对分子质量之比一定为44:2710. 在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前及反应过程中两个时刻各物质的质量如图所示,图中a、b、c、d分别表示相应物质的质量。下列说法正确的是()
A、该反应一定属于置换反应 B、戊一定是该反应的催化剂 C、参加反应的乙、丙的质量比一定为48:23 D、该反应中甲、丁的相对分子质量之比一定为44:2710. 在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前及反应过程中两个时刻各物质的质量如图所示,图中a、b、c、d分别表示相应物质的质量。下列说法正确的是()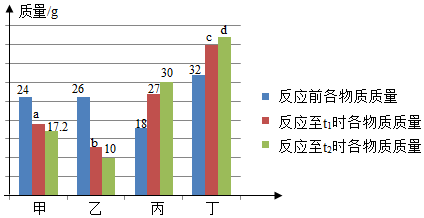 A、b的数值为14 B、该反应为复分解反应 C、反应过程中乙与丁发生改变的质量比为5:6 D、充分反应后生成丙的质量为37.5g11. 在一定条件下,一密闭容器内发生某反应,测得反应前后各物质的质量如下表所示。下列说法错误的是()
A、b的数值为14 B、该反应为复分解反应 C、反应过程中乙与丁发生改变的质量比为5:6 D、充分反应后生成丙的质量为37.5g11. 在一定条件下,一密闭容器内发生某反应,测得反应前后各物质的质量如下表所示。下列说法错误的是()物质
a
b
c
d
反应前的质量/g
40
5
16
15
反应后的质量/g
X
5
30
26
A、b可能是催化剂 B、X的值等于15 C、该反应是分解反应 D、参加反应的c与d的质量比为15:13二、填空题
-
12. 2.2g某物质在氧气中完全燃烧,生成6.6g二氧化碳和3.6g水(无其他生成物),则该物质中一定含有元素.(列式计算)各原子的个数比 .
13. 某化学兴趣小组的同学到化学实验室,用铝和氢氧化钠溶液反应来制备氢气。同学们取了3g纯铝片和40g一定质量分数的氢氧化钠溶液,充分反应后,铝片有剩余,称得反应后剩余物质的总质量为42.7g。试计算:(1)、生成氢气的质量是g;(2)、所用氢氧化钠溶液的溶质质量分数为。(提示:2Al+2NaOH+2H2O=2NaAlO2+3H2↑)14. 根据下图实验,回答问题: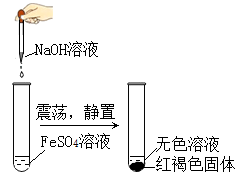 (1)、 中硫元素的化合价为。(2)、生成红褐色固体的总反应的化学方程式为 .
(1)、 中硫元素的化合价为。(2)、生成红褐色固体的总反应的化学方程式为 .提示:① 在空气中极易被氧化。
②方程式中 的配平系数为4.
三、计算题
-
15. 实验室新进一批块状大理石,某化学小组成员称取12.5g该大理石样品,加入足量稀盐酸测定碳酸钙的含量,完全反应后,称得固体剩余物的质量为2.5g,样品中杂质不溶于水且不与稀盐酸反应,请回答下列问题:(1)、该样品中碳酸钙的质量为。(2)、计算12.5g该样品最多可以制得二氧化碳的质量,写出必要的计算过程。16. 碳酸锶(SrCO3)可用于制造红色火焰、荧光玻璃等。小赵同学为测定某SrCO3和NaCl固体混合物中SrCO3的质量分数,在三个烧杯中进行相关实验,实验所用稀盐酸的溶质的质量分数相同。所得数据如下表所示:
烧杯编号
①
②
③
稀盐酸质量/g
100
200
300
固体混合物质量/g
100
100
100
反应后烧杯中物质的质量/g
195.6
291.2
391.2
试求:
(1)、烧杯②中产生CO2的质量为g。(2)、原固体混合物中SrCO3的质量分数(计算结果精确到0.1%)。(提示:SrCO3+2HCl=SrCl2+CO2↑+H2O)
17. “石头纸”是一种介于纸张和塑料之间的新型材料(主要成分为碳酸钙)。为测定其中碳酸钙的含量,课外活动小组的同学称取 50g 碎纸样品。分别在 5 只烧杯中进行了实验,实验数据见下表(假设纸张其他成分既不溶于水,也不与水反应):烧杯①
烧杯②
烧杯③
烧杯④
烧杯⑤
加入样品的质量/g
10
10
10
10
10
加入稀盐酸的质量/g
20
40
60
80
100
充分反应后生成气体的质量/g
0.88
1.76
2.44
3.52
3.52
(1)、10g 样品与足量稀盐酸反应最多生成气体克。(2)、烧杯填序号)中记录的实验数据有明显错误,理由是。(3)、求所用盐酸溶质质量分数。(写出计算过程)四、综合题
-
18. 根据如图所示的实验回答问题。
甲
 乙
乙 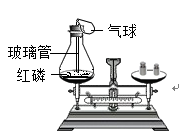 (1)、甲为蒸发溶液的实验。加热时若不搅拌,造成的后果是;当观察到时,停止加热。(2)、乙为通过红磷燃烧前后质量的测定验证质量守恒定律的实验。用红热的玻璃管引燃红磷,实验现象是:红磷燃烧,产生 , 放出大量热。实验中气球的作用除了使装置密闭之外,还可以防止;实验时若取用红磷的量不足,对实验的结果(选填“有”或“没有”)影响。19. 工业上使用一种国产低温催化剂生产氢气的反应过程如图所示
(1)、甲为蒸发溶液的实验。加热时若不搅拌,造成的后果是;当观察到时,停止加热。(2)、乙为通过红磷燃烧前后质量的测定验证质量守恒定律的实验。用红热的玻璃管引燃红磷,实验现象是:红磷燃烧,产生 , 放出大量热。实验中气球的作用除了使装置密闭之外,还可以防止;实验时若取用红磷的量不足,对实验的结果(选填“有”或“没有”)影响。19. 工业上使用一种国产低温催化剂生产氢气的反应过程如图所示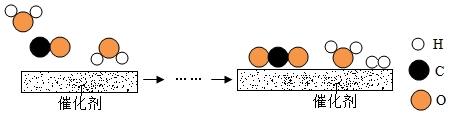 (1)、该微观反应过程中出现了种氧化物。(2)、参加反应的
(1)、该微观反应过程中出现了种氧化物。(2)、参加反应的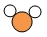 与
与  分子个数之比为。 (3)、该反的化学方程式为。20. 已知:2Na2O2+2CO2=2Na2CO3+O2;2Na2O2+2H2O=4NaOH+O2↑.为了证明过氧化钠(Na2O2)固体可在呼吸面具和潜水艇中做供氧剂,某化学兴趣小组的同学利用如图所示实验装置进行探究活动。(铁架台等已略去)
分子个数之比为。 (3)、该反的化学方程式为。20. 已知:2Na2O2+2CO2=2Na2CO3+O2;2Na2O2+2H2O=4NaOH+O2↑.为了证明过氧化钠(Na2O2)固体可在呼吸面具和潜水艇中做供氧剂,某化学兴趣小组的同学利用如图所示实验装置进行探究活动。(铁架台等已略去) (1)、A装置中所发生反应的化学方程式为。(2)、请将如图F方框中A装置的长颈漏斗和玻璃导管补画完整。(3)、D装置的作用是。E装置中可能发生的有关反应的化学方程式为。(4)、为了达到实验的目的,以上装置导管接口正确的连接顺序为a接、接、接、接b。(5)、氧气可采用B装置收集并用带火星的木条检验,这是利用了氧气的哪些性质?(6)、实验结束后,取C装置中固体溶于水,无气泡产生。请设计实验,检验C装置中固体的成分。(简要写出实验步骤、现象和结论)。(7)、某潜水艇上有100人,如果每人每分钟消耗氧气为0.001kg,假如所需要的氧气全部由Na2O2与CO2反应来提供,则该潜水艇一天所需要Na2O2的质量是多少?
(1)、A装置中所发生反应的化学方程式为。(2)、请将如图F方框中A装置的长颈漏斗和玻璃导管补画完整。(3)、D装置的作用是。E装置中可能发生的有关反应的化学方程式为。(4)、为了达到实验的目的,以上装置导管接口正确的连接顺序为a接、接、接、接b。(5)、氧气可采用B装置收集并用带火星的木条检验,这是利用了氧气的哪些性质?(6)、实验结束后,取C装置中固体溶于水,无气泡产生。请设计实验,检验C装置中固体的成分。(简要写出实验步骤、现象和结论)。(7)、某潜水艇上有100人,如果每人每分钟消耗氧气为0.001kg,假如所需要的氧气全部由Na2O2与CO2反应来提供,则该潜水艇一天所需要Na2O2的质量是多少?