华师大版科学九年级上册 2.2 重要的酸(第3课时)
试卷更新日期:2019-09-06 类型:同步测试
一、选择题
-
1. 下列方案不可行的是( )A、用氢氧化钠干燥二氧化碳气体 B、用稀硫酸除去炭粉中的氧化铜 C、用硝酸钡溶液区别硫酸和盐酸 D、用稀盐酸和大理石制取二氧化碳2. 下列各组离子反应可用H++OH-=H2O表示的是( )A、氢氧化钡和硫酸 B、氢氧化铜和盐酸 C、盐酸和氢氧化钠 D、硫酸和氢氧化镁3. 下列各组物质,相互不能发生反应的是()A、氢氧化钠溶液和硫酸 B、氧化铜和盐酸 C、二氧化碳和氢氧化钠溶液 D、硫酸和二氧化碳4. 在A+B→盐+水的反应中,A、B分別是( )A、纯碱和熟石灰 B、小苏打和盐酸 C、硫酸和熟石灰 D、熟石灰和氯化铵5. 下列各组溶液,相互能发生反应的是( )
①碳酸钠和氯化钙 ②氢氧化钾和盐酸 ③硫酸和氯化钠 ⑤碳酸钾和硝酸 ⑤硫酸铜和氯化铵
A、①②④ B、②④⑤ C、③④⑤ D、①②③6. 下列各组物质中,能相互反应且反应前后溶液总质量随时间变化符合如图所示的是( ) A、铁和硝酸银溶液 B、硫酸和烧碱溶液 C、氧化铜和盐酸 D、硝酸钾溶液和稀硫酸7. 关于硫酸和盐酸,下列说法不正确的是( )A、其浓溶液露置在空气中一段时间,质量分数都会减小 B、其稀溶液都能使紫色石蕊试液变红色 C、其稀溶液都可用于除去钢铁制品表面的铁锈 D、都能与Ba(NO3)2溶液反应生成白色沉淀8. 向表中的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成的气体或沉淀的质量与加入乙的质量关系用如图所示曲线表示的是()
A、铁和硝酸银溶液 B、硫酸和烧碱溶液 C、氧化铜和盐酸 D、硝酸钾溶液和稀硫酸7. 关于硫酸和盐酸,下列说法不正确的是( )A、其浓溶液露置在空气中一段时间,质量分数都会减小 B、其稀溶液都能使紫色石蕊试液变红色 C、其稀溶液都可用于除去钢铁制品表面的铁锈 D、都能与Ba(NO3)2溶液反应生成白色沉淀8. 向表中的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成的气体或沉淀的质量与加入乙的质量关系用如图所示曲线表示的是()序号
甲
乙
①
铜、锌的混合物
稀硫酸
②
生锈的铁钉
稀盐酸
③
稀的混合溶液
氯化钡溶液
④
硫酸和硫酸铜的混合溶液
氢氧化钠溶液
 A、①③ B、①④ C、②③ D、②④
A、①③ B、①④ C、②③ D、②④二、非选择题
-
9. 硫酸和盐酸既是实验室常用的试剂,也是重要的化工原料.它们既有相似之处,又有不同之处(1)、它们的水溶液的pH都7 (填“大于”、“小于”、“等于”).(2)、它们都能除去铁锈,写出盐酸与铁锈主要成分反应的化学方程式:.
(3)、打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶敞口放置,瓶口出现白雾的是.
(4)、请写出把硫酸转变为盐酸的化学方程式.
10. 硫酸和盐酸既是实验室常用的试剂,也是重要的化工原料.(1)、从组成上看,两者的不同点是.
(2)、打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是.
(3)、只用一种试剂,鉴别两瓶失去标签的稀盐酸和稀硫酸溶液,你选用的试剂是.
(4)、用熟石灰中和一定量的稀盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示,若改用n克熟石灰去中和相同质量和质量分数的稀硫酸,所得溶液的pH7(选填“>”、“<”或“=”).11. 在一次学生分组实验之后,小红同学利用课外活动时间来到实验室帮助老师整理实验药品.在一个实验台前,小红发现实验台上散乱地摆放着下列药品 (1)、小红发现有两瓶盛有无色溶液的试剂瓶④⑦,标签已经脱落,分别是硫酸和盐酸.请你帮助他设计一个小实验来鉴别两瓶试剂.(写出实验方法和判断依据)(2)、小红将脱落的标签贴上后,他按氧化物、酸、碱、盐的顺序将七种药品分类摆放,请根据他的分类的情况用序号填空:氧化物 .(3)、小红从上面七种药品选择两种,他准备做一个中和反应的实验.他在做中和反应实验时为了便于观察反应是否发生,他在所取的少量溶液中加入几滴酚酞试液,试液变红,当他向所取的溶液中再滴加酸时,观察到红色变成无色.根据实验现象写出一个中和反应的化学方程式.(4)、小红还发现试剂瓶①没有盖上瓶塞,一直敞口放置着.他猜想可能有一部分生石灰已变质生成了碳酸钙.为确认这一猜想,小红称取了10g样品(假设样品中只含有生石灰和碳酸钙,且混合均匀),加入过量稀盐酸60g,至样品不再有气体放出为止,称量反应残余物质质量为69.56g.他根据有关的数据确认了生石灰发生了变质及变质的程度,请你计算此瓶生石灰的纯度.12. 为测定由盐酸和硫酸组成的某混合酸中溶质的质量分数,取100g该混合酸,逐滴滴加某Ba(OH)2溶液,生成沉淀BaSO4的质量
(1)、小红发现有两瓶盛有无色溶液的试剂瓶④⑦,标签已经脱落,分别是硫酸和盐酸.请你帮助他设计一个小实验来鉴别两瓶试剂.(写出实验方法和判断依据)(2)、小红将脱落的标签贴上后,他按氧化物、酸、碱、盐的顺序将七种药品分类摆放,请根据他的分类的情况用序号填空:氧化物 .(3)、小红从上面七种药品选择两种,他准备做一个中和反应的实验.他在做中和反应实验时为了便于观察反应是否发生,他在所取的少量溶液中加入几滴酚酞试液,试液变红,当他向所取的溶液中再滴加酸时,观察到红色变成无色.根据实验现象写出一个中和反应的化学方程式.(4)、小红还发现试剂瓶①没有盖上瓶塞,一直敞口放置着.他猜想可能有一部分生石灰已变质生成了碳酸钙.为确认这一猜想,小红称取了10g样品(假设样品中只含有生石灰和碳酸钙,且混合均匀),加入过量稀盐酸60g,至样品不再有气体放出为止,称量反应残余物质质量为69.56g.他根据有关的数据确认了生石灰发生了变质及变质的程度,请你计算此瓶生石灰的纯度.12. 为测定由盐酸和硫酸组成的某混合酸中溶质的质量分数,取100g该混合酸,逐滴滴加某Ba(OH)2溶液,生成沉淀BaSO4的质量和pH的变化关系如图1所示.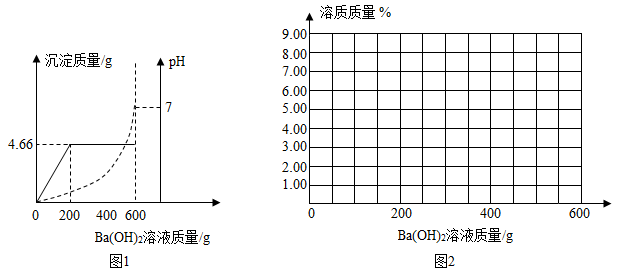
(1)、当加入的氢氧化钡溶液为g时,混合酸恰好被中和。(2)、求Ba(OH)2溶液中的溶质质量分数是多少?(写出计算过程,结果精确到0,01%)(3)、盐酸的溶质质量分数是 . (结果精确到0.01%)(4)、请在图2中画出向100g该混合酸中加入600g Ba(OH)2溶液的过程中,混合酸中溶质的质量与所加的Ba(OH)2溶液的质量关系图.