高化人教新版必修1第一章第二节 离子反应同步训练
试卷更新日期:2019-09-03 类型:同步测试
一、单选题
-
1. 下列属于电解质的是( )A、明矾 B、盐酸 C、氨气 D、钾钠合金2. 下列各组物质,前者属于电解质,后者属于非电解质的是()A、NaCl晶体、BaSO4 B、铜、二氧化硫 C、硫酸、乙醇 D、熔融的KNO3、硫酸溶液3. 下列关于电解质说法正确是( )A、能导电的物质叫电解质 B、NaCl晶体不导电,所以NaCl不是电解质 C、熔融的KOH导电,所以KOH是电解质 D、电解质在通电时发生电离4. 已知某溶液中存在H+、Ba2+、Fe3+三种阳离子,则其中可能大量存在的阴离子是( )A、SO
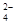 B、CO32-
C、NO3-
D、OH-
5. 在无色透明溶液中,能大量共存的离子组是( )A、Mg2+、Na+、SO42- B、K+、H+、HCO3- C、Cu2+、NO3-、SO42- D、Ba2+、NO3-、CO32-6. 下列离子方程式书写正确的是( )A、钠与水反应:Na+2H2O=Na++2OH-+H2↑ B、稀盐酸与苏打溶液反应:HCO +H+=CO2↑+H2O C、向次氨酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO D、铁盐腐蚀铜质电路板:2Fe3++Cu=2Fe2++Cu2+7. 下列实验过程中产生的现象与图形相符合的是( )
B、CO32-
C、NO3-
D、OH-
5. 在无色透明溶液中,能大量共存的离子组是( )A、Mg2+、Na+、SO42- B、K+、H+、HCO3- C、Cu2+、NO3-、SO42- D、Ba2+、NO3-、CO32-6. 下列离子方程式书写正确的是( )A、钠与水反应:Na+2H2O=Na++2OH-+H2↑ B、稀盐酸与苏打溶液反应:HCO +H+=CO2↑+H2O C、向次氨酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO D、铁盐腐蚀铜质电路板:2Fe3++Cu=2Fe2++Cu2+7. 下列实验过程中产生的现象与图形相符合的是( )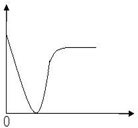 A、稀硫酸滴加到Ba(OH)2溶液中(横坐标是稀硫酸的体积,纵坐标为溶液的导电能力) B、铁粉加到一定量 CuSO4 溶液中(横坐标是铁粉的质量,纵坐标为沉淀质量) C、CO2 通入一定量 NaOH 溶液中(横坐标是 CO2 的体积,纵坐标为溶液的导电能力) D、稀盐酸滴加到一定量 NaOH 溶液中(横坐标是稀盐酸的体积,纵坐标为钠离子物质的量)8. 下表中对离子方程式的评价合理的是( )
A、稀硫酸滴加到Ba(OH)2溶液中(横坐标是稀硫酸的体积,纵坐标为溶液的导电能力) B、铁粉加到一定量 CuSO4 溶液中(横坐标是铁粉的质量,纵坐标为沉淀质量) C、CO2 通入一定量 NaOH 溶液中(横坐标是 CO2 的体积,纵坐标为溶液的导电能力) D、稀盐酸滴加到一定量 NaOH 溶液中(横坐标是稀盐酸的体积,纵坐标为钠离子物质的量)8. 下表中对离子方程式的评价合理的是( )选项
化学反应及其离子方程式
评价
A
H2SO4溶液与Ba(OH)2溶液反应: H++ +Ba2++OH−=BaSO4↓+H2O
正确
B
向碳酸镁浊液中加入足量稀盐酸:
+2H+=CO2↑+H2O
错误,碳酸镁不应写成离子形式
C
向沸水中滴加饱和的氯化铁溶液至液体变为红褐色:Fe3++3H2O=Fe(OH)3↓+3H+
正确
D
向NaOH溶液中通入少量CO2反应:OH−+CO2=
正确
A、A B、B C、C D、D二、综合题
-
9. 现有以下物质:①铜 ②氨的水溶液 ③纯醋酸 ④NaOH固体 ⑤稀硫酸 ⑥CO2 ⑦BaSO4固体 ⑧乙醇 ⑨CaO固体 ⑩熔融的KNO3(1)、能导电的是;(2)、属于非电解质的是 ;(3)、既不属于电解质也不属于非电解质的是 ;(4)、写出上述物质中②和⑤反应的离子方程式(5)、写出上述物质中⑤和Ba(OH)2反应的离子方程式10.(1)、书写下列反应的离子方程式
①NaOH溶液和H2SO4溶液:;
②NaCl溶液和AgNO3溶液:;
③Ba(OH)2溶液和H2SO4溶液:;
④Fe与CuSO4溶液反应:;
⑤Na2CO3溶液与Ca(OH)2溶液反应: 。
(2)、写出下列离子方程式表示的化学方程式。①CO32-+2H+=CO2↑+H2O;
②Ag++Cl-=AgCl↓;
③Cu2++2OH-=Cu(OH)2↓;
④SO2+2OH-=SO32-+H2O;
⑤Fe2O3+6H+=2Fe3++3H2O;
⑥Ba2++2OH-+CO2=BaCO3↓+H2O;
⑦Ba2++SO42-=BaSO4↓;
⑧Fe(OH)3+3H+=Fe3++3H2O。
11. 为了确认电解质溶液中部分离子相互间能否发生反应,及离子反应发生的条件,做如表四组实验.编号
Ⅰ
Ⅱ
Ⅲ
Ⅳ
实验
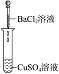

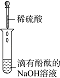
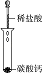 (1)、实验Ⅰ的现象 , 写出反应的离子方程式 .(2)、实验Ⅱ的目的是 .(3)、实验Ⅲ的现象证明了溶液中的两种离子之间发生了化学反应.(4)、实验Ⅳ中发生反应的离子方程式是 .
(1)、实验Ⅰ的现象 , 写出反应的离子方程式 .(2)、实验Ⅱ的目的是 .(3)、实验Ⅲ的现象证明了溶液中的两种离子之间发生了化学反应.(4)、实验Ⅳ中发生反应的离子方程式是 .