甘肃省陇南市徽县2018-2019学年中考化学5月模拟考试试卷
试卷更新日期:2019-08-27 类型:中考模拟
一、单选题
-
1. 如图为空气成分示意图(按体积分数计算),其中“c”代表的是( )
 A、氧气 B、氮气 C、二氧化碳 D、稀有气体2. 下列汽车尾气的主要成分属于单质的是( )A、氮气 B、一氧化碳 C、二氧化碳 D、一氧化氮3. 下列物质可用作氮肥的是()A、Ca3(PO)4 B、K2CO3 C、NH4Cl D、NaCl4. 下列实验操作正确的是( )A、
A、氧气 B、氮气 C、二氧化碳 D、稀有气体2. 下列汽车尾气的主要成分属于单质的是( )A、氮气 B、一氧化碳 C、二氧化碳 D、一氧化氮3. 下列物质可用作氮肥的是()A、Ca3(PO)4 B、K2CO3 C、NH4Cl D、NaCl4. 下列实验操作正确的是( )A、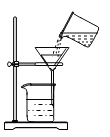 过滤
B、
过滤
B、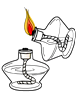 点燃酒精灯
C、
点燃酒精灯
C、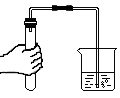 检查装置气密性
D、
检查装置气密性
D、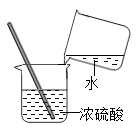 稀释浓硫酸
5. 下列人体所必需的元素中,缺乏后会导致佝偻病、骨质疏松的是( )A、铁 B、钙 C、碘 D、锌6. 下列物质对应的化学式书写正确的是( )A、氯化铝 AlCl B、氧化钠 NaO C、硫酸铁 FeSO4 D、硝酸镁 Mg(NO3)27. 海带中富含碘元素(I),可利用反应2NaI+Cl2═2NaCl+I2从海带中提取碘单质(I2)。此反应属于()A、化合反应 B、分解反应 C、复分解反应 D、置换反应8. NaOH溶液和稀盐酸发生中和反应的过程中,溶液pH的变化如图所示。下列说法正确的是()
稀释浓硫酸
5. 下列人体所必需的元素中,缺乏后会导致佝偻病、骨质疏松的是( )A、铁 B、钙 C、碘 D、锌6. 下列物质对应的化学式书写正确的是( )A、氯化铝 AlCl B、氧化钠 NaO C、硫酸铁 FeSO4 D、硝酸镁 Mg(NO3)27. 海带中富含碘元素(I),可利用反应2NaI+Cl2═2NaCl+I2从海带中提取碘单质(I2)。此反应属于()A、化合反应 B、分解反应 C、复分解反应 D、置换反应8. NaOH溶液和稀盐酸发生中和反应的过程中,溶液pH的变化如图所示。下列说法正确的是() A、反应开始前,测量的是NaOH溶液的pH B、b点时,NaOH和HCl恰好完全反应 C、a点处的溶液能够使酚酞溶液变红 D、c点处的溶液能与Fe反应产生气体9. 下列实验操作能达到实验目的是()
A、反应开始前,测量的是NaOH溶液的pH B、b点时,NaOH和HCl恰好完全反应 C、a点处的溶液能够使酚酞溶液变红 D、c点处的溶液能与Fe反应产生气体9. 下列实验操作能达到实验目的是()选项
实验目的
实验操作
A
证明CaO能与水反应
加入水,测温度
B
证明氧气能支持燃烧
伸入带火星的木条
C
除去CO2气体中的CO
通入氧气后,点燃
D
除去Na2CO3中NaOH
加入适量的稀盐酸
A、A B、B C、C D、D10. 氧烛是一种用于缺氧环境中自救的化学氧源,广泛用于航空、航海等领域,其主要成分为NaClO3 , 还含有适量的催化剂、成型剂等。氧烛通过撞击火帽引发反应后,能持续放出高纯氧气,主要反应原理为2NaClO3═2NaCl+3O2↑.一根氧烛大约可以供100个人呼吸1小时。下列说法错误的是()A、氧烛是一种纯净物 B、NaClO3中Cl为+5价 C、氧烛制取氧气的反应为分解反应 D、在运输氧烛时,应避免其受到撞击二、填空题
-
11. 用化学用语填空。(1)、酸中都含有的离子。(2)、常用来改良酸性土壤的碱。(3)、易潮解的一种碱。(4)、三个二氧化硫分子。12. 《神秘岛》是儒勒•凡尔纳海洋三部曲的第三部,讲述了美国南北战争时期,被困在南军城中的几个北方人乘气球逃脱之后,飘落到“林肯岛”上求生的故事。(1)、将两片怀表上的玻璃合在一起,中部灌满水,边缘用泥粘合,制成凸透镜;用透镜集聚太阳光,照射下列物质,可以燃烧起来的是(填字母序号,下同)。
 (2)、将岛上的水生植物晒干、焚烧后,可获得Na2CO3等。Na2CO3中含有种元素。(3)、将赤铁矿石和木炭一层又一层叠加起来,用鼓风机吹进空气,高温加热后可以获得铁。写出一氧化碳与赤铁矿石反应的化学方程式:。(4)、岛上的黄铁矿(主要成分为FeS2)在空气中高温加热时生成一种有激性气味的气体,该气体可用来制造硫酸。这种气体是___A、O2 B、Fe C、SO2 D、NH313. 为了保证长时间潜航,在潜水艇里要配备氧气再生装置。有以下几种制氧气的方法:①加热高锰酸钾②电解水③在常温下过氧化钠(Na2O2)固体与二氧化碳反应生成碳酸钠和氧气。(1)、写出方法③制取氧气的化学方程式。(2)、你认为最适合于潜水艇里制氧气的方法是(填序号)。(3)、如图为某化学反应的微观过程,其中不同的两种小球表示两种不同原子。
(2)、将岛上的水生植物晒干、焚烧后,可获得Na2CO3等。Na2CO3中含有种元素。(3)、将赤铁矿石和木炭一层又一层叠加起来,用鼓风机吹进空气,高温加热后可以获得铁。写出一氧化碳与赤铁矿石反应的化学方程式:。(4)、岛上的黄铁矿(主要成分为FeS2)在空气中高温加热时生成一种有激性气味的气体,该气体可用来制造硫酸。这种气体是___A、O2 B、Fe C、SO2 D、NH313. 为了保证长时间潜航,在潜水艇里要配备氧气再生装置。有以下几种制氧气的方法:①加热高锰酸钾②电解水③在常温下过氧化钠(Na2O2)固体与二氧化碳反应生成碳酸钠和氧气。(1)、写出方法③制取氧气的化学方程式。(2)、你认为最适合于潜水艇里制氧气的方法是(填序号)。(3)、如图为某化学反应的微观过程,其中不同的两种小球表示两种不同原子。
①反应属于(填基本反应类型)反应。
②虚线框内应填的微观图示是(选填A、B、C、D)。
 14. 如图是甲、乙两种固体物质的溶解度曲线。
14. 如图是甲、乙两种固体物质的溶解度曲线。 (1)、t1℃时,甲、乙两种物质的溶解度。(2)、t2℃时,将等质量的甲、乙两种物质加水溶解配制成饱和溶液,所得溶液质量的大小关系为:甲乙(填“>”、“=”或“<”)。(3)、把一瓶接近饱和的甲物质的溶液变为饱和溶液,可行的方法是。(答一种方法即可)(4)、甲中含少量乙,若要提取纯净的甲物质,具体的操作是。15. 现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为浅绿色溶液,G为蓝色溶液,它们之间存在如图关系:
(1)、t1℃时,甲、乙两种物质的溶解度。(2)、t2℃时,将等质量的甲、乙两种物质加水溶解配制成饱和溶液,所得溶液质量的大小关系为:甲乙(填“>”、“=”或“<”)。(3)、把一瓶接近饱和的甲物质的溶液变为饱和溶液,可行的方法是。(答一种方法即可)(4)、甲中含少量乙,若要提取纯净的甲物质,具体的操作是。15. 现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为浅绿色溶液,G为蓝色溶液,它们之间存在如图关系: (1)、推测下列物质的化学式:B , D , F;(2)、写出C→A转化的化学方程式:。
(1)、推测下列物质的化学式:B , D , F;(2)、写出C→A转化的化学方程式:。三、实验题
-
16. 如图是初中化学常见的气体发生与收集装置,根据要求回答下列问题。
 (1)、写出仪器名称a , b。(2)、实验室用装置A制取氧气的化学方程式是。(3)、若采用C装置收集氧气,验满的操作是。(4)、实验室用锌粒和稀硫酸制取氢气所选用的一组发生和收集装置是(填序号),写出该反应的化学方程式。(5)、实验室以大理石和稀盐酸为原料制取二氧化碳,采用装置作为气体的发生装置反应的化学方程式为。收集二氧化碳采用的方法是法。(6)、氯气(Cl2)是一种黄绿色的有毒气体,密度比空气大,能和水、氢氧化钠溶液等反应。实验室用装置F收集氯气,氯气应从(填“c”或“d”)端通入。为防止Cl2造成污染,还要用碱液吸收多余的Cl2 . 请完成Cl2和NaOH反应的化学方程式:Cl2+2NaOH=+NaClO+H2O
(1)、写出仪器名称a , b。(2)、实验室用装置A制取氧气的化学方程式是。(3)、若采用C装置收集氧气,验满的操作是。(4)、实验室用锌粒和稀硫酸制取氢气所选用的一组发生和收集装置是(填序号),写出该反应的化学方程式。(5)、实验室以大理石和稀盐酸为原料制取二氧化碳,采用装置作为气体的发生装置反应的化学方程式为。收集二氧化碳采用的方法是法。(6)、氯气(Cl2)是一种黄绿色的有毒气体,密度比空气大,能和水、氢氧化钠溶液等反应。实验室用装置F收集氯气,氯气应从(填“c”或“d”)端通入。为防止Cl2造成污染,还要用碱液吸收多余的Cl2 . 请完成Cl2和NaOH反应的化学方程式:Cl2+2NaOH=+NaClO+H2O四、科学探究题
-
17. 某兴趣小组发现铁钉生锈需要几天的时间,询问老师如何加快铁钉生锈的速度。
老师说氯化物可能加快铁钉生锈的速度。
(提出问题)氯化物对铁钉生锈有怎样的影响?
(查阅资料)
ⅰ.NaCl、CaCl2、CuCl2等由氯离子与金属离子构成的盐属于氯化物。
ⅱ.铜能与氧气反应,生成黑色的CuO。
ⅲ.CuO能与稀硫酸发生反应:CuO+H2SO4═CuSO4+H2O。
(进行实验、分析解释、获得结论)
(1)、实验1:探究氯化物对铁钉生锈速度的影响。试管
编号
①
②
③
④
实验




现象
2天后,铁钉表面出现红色
1天后,铁钉表面出现红色
1天后,铁钉表面出现红色
7分钟时铁钉表面出现红色,20分钟后试管底部出现红色沉淀
对比实验①②③可以得到的结论是。
(2)、小组同学认为,试管④中的红色沉淀可能是铁锈,也可能是铜。他们认为红色沉淀可能是铜的理由是(用化学方程式解释)。(3)、实验2:探究试管④中红色沉淀的物质组成。实验步骤
实验操作
实验现象
Ⅰ
取出试管④中的铁钉,过滤剩余物,洗涤滤纸上的物质
固体为红色
Ⅱ
将步骤Ⅰ所得红色固体加入试管中,再向试管中加入足量的…….
红色固体大部分溶解,溶液变为黄色
Ⅲ
将步骤Ⅱ所得混合物过滤,洗涤、干燥滤纸上的固体后,置于石棉网上充分加热
红色固体变黑
Ⅳ
向试管中加入步骤Ⅲ所得黑色固体,再加入足量稀硫酸
黑色固体全部溶解,溶液变为蓝色
步骤Ⅱ中所加入的试剂是。
(4)、步骤Ⅲ、Ⅳ的实验目的是。(5)、由实验2可得出结论:试管④中红色沉淀的物质组成是。(6)、(反思与评价)结合实验1、2的结论,对于“氯化物对铁钉生锈速度的影响”,小组同学提出了进一步的假设:。
五、计算题
-
