人教版化学高二选修3第三章第一节晶体的常识同步练习
试卷更新日期:2015-12-30 类型:同步测试
一、选择题
-
1. 下列关于晶体的说法中,不正确的是( )A、凡具有规则几何外形的固体一定是晶体 B、晶体内部粒子按一定规律周期性重复排列 C、晶胞是晶体结构的基本单元 D、晶体尽量采用紧密堆积方式,以使其变得比较稳定2. 下列区分晶体和非晶体最可靠的科学方法是( )A、测定熔、沸点 B、观察外形 C、X射线衍射 D、比较硬度3.
某离子化合物的晶胞如图所示。阳离子位于晶胞的中心,阴离子位于晶胞的8个顶点上,则该离子化合物中阴、阳离子的个数比为( )
 A、1:8 B、1:4 C、1:2 D、1:14.
A、1:8 B、1:4 C、1:2 D、1:14.下图是a、b两种不同物质的熔化曲线,下列说法正确的是( )
 A、a是晶体 B、a是非晶体 C、b是晶体 D、a、b都是非晶体5.
A、a是晶体 B、a是非晶体 C、b是晶体 D、a、b都是非晶体5.如右图所示石墨晶体结构的每一层里平均每个最小的正六边形占有碳原子数目为( )
 A、2 B、3 C、4 D、66. 水的状态除了气、液和固态外,还有玻璃态。它是由液态水急速冷却到165K时形成的。玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述中正确的是( )A、水由液态变为玻璃态,体积缩小 B、水由液态变为玻璃态,体积膨胀 C、玻璃态是水的一种特殊状态 D、玻离态水能使X射线产生衍射7.
A、2 B、3 C、4 D、66. 水的状态除了气、液和固态外,还有玻璃态。它是由液态水急速冷却到165K时形成的。玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述中正确的是( )A、水由液态变为玻璃态,体积缩小 B、水由液态变为玻璃态,体积膨胀 C、玻璃态是水的一种特殊状态 D、玻离态水能使X射线产生衍射7.某晶体的部分结构如图所示,这种晶体中A、B、C三种粒子数之比是( )
 A、3:9:4 B、1:4:2 C、2:9:4 D、3:8:48.
A、3:9:4 B、1:4:2 C、2:9:4 D、3:8:48.如图所示,一块密度、厚度均匀的矩形被测样品,长AB为宽CD的两倍,若多用电表沿两对称轴测其电阻均为R,这块样品一定是( )
 A、金属 B、半导体 C、非晶体 D、晶体9.
A、金属 B、半导体 C、非晶体 D、晶体9.氢气是重要而洁净的能源,要利用氢气做能源,必须安全有效地储存氢气。据研究镧(La)镍(Ni)合金材料有较大的储氢容量,其晶体结构的最小单元如下图所示。则这种合金的化学式为( )
 A、LaNi6 B、LaNi3 C、LaNi4 D、LaNi510. 下列不属于晶体的特点的是( )A、一定有固定的几何外形 B、一定有各向异性 C、一定有固定的熔点 D、一定是无色透明的固体11. 下列叙述正确的是( )A、固体SiO2一定是晶体 B、晶体有固定的组成,非晶体没有固定的组成 C、晶体内部的微粒按一定规律呈周期性有序排列 D、晶体的基本结构单元(晶胞)全部是平行六面体12.
A、LaNi6 B、LaNi3 C、LaNi4 D、LaNi510. 下列不属于晶体的特点的是( )A、一定有固定的几何外形 B、一定有各向异性 C、一定有固定的熔点 D、一定是无色透明的固体11. 下列叙述正确的是( )A、固体SiO2一定是晶体 B、晶体有固定的组成,非晶体没有固定的组成 C、晶体内部的微粒按一定规律呈周期性有序排列 D、晶体的基本结构单元(晶胞)全部是平行六面体12.据晶体中的晶胞结构,判断下列晶体的化学式中不正确的是( )
 A、A B、B C、C D、D13. 下列关于晶体的说法正确的是( )A、将饱和硫酸铜溶液降温,析出的固体不是晶体 B、假宝石往往是玻璃仿造的,可以用划痕的方法鉴别宝石和玻璃制品 C、石蜡和玻璃都是非晶体,但它们都有固定的熔点 D、蓝宝石在不同方向上的硬度一定相同14. 铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶角,Ba2+处于晶胞中心,O2-处于晶胞棱边中心,则该化合物的化学式为( )A、BaPbO3 B、BaPb2O3 C、BaPbO D、BaPbO415.
A、A B、B C、C D、D13. 下列关于晶体的说法正确的是( )A、将饱和硫酸铜溶液降温,析出的固体不是晶体 B、假宝石往往是玻璃仿造的,可以用划痕的方法鉴别宝石和玻璃制品 C、石蜡和玻璃都是非晶体,但它们都有固定的熔点 D、蓝宝石在不同方向上的硬度一定相同14. 铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶角,Ba2+处于晶胞中心,O2-处于晶胞棱边中心,则该化合物的化学式为( )A、BaPbO3 B、BaPb2O3 C、BaPbO D、BaPbO415.最近发现,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该新型超导材料的一个晶胞如图所示(碳原子:●,镍原子:○,镁原子:●),则该晶体的化学式是( )
 A、Mg2CNi3 B、MgC2Ni C、MgCNi2 D、MgCNi316. 下列有关晶胞的叙述,正确的是( )A、晶胞的结构是晶体的结构 B、不同的晶体中晶胞的大小和形状都相同 C、晶胞中的任何一个粒子都属于该晶胞 D、已知晶胞的组成就可推知晶体的组成17.
A、Mg2CNi3 B、MgC2Ni C、MgCNi2 D、MgCNi316. 下列有关晶胞的叙述,正确的是( )A、晶胞的结构是晶体的结构 B、不同的晶体中晶胞的大小和形状都相同 C、晶胞中的任何一个粒子都属于该晶胞 D、已知晶胞的组成就可推知晶体的组成17.纳米材料的表面粒子数占总粒子数的比例极大,这是它有许多特殊性质的原因。假设某氯化钠纳米颗粒的大小和形状恰好与氯化钠晶胞的大小和形状相同(如图所示),则这种纳米颗粒的表面粒子数与总粒子数的比值为( )
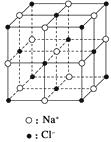 A、7∶8 B、13∶14 C、25∶25 D、26∶2718.
A、7∶8 B、13∶14 C、25∶25 D、26∶2718.纳米材料的表面粒子数占粒子总数的比例很大,这是它有许多特殊性质的原因。假设某硼镁化合物的结构如下图所示(六个硼原子位于棱柱内),则这种纳米颗粒的表面粒子数占总粒子数的百分比为( )
 A、22% B、70% C、66.7% D、33.3%19. 下列物质中属于晶体的是( )A、海盐 B、玻璃 C、陶瓷 D、胆矾20. 晶体与非晶体在微观结构上存在着本质区别,这就决定了晶体在宏观上也存在着一些不同于非晶体的独特性质,下列关于晶体性质的叙述中,不正确的是( )A、晶体的自范性指的是在适宜条件下晶体能够自发地呈现封闭规则的多面体几何外形 B、晶体的各向异性和对称性是矛盾的 C、晶体的对称性是微观粒子按一定规律做周期性重复排列的必然结果 D、晶体的各向异性直接取决于微观粒子的排列具有特定的方向性
A、22% B、70% C、66.7% D、33.3%19. 下列物质中属于晶体的是( )A、海盐 B、玻璃 C、陶瓷 D、胆矾20. 晶体与非晶体在微观结构上存在着本质区别,这就决定了晶体在宏观上也存在着一些不同于非晶体的独特性质,下列关于晶体性质的叙述中,不正确的是( )A、晶体的自范性指的是在适宜条件下晶体能够自发地呈现封闭规则的多面体几何外形 B、晶体的各向异性和对称性是矛盾的 C、晶体的对称性是微观粒子按一定规律做周期性重复排列的必然结果 D、晶体的各向异性直接取决于微观粒子的排列具有特定的方向性二、 非选择题
-
21.
已知晶体硼的基本结构单元是由硼原子组成的正二十面体(如图所示)。其中有二十个等边三角形的面和一定数目的顶点,每个顶点各有一个硼原子,则这个基本结构单元由个硼原子构成,共含有个B—B键。
 22.
22.A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,B、C、D同周期,A、D同主族,E和其他元素既不在同周期也不在同主族,B、C、D的最高价氧化物的水化物两两混合均能发生反应生成盐和水。

根据以上信息,回答下列问题。
(1)、A和D的氢化物中,沸点较低的是(选填“A”或“D”);A和B的离子中,半径较小的是(填离子符号)。(2)、元素C在元素周期表中的位置是。(3)、A和E可组成离子化合物,其晶胞结构如上图所示,阳离子(用“•”表示)位于该正方体的顶点和面心,阴离子(用“o”表示)均位于小正方体中心。该化合物的电子式是。23.如图所示,在石墨晶体中,每一层由无数个正六边形构成,试回答下列问题:
 (1)、每个正六边形实际上占有的碳原子数为个。(2)、石墨晶体每一层内碳原子数与C—C化学健之比是。(3)、ng碳原子可构成个正六边形。
(1)、每个正六边形实际上占有的碳原子数为个。(2)、石墨晶体每一层内碳原子数与C—C化学健之比是。(3)、ng碳原子可构成个正六边形。
