湖北省荆州市2019年中考化学试卷
试卷更新日期:2019-08-08 类型:中考真卷
一、单选题
-
1. 诗词是中华民族的文化瑰宝,下列诗句中隐含有化学变化的是()A、千锤万凿出深山 B、蜡炬成灰泪始干 C、只要功夫深,铁杵磨成针 D、夜来风雨声,花落知多少2. “绿水青山就是金山银山”。下列倡议不符合该理念的是()A、秸秆就地焚烧 B、合理施用化肥和农药 C、回收并集中处理废旧电池 D、用清洁能源替代化石燃料3. 下列物质不是氧化物的是()A、冰 B、干冰 C、臭氧 D、过氧化氢4. 下列关于分子的说法错误的是()A、分子在不断运动 B、分子之间有间隔 C、分子构成所有的物质 D、水分子保持水的化学性质5. 下列有关催化剂的说法正确的是()A、只能加快反应速率 B、二氧化锰在任何化学反应中都是催化剂 C、能增加生成物的质量 D、质量和化学性质在化学反应前后不变6. 下列灭火原理与“釜底抽薪”相同的是()A、锅内油着火用锅盖盖灭 B、用高压水枪喷水灭火 C、砍掉部分林木形成隔离带灭火 D、用二氧化碳灭火器灭火7. 下列实验操作中存在错误的是()A、
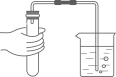 检查气密性
B、
检查气密性
B、 检验氧气
C、
检验氧气
C、 稀释浓硫酸
D、
稀释浓硫酸
D、 铁丝在氧气中燃烧
8. 已知化学反应:X+YSO4=Y+XSO4 , 根据此反应信息判断正确的是()A、X一定是金属铁 B、Y一定是金属铜 C、X的金属活动性比Y强 D、Y的金属活动性比X强9. 在pH=2的无色溶液中,下列离子能大量共存的是()A、Ba2+ 、HCO3﹣、SO42﹣ B、Ag+、Mg2+、NO3﹣ C、K+、OH﹣、CO32﹣ D、NH4+、Fe2+、Cl﹣10. 将某稀硫酸分成两等份,分别向其中加入锌粉或铁粉,反应结束后剩余的铁比剩余的锌多,产生氢气分别为ag和bg,则a和b的关系是()A、a<b B、a=b C、a>b D、无法判断11. 以下实验方案设计中,不能达到实验目的的是()
铁丝在氧气中燃烧
8. 已知化学反应:X+YSO4=Y+XSO4 , 根据此反应信息判断正确的是()A、X一定是金属铁 B、Y一定是金属铜 C、X的金属活动性比Y强 D、Y的金属活动性比X强9. 在pH=2的无色溶液中,下列离子能大量共存的是()A、Ba2+ 、HCO3﹣、SO42﹣ B、Ag+、Mg2+、NO3﹣ C、K+、OH﹣、CO32﹣ D、NH4+、Fe2+、Cl﹣10. 将某稀硫酸分成两等份,分别向其中加入锌粉或铁粉,反应结束后剩余的铁比剩余的锌多,产生氢气分别为ag和bg,则a和b的关系是()A、a<b B、a=b C、a>b D、无法判断11. 以下实验方案设计中,不能达到实验目的的是()选项
实验目的
实验方案
A
除去炭粉中少量的CuO
在空气中充分灼烧
B
分离铜粉中混有的铁粉
用磁铁靠近粉末
C
干燥二氧化碳气体
通过浓硫酸
D
鉴别硫酸钡与碳酸钡
加入足量稀硝酸
A、A B、B C、C D、D12. 由CO和SO2组成的混合气体,测得其中碳元素的质量分数是24%,则该混合气体中硫元素的质量分数是()A、16% B、18% C、20% D、22%二、填空题
-
13. 化学与生活密切相关。请回答下列问题:(1)、荆州是鱼米之乡,大米中含有的主要糖类物质是(填名称)。(2)、亚硝酸钠(NaNO2)有毒,其中氮元素的化合价为。(3)、煤炉火焰越扇越旺,是因为扇风时提供了更多的。(4)、羊毛、棉花、腈纶中属于合成纤维的是。14. 用化学式或化学方程式表示:(1)、生理盐水中的溶质是。(2)、稀盐酸、稀硫酸的一些化学性质相似,是因为它们的溶液中都含有。(3)、驱动氢能汽车的能量可来源于氢气燃烧,其反应的化学方程式为。(4)、实现“险在荆江”到“美在荆江”,农林工作者用波尔多液[Ca(OH)2与CuSO4的混合物]给沿岸树木杀菌,两者反应的化学方程式为。15. 硒(Se)是一种多功能生命营养素,其原子结构示意图如下图所示。请回答下列问题:
 (1)、图中x=。(2)、硒元素与硫元素在元素周期表中处在同一个(填“横行”或“纵行”),两者化学性质相似的原因是。(3)、硒酸与氢氧化钾溶液完全反应的化学方程式为。16. 甲、乙、丙三种物质的溶解度曲线如下图所示。请回答下列问题:
(1)、图中x=。(2)、硒元素与硫元素在元素周期表中处在同一个(填“横行”或“纵行”),两者化学性质相似的原因是。(3)、硒酸与氢氧化钾溶液完全反应的化学方程式为。16. 甲、乙、丙三种物质的溶解度曲线如下图所示。请回答下列问题: (1)、在0℃~60℃之间,三种物质中溶解度受温度影响最小的是。(2)、20℃时,三种物质的溶解度由小到大的顺序为。(3)、在不改变溶液中溶质的质量分数的前提下,要使接近饱和的丙溶液变为饱和溶液,可采取的一种措施是。(4)、50℃时,将甲、乙、丙各20 g分别加入盛有50 g水的烧杯中,充分溶解,静置,然后各取上层清液m g,再降温至10℃,此时三种溶液中溶质的质量分数分别为ω(甲)、ω(乙)、ω(丙),则三者之间的大小关系是。
(1)、在0℃~60℃之间,三种物质中溶解度受温度影响最小的是。(2)、20℃时,三种物质的溶解度由小到大的顺序为。(3)、在不改变溶液中溶质的质量分数的前提下,要使接近饱和的丙溶液变为饱和溶液,可采取的一种措施是。(4)、50℃时,将甲、乙、丙各20 g分别加入盛有50 g水的烧杯中,充分溶解,静置,然后各取上层清液m g,再降温至10℃,此时三种溶液中溶质的质量分数分别为ω(甲)、ω(乙)、ω(丙),则三者之间的大小关系是。三、推断题
-
17. A,B,C,D都是九年级化学教材中较常见的物质,它们存在下图所示的转化关系(反应条件略去)。
 (1)、若A为较活泼金属,C为气体单质,则该反应的基本反应类型是。(2)、分别写出一个符合下列要求的化学方程式。
(1)、若A为较活泼金属,C为气体单质,则该反应的基本反应类型是。(2)、分别写出一个符合下列要求的化学方程式。①若C为金属单质,A、B、D都是化合物:。
②若A是最简单的有机物,C为水,。
(3)、若A为蓝色溶液,生成的C、D都是沉淀,则B可能是。四、实验题
-
18. 根据下图回答问题:
 (1)、酒精灯加热时,应用温度最高的焰。(2)、实验室制取二氧化碳时,选择的发生装置和收集装置依次是(填字母),该反应的化学方程式是。(3)、实验室用装置A作为制取氧气的发生装置,反应结束后,若要分离出MnO2 , 除A~F中相关仪器外,还需补充的一种玻璃仪器是(写名称)。
(1)、酒精灯加热时,应用温度最高的焰。(2)、实验室制取二氧化碳时,选择的发生装置和收集装置依次是(填字母),该反应的化学方程式是。(3)、实验室用装置A作为制取氧气的发生装置,反应结束后,若要分离出MnO2 , 除A~F中相关仪器外,还需补充的一种玻璃仪器是(写名称)。五、科学探究题
-
19. 现有一瓶无色溶液,溶质可能是KOH、K2CO3中的一种或两种,某兴趣小组对其成分进行如下实验探究:
(查阅资料)①KOH与NaOH的化学性质相似,K2CO3与Na2CO3的化学性质相似。②K2CO3溶液呈碱性,BaCl2溶液、CaCl2溶液、KCl溶液呈中性。
(实验探究)设计并进行实验
实验操作步骤
实验现象
实验结论
⑴向盛有少量样品溶液的试管中加入过量CaCl2溶液
肯定含有K2CO3
⑵将操作(1)后的试管静置,再向上层清液中加入几滴酚酞溶液
酚酞溶液变红色
肯定含有
(评价反思)①甲同学提出操作(1)加入的CaCl2溶液必须过量,其目的是证明K2CO3存在的同时还要。
②乙同学提出操作(1)在溶液较浓时,没有K2CO3也能产生相同现象,其原因是;建议改加过量的BaCl2溶液,BaCl2参加反应的化学方程式为。
(拓展应用)KOH和K2CO3的混合溶液敞口久置后可能变成K2CO3溶液,反应的化学方程式为。
六、计算题
-
20. 向盛有Fe2O3粉末的烧杯中加入过量的稀H2SO4 , 充分搅拌,粉末完全溶解;再向所得溶液中逐滴加入NaOH溶液,生成沉淀与加入NaOH溶液之间的质量关系如图所示。请回答下列问题:
 (1)、写出AB段内反应的化学方程式:。(2)、加入NaOH溶液40g时溶液中存在的溶质是(写化学式)。(3)、计算氢氧化钠溶液中溶质的质量分数。(要求写出计算过程)
(1)、写出AB段内反应的化学方程式:。(2)、加入NaOH溶液40g时溶液中存在的溶质是(写化学式)。(3)、计算氢氧化钠溶液中溶质的质量分数。(要求写出计算过程)
-
-
-