广西梧州市2019年中考化学试卷
试卷更新日期:2019-08-08 类型:中考真卷
一、单选题
-
1. 2019年世界地球日主题为“珍爱美丽地球、守护自然资源”。下列做法不符合这一主题的是()A、将垃圾分类回收再利用 B、利用风能发电 C、将生活污水直接排放到河中 D、减少使用塑料袋2. 空气中体积分数约占78%的气体是()A、稀有气体 B、二氧化碳 C、氧气 D、氮气3. 我们生活在一个不断变化的物质世界里。下列属于化学变化的是()A、镁条燃烧 B、试管破裂 C、酒精挥发 D、水结成冰4. 下列实验操作错误的是()A、
 点燃酒精灯
B、
点燃酒精灯
B、 滴加溶液
C、
滴加溶液
C、 加热液体
D、
加热液体
D、 取少量固体
5. 下列有关氧气的说法错误的是()A、能燃烧 B、无色 C、无味 D、能供给呼吸6. 下列物质中,属于化合物的是()A、氯酸钾 B、硬水 C、黄铜 D、臭氧7. 某农技站货架上待售的化肥有CO(NH2)2 , 它属于化肥中的()A、磷肥 B、氮肥 C、钾肥 D、复合肥8. 下列生活中常见的物质,分别取少量放入水中,不能形成溶液的是()A、食醋 B、食盐 C、白糖 D、植物油9. 明代宋应星所著的《天工开物》中记载的炼锡方法,用化学方程式表示为:SnO2+2C Sn+2CO↑,该反应属于()A、置换反应 B、分解反应 C、化合反应 D、复分解反应10. 法国当地时间2019年4月15日,巴黎圣母院塔楼发生火灾,中空结构的木质塔尖剧烈燃烧而坍塌。下列关于该事件说法错误的是()A、木材是可燃物 B、用水灭火前要先切断电源 C、水能灭火是因为水降低了可燃物的着火点 D、塔尖剧烈燃烧的原因之一是木材与空气的接触面积大11. 如图是电解水的微观示意图,从中获得的信息错误的是()
取少量固体
5. 下列有关氧气的说法错误的是()A、能燃烧 B、无色 C、无味 D、能供给呼吸6. 下列物质中,属于化合物的是()A、氯酸钾 B、硬水 C、黄铜 D、臭氧7. 某农技站货架上待售的化肥有CO(NH2)2 , 它属于化肥中的()A、磷肥 B、氮肥 C、钾肥 D、复合肥8. 下列生活中常见的物质,分别取少量放入水中,不能形成溶液的是()A、食醋 B、食盐 C、白糖 D、植物油9. 明代宋应星所著的《天工开物》中记载的炼锡方法,用化学方程式表示为:SnO2+2C Sn+2CO↑,该反应属于()A、置换反应 B、分解反应 C、化合反应 D、复分解反应10. 法国当地时间2019年4月15日,巴黎圣母院塔楼发生火灾,中空结构的木质塔尖剧烈燃烧而坍塌。下列关于该事件说法错误的是()A、木材是可燃物 B、用水灭火前要先切断电源 C、水能灭火是因为水降低了可燃物的着火点 D、塔尖剧烈燃烧的原因之一是木材与空气的接触面积大11. 如图是电解水的微观示意图,从中获得的信息错误的是()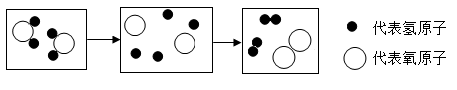 A、生成物中有2种单质 B、反应前后原子的种类、数目均不变 C、该反应说明水是由氢气和氧气组成的 D、化学变化中分子可以分成原子,原子可重新结合成新的分子12. 下列有关实验操作或现象的描述正确的是()A、用湿润的pH试纸测定盐酸的pH B、磷在氧气中剧烈燃烧,产生大量白烟 C、红热的铁丝在空气中剧烈燃烧,火星四射 D、稀释浓硫酸时,将水注入浓硫酸中并不断搅拌13. 下列有关碳和碳的化合物说法错误的是()A、植物光合作用吸收二氧化碳 B、可燃冰的主要成分是甲烷水合物 C、二氧化碳与一氧化碳都可以用于灭火 D、煤的综合利用措施主要有煤的气化、焦化和液化14. 下列关于碳酸钠与碳酸氢钠的说法错误的是()A、 溶液呈碱性 B、 固体难溶于水 C、“纯碱”是碳酸钠的俗名 D、 可用于烘焙糕点15. 金属铝的冶炼要用到冰晶石,制备冰晶石的化学方程式为(冰晶石用A表示):12HF+3Na2CO3+2Al(OH)3=2A+3CO2+9H2O,则A的化学式为()A、 B、 C、 D、16. a、b、c三种不含结晶水的物质的溶解度曲线如图,下列说法正确的是()
A、生成物中有2种单质 B、反应前后原子的种类、数目均不变 C、该反应说明水是由氢气和氧气组成的 D、化学变化中分子可以分成原子,原子可重新结合成新的分子12. 下列有关实验操作或现象的描述正确的是()A、用湿润的pH试纸测定盐酸的pH B、磷在氧气中剧烈燃烧,产生大量白烟 C、红热的铁丝在空气中剧烈燃烧,火星四射 D、稀释浓硫酸时,将水注入浓硫酸中并不断搅拌13. 下列有关碳和碳的化合物说法错误的是()A、植物光合作用吸收二氧化碳 B、可燃冰的主要成分是甲烷水合物 C、二氧化碳与一氧化碳都可以用于灭火 D、煤的综合利用措施主要有煤的气化、焦化和液化14. 下列关于碳酸钠与碳酸氢钠的说法错误的是()A、 溶液呈碱性 B、 固体难溶于水 C、“纯碱”是碳酸钠的俗名 D、 可用于烘焙糕点15. 金属铝的冶炼要用到冰晶石,制备冰晶石的化学方程式为(冰晶石用A表示):12HF+3Na2CO3+2Al(OH)3=2A+3CO2+9H2O,则A的化学式为()A、 B、 C、 D、16. a、b、c三种不含结晶水的物质的溶解度曲线如图,下列说法正确的是() A、a的溶解度大于b的溶解度 B、将a的溶液由 降温到 ,一定有晶体析出 C、 时,50g的a溶于50g水,溶液的质量分数为 D、c的饱和溶液由 降温到 ,溶液的质量分数不变17. 关于配制50g8%的氢氧化钠溶液,下列说法正确的是()A、用量筒量取 水 B、将氢氧化钠固体放在小烧杯中称量 C、把称量好的氢氧化钠固体放入量筒中溶解 D、配制好的溶液存放在带玻璃塞的广口瓶中18. 下列各组物质的水溶液,不用其他试剂就能鉴别出来的是()A、 、NaCl、 、HCl B、NaOH、 、 、KOH C、 、KCl、 、 D、NaCl、 、 、NaOH19. 为除去粗盐中的泥沙、Ca2+、Mg2+、SO42-等杂质,可将粗盐溶于水,再进行下列五步操作:①过滤②加过量的氢氧化钠溶液③加适量盐酸④加过量的碳酸钠溶液⑤加过量的氯化钡溶液。正确的操作顺序是()A、④⑤②①③ B、②④⑤①③ C、②⑤④①③ D、⑤②④③①20. 一定条件下,在密闭容器内发生了某反应,测得反应前后各物质的质量如下:
A、a的溶解度大于b的溶解度 B、将a的溶液由 降温到 ,一定有晶体析出 C、 时,50g的a溶于50g水,溶液的质量分数为 D、c的饱和溶液由 降温到 ,溶液的质量分数不变17. 关于配制50g8%的氢氧化钠溶液,下列说法正确的是()A、用量筒量取 水 B、将氢氧化钠固体放在小烧杯中称量 C、把称量好的氢氧化钠固体放入量筒中溶解 D、配制好的溶液存放在带玻璃塞的广口瓶中18. 下列各组物质的水溶液,不用其他试剂就能鉴别出来的是()A、 、NaCl、 、HCl B、NaOH、 、 、KOH C、 、KCl、 、 D、NaCl、 、 、NaOH19. 为除去粗盐中的泥沙、Ca2+、Mg2+、SO42-等杂质,可将粗盐溶于水,再进行下列五步操作:①过滤②加过量的氢氧化钠溶液③加适量盐酸④加过量的碳酸钠溶液⑤加过量的氯化钡溶液。正确的操作顺序是()A、④⑤②①③ B、②④⑤①③ C、②⑤④①③ D、⑤②④③①20. 一定条件下,在密闭容器内发生了某反应,测得反应前后各物质的质量如下:物质
a
b
c
d
反应前的质量/g
10
15
20
1
反应后的质量/g
0
10
x
y
下列说法错误的是()
A、d可能是该反应的催化剂 B、c的质量范围一定是:0≤x≤30 C、参加反应的a与b的质量之比一定为2:1 D、若16≤y≤36,则该反应一定是化合反应二、填空题
-
21. 请用化学用语填写下列空白,注意按示例要求书写大小写。示例:Ag+(1)、锌元素;(2)、2个氢氧根离子;(3)、氯化镁;(4)、3个五氧化二磷分子。22. 梧州市冰泉豆浆以“香、滑、浓”独具风味,驰名中外。下面是某品牌豆浆的营养成分表。请回答:
成分
蛋白质
油脂
糖类
钙
铁
维生素
质量分数(%)
1.8
0.7
1.1
0.01
0.0005
0.015
(1)、表中含有人体所需要的微量元素是。(2)、维生素有多种,每种都有独特功能。若人体缺乏维生素 , 会引起坏血病。(3)、豆浆中的在消化道内逐渐被分解成可被人体吸收的多种氨基酸。(4)、淀粉属于糖类,在淀粉溶液中加入几滴碘水,溶液会变色。23. 聚合物锂离子电池被誉为“21世纪的电池”,如图是元素周期表中锂元素的相关信息。请回答下列问题: (1)、该元素位于元素周期表中第周期,在化学反应中容易(填“得到”或“失去”)电子。(2)、该元素与第8号元素组成的化合物的化学式是。(3)、利用锂与水的反应可制成锂水电池,作为潜艇的储备电源。已知锂与水反应生成一种碱和一种可燃性气体,请写出该反应的化学反应方程式。
(1)、该元素位于元素周期表中第周期,在化学反应中容易(填“得到”或“失去”)电子。(2)、该元素与第8号元素组成的化合物的化学式是。(3)、利用锂与水的反应可制成锂水电池,作为潜艇的储备电源。已知锂与水反应生成一种碱和一种可燃性气体,请写出该反应的化学反应方程式。三、流程题
-
24. 制备高纯硅和二氧化硅主要工艺流程如图所示。
 (1)、2019年,我国华为公司推出了5G商用芯片。制造芯片要用到高纯硅,硅属于元素(填“金属”或“非金属”)。(2)、反应①的化学方程式为:SiO2+2C Si+2CO↑,从氧化还原反应角度分析,C发生了反应。(3)、用于制造光导纤维的高纯二氧化硅,可利用反应②制备,同时生成一种可循环使用的物质,该反应的化学方程式为。整个工艺流程中,还可以循环利用的另一种物质是。
(1)、2019年,我国华为公司推出了5G商用芯片。制造芯片要用到高纯硅,硅属于元素(填“金属”或“非金属”)。(2)、反应①的化学方程式为:SiO2+2C Si+2CO↑,从氧化还原反应角度分析,C发生了反应。(3)、用于制造光导纤维的高纯二氧化硅,可利用反应②制备,同时生成一种可循环使用的物质,该反应的化学方程式为。整个工艺流程中,还可以循环利用的另一种物质是。四、计算题
-
25. 梧州市某化学兴趣小组检测某硫酸厂排放的废液中硫酸的含量,取废液样品100g,逐滴加入4%的NaOH溶液,溶液的pH随加入NaOH溶液质量变化如图所示(假设废液中其它成分均为中性,且不和NaOH反应)。

请计算:
(1)、H2O的相对分子质量=。(2)、该废液中硫酸的质量分数。(结果精确到0.01%)五、实验题
-
26. 下列是中学化学常用的仪器和装置,请回答:
 (1)、仪器①的名称是。(2)、实验室用过氧化氢溶液和二氧化锰可以制取氧气,该反应的化学方程式为。(3)、若用高锰酸钾固体为原料制取并收集氧气,正确的接口连接顺序是 , 实验前应先 , 再加入药品。实验结束时应注意先 , 再熄灭酒精灯,以防发生倒吸。
(1)、仪器①的名称是。(2)、实验室用过氧化氢溶液和二氧化锰可以制取氧气,该反应的化学方程式为。(3)、若用高锰酸钾固体为原料制取并收集氧气,正确的接口连接顺序是 , 实验前应先 , 再加入药品。实验结束时应注意先 , 再熄灭酒精灯,以防发生倒吸。六、科学探究题
-
27. 市售的“自热米饭”带有一个发热包,遇水后可迅速升温至150℃,保温时间达3小时,能将生米做成熟饭。梧州市某中学化学兴趣小组对发热包非常感兴趣,进行了以下探究。
(查阅资料)
①发热包主要由生石灰、铁粉、镁粉、铝粉、炭粉、氯化钠中的若干种组成。
②氢氧化镁和氢氧化铝均为不溶于水的白色固体,但后者可溶于NaOH溶液。
(成分探究)取出某品牌的发热包内灰黑色的固体粉末,分成两份。
(1)、小吴用磁铁靠近其中一份粉末,发现有黑色物质被磁铁吸引,证明粉末中含有。用磁铁将该物质全部吸出后,剩余粉末为样品A。(2)、小周将另一份粉末加水溶解、过滤后,取部分滤液滴入酚酞试液,滤液变色,证明原粉末中含生石灰;再向滤液中加入 , 看到白色沉淀生成,证明原粉末中含有氯化钠。(3)、除上述物质外,还可能存在镁粉、铝粉、炭粉,对此大家提出了以下几种猜想:猜想一:只存在上述三种中的一种;
猜想二:上述三种同时存在;
猜想三:存在铝粉和炭粉;
猜想四:存在镁粉和铝粉;
猜想五:。
(4)、(实验验证)小施用样品A进行实验,流程如下。向滤液B滴加氢氧化钠溶液时,他观察到开始时有白色沉淀生成,后来又全部消失,最后得到的是无色溶液E。
(实验结论)
不溶物D是。
大家结合实验现象讨论后,认为猜想正确,理由是。
(5)、(原理探究)
小吴利用如图装置证明发热包放热主要来自于生石灰与水的反应。加水后发现A中温度迅速升高,B中有气泡产生,该气体为(填名称)。但温度很快下降,说明该反应很快结束,不能长时间保温。
(猜想)大家大胆猜测应该还有其他放热反应存在。
(实验验证)
同学们按资料介绍,用铁粉、炭粉和食盐水在锥形瓶中模拟铁的锈蚀实验,不久后发现锥形瓶外壁微烫,并持续较长时间。该现象很好地解释了发热包的保温机理。
(拓展活动)
在上述铁的锈蚀实验中未观察到红色的铁锈产生。老师告诉同学们,铁锈蚀时首先生成一种碱。请写出该反应的化学方程式。
-
-
-