湖北省武汉市硚口区2018-2019学年中考化学5月模拟考试试卷
试卷更新日期:2019-08-05 类型:中考模拟
一、单选题
-
1. 下图所示实验中,验证物质的性质时,主要发生化学变化的是( )A、
 物质溶解
B、
物质溶解
B、 鲜花变色
C、
鲜花变色
C、 石墨导电
D、
石墨导电
D、 金属刻画
2. 下列说法错误的是( )A、构成物质的粒子有分子、原子和离子 B、化学反应前后分子的个数可能不改变 C、不同元素的原子,质子数、中子数和电子数一定不同 D、相同原子构成的纯净物一定是单质,离子构成的纯净物一定是化合物3. 下列说法错误的是( )A、有的元素符号表示的含义只有二种含义,但有的元素符号的含义有三种 B、一种物质中同一元素的化合价可能不同 C、氧化物、酸和碱都属于化合物且都含有氧元素 D、金刚石、石墨是碳原子构成的碳单质,而C60是由分子构成的碳单质4. 生活中处处有化学,下列说法错误的是( )A、可用肥皂水鉴别硬水和软水 B、煤、石油、天然气是不可再生能源 C、铁在潮湿的空气中易生锈 D、塑料、合成纤维、合成橡胶、合金都属于合成材料5. 下列实验能够直接用于验证质量守恒定律的是( )A、
金属刻画
2. 下列说法错误的是( )A、构成物质的粒子有分子、原子和离子 B、化学反应前后分子的个数可能不改变 C、不同元素的原子,质子数、中子数和电子数一定不同 D、相同原子构成的纯净物一定是单质,离子构成的纯净物一定是化合物3. 下列说法错误的是( )A、有的元素符号表示的含义只有二种含义,但有的元素符号的含义有三种 B、一种物质中同一元素的化合价可能不同 C、氧化物、酸和碱都属于化合物且都含有氧元素 D、金刚石、石墨是碳原子构成的碳单质,而C60是由分子构成的碳单质4. 生活中处处有化学,下列说法错误的是( )A、可用肥皂水鉴别硬水和软水 B、煤、石油、天然气是不可再生能源 C、铁在潮湿的空气中易生锈 D、塑料、合成纤维、合成橡胶、合金都属于合成材料5. 下列实验能够直接用于验证质量守恒定律的是( )A、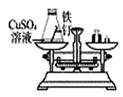 B、
B、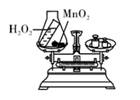 C、
C、 D、
D、 6. 某兴趣小组在老师指导下,用pH传感器测得图Ⅰ烧杯中溶液的pH随通入气体时间的变化曲线如图所示。下列说法正确的是( )
6. 某兴趣小组在老师指导下,用pH传感器测得图Ⅰ烧杯中溶液的pH随通入气体时间的变化曲线如图所示。下列说法正确的是( ) A、实验中会观察到锥形瓶中产生大量气泡,乙中澄清石灰水变浑浊 B、AB段pH不变的可能原因是甲中反应还没有开始 C、BC段发生的化学反应主要是HCl和石灰水的反应 D、D点所得溶液的成分除H2O外只有氯化钙7. 已知A,B,C,D,E是初中化学中常见的五种物质,均含有同一种元素。其中,A为单质, B和C含有相同的元素。它们在一定条件下的转化关系如图所示(“→”表示物质间的转化关系,反应条件和部分反应物、生成物已省略),根据初中所学知识判断下列说法正确的是( )
A、实验中会观察到锥形瓶中产生大量气泡,乙中澄清石灰水变浑浊 B、AB段pH不变的可能原因是甲中反应还没有开始 C、BC段发生的化学反应主要是HCl和石灰水的反应 D、D点所得溶液的成分除H2O外只有氯化钙7. 已知A,B,C,D,E是初中化学中常见的五种物质,均含有同一种元素。其中,A为单质, B和C含有相同的元素。它们在一定条件下的转化关系如图所示(“→”表示物质间的转化关系,反应条件和部分反应物、生成物已省略),根据初中所学知识判断下列说法正确的是( )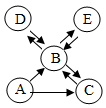 A、A→B的反应一定是化合反应 B、D和E的物质类别可以相同,也可以不同 C、若D是一种白色固体,则B→D的反应属于复分解反应 D、若C为单质, A和B含有相同的元素,其他条件不变。则D→B的反应一定是分解反应8. 夏飞同学想要用含有杂质二氧化碳、氢气和水蒸气的一氧化碳气体测定mg样品中氧化铁的质量分数。装置如图所示,连接实验装置后先通一段时间氮气,再继续实验(已知试剂均足量,样品中的杂质不参与反应也不挥发)。下列说法正确的是( )
A、A→B的反应一定是化合反应 B、D和E的物质类别可以相同,也可以不同 C、若D是一种白色固体,则B→D的反应属于复分解反应 D、若C为单质, A和B含有相同的元素,其他条件不变。则D→B的反应一定是分解反应8. 夏飞同学想要用含有杂质二氧化碳、氢气和水蒸气的一氧化碳气体测定mg样品中氧化铁的质量分数。装置如图所示,连接实验装置后先通一段时间氮气,再继续实验(已知试剂均足量,样品中的杂质不参与反应也不挥发)。下列说法正确的是( )①装置甲、乙、丁中的试剂分别是浓硫酸、氢氧化钠溶液、澄清石灰水; ②实验时先点燃丙、戊处的酒精灯,过一会再通入混合气体; ③该实验既可验证一氧化碳的还原性,又可验证一氧化碳的可燃性; ④实验中会观察到甲、丁中液体均变浑浊; ⑤实验结束后称量丙中固体质量为ng,则样品中氧化铁的质量分数为10(m-n)/3m×100% ⑥利用丁装置在反应前后改变的质量也能计算出氧化铁的质量分数
 A、①②③⑤ B、②③⑤ C、②③④⑤ D、③④⑤⑥
A、①②③⑤ B、②③⑤ C、②③④⑤ D、③④⑤⑥二、填空题
-
9. 某粒子的结构示意图如下图所示,请回答下列问题:
 (1)、如该粒子表示一种原子,则x与y的差值为(填数值);(2)、如该粒子表示一种阳离子,则该粒子的元素在元素周期表中位于第周期;(3)、写出x=8和x=13的二种元素组成的单质在常温下发生反应的化学方程式:。10. 如图是甲、乙、丙三种物质在水中的溶解度曲线.
(1)、如该粒子表示一种原子,则x与y的差值为(填数值);(2)、如该粒子表示一种阳离子,则该粒子的元素在元素周期表中位于第周期;(3)、写出x=8和x=13的二种元素组成的单质在常温下发生反应的化学方程式:。10. 如图是甲、乙、丙三种物质在水中的溶解度曲线. (1)、t2℃时,甲的溶解度为;(2)、t3℃时,等质量甲、乙、丙的饱和溶液降温到t2℃,所得溶液质量的大小关系是;(3)、t1℃时,丙的饱和溶液中含有少量的甲,现要提纯丙并得到丙的固体,可以采用的操作方法是;(4)、下列说法正确的是___________.A、将甲、乙、丙的溶液分别从t1℃升温到t2℃,不考虑水分的蒸发,则溶质质量分数可能都不变 B、t2℃时,向100g甲的饱和溶液中加入100g水,充分搅拌后溶质质量分数为10% C、t3℃时,等质量的甲、乙、丙分别制成饱和溶液,需要水的质量最多的是丙 D、t2℃时,升高丙溶液的温度,一定有晶体析出.
(1)、t2℃时,甲的溶解度为;(2)、t3℃时,等质量甲、乙、丙的饱和溶液降温到t2℃,所得溶液质量的大小关系是;(3)、t1℃时,丙的饱和溶液中含有少量的甲,现要提纯丙并得到丙的固体,可以采用的操作方法是;(4)、下列说法正确的是___________.A、将甲、乙、丙的溶液分别从t1℃升温到t2℃,不考虑水分的蒸发,则溶质质量分数可能都不变 B、t2℃时,向100g甲的饱和溶液中加入100g水,充分搅拌后溶质质量分数为10% C、t3℃时,等质量的甲、乙、丙分别制成饱和溶液,需要水的质量最多的是丙 D、t2℃时,升高丙溶液的温度,一定有晶体析出.三、流程题
-
11. 有一包固体粉末A,可能含有Mg、Al2O3、CuO、NaCl、Na2CO3、NaOH中的一种或几种,为探究其成分,甲同学取少量的A做如下实验,现象如图所示。

根据实验过程中的现象判断:
(1)、写出生成沉淀G的化学方程式是。(2)、混合物A中一定有。(3)、溶液F中,一定存在溶质是。(4)、滤液B中,可能存在的溶质是 , 若要证明该物质是否存在,应补做实验是(写出主要实验步骤、现象及结论,如有多种任选一种即可)。四、计算题
-
12. 绿矾(FeSO4·nH2O)是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。绿矾不稳定,加热时会失去结晶水生成硫酸亚铁,硫酸亚铁在空气中易被氧化。某化学兴趣小组为测定绿矾中结晶水的含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。称重B装置,记为 n1 g。(已知碱石灰是氧化钙和氢氧化钠的混合物)

实验步骤如下:
Ⅰ.打开K1和K2 , 缓缓通入N2一段时间后连接好装置,关闭K1;Ⅱ.点燃酒精灯,加热一段时间;Ⅲ.熄灭酒精灯;Ⅳ. ………称量A的质量为m3g,称量B的质量为n2g.
回答下列问题:
(1)、步骤Ⅳ中“………”的具体操作是。(2)、装置B中发生反应的化学方程式为。(3)、根据实验记录,如只选择装置A的数据计算绿矾中结晶水的百分含量为(列式表示)。(4)、如选择实验前后B装置数据计算,则装置C的作用是 。若两组数据的计算结果都偏小,则可能的共同原因是。13. 某纯碱样品中含有杂质NaCl,为测定该样品中Na2CO3的质量分数,称取纯碱样品13.4 g,向其中逐渐加入稀盐酸,如图是产生的气体质量与加入稀盐酸质量的关系图。 (1)、当加入稀盐酸40.0 g时,所得溶液中溶质的成分是(写化学式)。(2)、恰好反应后所得溶液中溶质的质量分数。(写出计算过程,结果精确到0.1%)。
(1)、当加入稀盐酸40.0 g时,所得溶液中溶质的成分是(写化学式)。(2)、恰好反应后所得溶液中溶质的质量分数。(写出计算过程,结果精确到0.1%)。
-