河南省安阳市2018-2019学年中考化学一模考试试卷
试卷更新日期:2019-08-05 类型:中考模拟
一、单选题
-
1. 下列物质的性质,属于化学性质的是( )A、吸附性 B、溶解性 C、挥发性 D、氧化性2. “绿水青山就是金山银山”。下列物质的大量排放不违背该理念的是( )A、氮气 B、二氧化硫 C、固体粉尘 D、工业废水3. 某品牌的小食品贴有如图所示的标签,从营养均衡的角度分析,该食品还缺少的营养素是( )
 A、油脂 B、糖类 C、维生素 D、蛋白质4. 构成下列物质的微粒与构成干冰的微粒种类相同的是( )A、铜 B、液氧 C、金刚石 D、氯化钠5. 下列操作错误的是( )A、
A、油脂 B、糖类 C、维生素 D、蛋白质4. 构成下列物质的微粒与构成干冰的微粒种类相同的是( )A、铜 B、液氧 C、金刚石 D、氯化钠5. 下列操作错误的是( )A、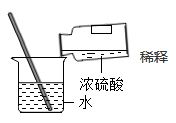 稀释
B、
稀释
B、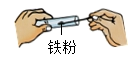 取药
C、
取药
C、 称量
D、
称量
D、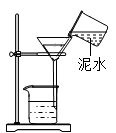 过滤
6. 下列关于水的说法正确的是( )A、冰水共存物属于混合物 B、凡是有水生成的反应一定是中和反应 C、生活中常用煮沸的方法降低水的硬度 D、电解水实验中,正负电极产生的气体体积比约为2:17. 打开盛有浓氨水的试剂瓶,会闻到刺激性气味,其原因是( )A、分子间有间隔 B、分子的质量很小 C、分子分解成原子 D、分子在不断运动8. 有元素化合价升降的反应属于氧化还原反应。下列反应一定是氧化还原反应的是( )A、化合反应 B、置换反应 C、分解反应 D、复分解反应9. 下列鉴别两种不同物质所用试剂或方法,错误的是( )A、CO2与O2:燃着的木条 B、棉线与羊毛线:点燃 C、硫酸与硫酸钠溶液:加酚酞溶液 D、KNO3和NH4NO3:加熟石灰研磨10. 下列除杂试剂错误的是( )A、氮气中氧气(碳) B、铜粉中氧化铜(一氧化碳) C、碳酸钙中的氯化钙(水) D、氯化钠溶液中的硫酸铜(氢氧化钡)11. 实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致结果偏大的是( )
过滤
6. 下列关于水的说法正确的是( )A、冰水共存物属于混合物 B、凡是有水生成的反应一定是中和反应 C、生活中常用煮沸的方法降低水的硬度 D、电解水实验中,正负电极产生的气体体积比约为2:17. 打开盛有浓氨水的试剂瓶,会闻到刺激性气味,其原因是( )A、分子间有间隔 B、分子的质量很小 C、分子分解成原子 D、分子在不断运动8. 有元素化合价升降的反应属于氧化还原反应。下列反应一定是氧化还原反应的是( )A、化合反应 B、置换反应 C、分解反应 D、复分解反应9. 下列鉴别两种不同物质所用试剂或方法,错误的是( )A、CO2与O2:燃着的木条 B、棉线与羊毛线:点燃 C、硫酸与硫酸钠溶液:加酚酞溶液 D、KNO3和NH4NO3:加熟石灰研磨10. 下列除杂试剂错误的是( )A、氮气中氧气(碳) B、铜粉中氧化铜(一氧化碳) C、碳酸钙中的氯化钙(水) D、氯化钠溶液中的硫酸铜(氢氧化钡)11. 实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致结果偏大的是( )①称量的氯化钠固体中含有不溶性杂质;②用量筒量取水时俯视读数;
③往烧杯中加水时有水洒出;④将配制好的溶液装入试剂瓶中时有少量溅出。
A、①② B、②③ C、②④ D、③④12. 实验小组用传感器探究稀NaOH溶液与稀盐酸反应过程中温度和pH的变化,测定结果如下图所示。下列说法错误的是( ) A、反应过程中有热量放出 B、30 s时,溶液中溶质为HCl和NaCl C、从20 s到40 s,溶液温度升高、pH增大 D、该实验是将稀盐酸滴入稀NaOH溶液中13. 如图中“﹣”表示相连的物质之间可以发生反应,“→”表示一种物质可以转化成另一种物质,下列各组物质按甲、乙、丙的顺序不符合图示要求的是( )
A、反应过程中有热量放出 B、30 s时,溶液中溶质为HCl和NaCl C、从20 s到40 s,溶液温度升高、pH增大 D、该实验是将稀盐酸滴入稀NaOH溶液中13. 如图中“﹣”表示相连的物质之间可以发生反应,“→”表示一种物质可以转化成另一种物质,下列各组物质按甲、乙、丙的顺序不符合图示要求的是( )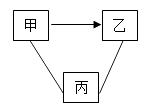 A、C、CO、O2 B、Mg、MgCl2、ZnSO4 C、Ca(OH)2、CaCl2、Na2CO3 D、BaCl2、BaCO3、H2SO414. 有一包Mg和MgO的混合物共12.8 g,与一定量的稀硫酸恰好完全反应,所得溶液中溶质的质量为48 g,则原混合物中氧元素的质量为( )A、1.6 g B、2.4 g C、3.2 g D、9.6 g
A、C、CO、O2 B、Mg、MgCl2、ZnSO4 C、Ca(OH)2、CaCl2、Na2CO3 D、BaCl2、BaCO3、H2SO414. 有一包Mg和MgO的混合物共12.8 g,与一定量的稀硫酸恰好完全反应,所得溶液中溶质的质量为48 g,则原混合物中氧元素的质量为( )A、1.6 g B、2.4 g C、3.2 g D、9.6 g二、填空题
-
15. 硒是人体必需微量元素之一,其元素符号为;尿素能使植物叶色浓绿,其化学式为。16. 燃烧与我们的生活密切相关。油锅中的油着火时可用锅盖盖灭,其原理是;乙醇完全燃烧的化学方程式为;相同质量的煤粉比煤块燃烧得更快、更剧烈,其原因是。17. 硅是制造芯片的重要材料。由下图可知,硅的相对原子质量为 , 其原子结构示意图为。
 18. A,B,C三种固体物质的溶解度曲线如图所示,请回答:当A中混有少量B时,可采用方法提纯 A物质。t2℃时,将75 g A的饱和溶液稀释为20%的溶液,需加水的质量为g.t2 ℃时,将A、B、C三种物质的饱和溶液降温至t1 ℃,所得溶液溶质的质量分数由大到小的顺序为。
18. A,B,C三种固体物质的溶解度曲线如图所示,请回答:当A中混有少量B时,可采用方法提纯 A物质。t2℃时,将75 g A的饱和溶液稀释为20%的溶液,需加水的质量为g.t2 ℃时,将A、B、C三种物质的饱和溶液降温至t1 ℃,所得溶液溶质的质量分数由大到小的顺序为。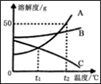 19. 碳酸氢钠受热易分解,生成碳酸钠、水和二氧化碳,反应的化学方程式为 , 充分加热10 g含碳酸钠的碳酸氢钠固体,反应前后固体中钠元素的质量分数之比为7:10,则生成水和二氧化碳的质量之和为g。20. 如图是某反应的微观示意图。
19. 碳酸氢钠受热易分解,生成碳酸钠、水和二氧化碳,反应的化学方程式为 , 充分加热10 g含碳酸钠的碳酸氢钠固体,反应前后固体中钠元素的质量分数之比为7:10,则生成水和二氧化碳的质量之和为g。20. 如图是某反应的微观示意图。 (1)、写出反应前后化合价没有改变的元素。(2)、写出该反应的化学方程式。
(1)、写出反应前后化合价没有改变的元素。(2)、写出该反应的化学方程式。三、推断题
-
21. A~D是四种不同种类的物质,其中A可用于金属除锈,B难溶于水。它们相互之间的关系如图所示(部分物质已略去)。

则A的化学式为;A 与D反应的实质为;A→B的化学方程式为;C与D反应的化学方程式为(合理即可)。
四、简答题
-
22. 向含有Cu(NO3)2和AgNO3的混合溶液中加入一定量的锌粉,充分反应后过滤,过滤后所得固体的质量等于加入的锌粉的质量。(1)、写出一个相关反应的化学方程式。(2)、请分析过滤所得固体物质中的成分。
五、实验题
-
23. 已知甲酸(HCOOH)具有挥发性,在热的浓硫酸中分解生成一氧化碳和水。用下图所示实验装置制取CO,然后用CO还原Fe3O4 , 并检验气体产物。
 (1)、氢氧化钠固体的作用是什么?(2)、写出B中Fe3O4发生反应的化学方程式。(3)、C中观察到的现象是什么?24. 化学是以实验为基础的科学,实验是科学探究的重要手段。(1)、下列实验仪器中不能用于加热的是(填字母代号)。
(1)、氢氧化钠固体的作用是什么?(2)、写出B中Fe3O4发生反应的化学方程式。(3)、C中观察到的现象是什么?24. 化学是以实验为基础的科学,实验是科学探究的重要手段。(1)、下列实验仪器中不能用于加热的是(填字母代号)。a烧杯 b量筒 c试管 d蒸发皿
(2)、某化学小组用如图所示装置制取O2。
①写出A装置中发生反应的化学方程式。
②A装置中长颈漏斗下端浸没在液面以下的原因是什么?
③用A装置还可以制取CO2 , 写出反应的化学方程式。
④若用B装置采用排空气法收集氧气,请将B装置中导管补画完整。
(3)、向某盐酸和氯化镁的混合溶液中加入氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。
①可用测a点溶液的酸碱度。
②bc段(不含b点) 反应的化学方程式为。
(4)、加热15 g 氯酸钾和二氧化锰的固体混合物制取氧气,待反应完全后,可以得到10.2 g 固体物质。请计算原固体混合物中氯酸钾的质量。六、流程题
-
25. 有一包由KCl、MgSO4和CaCl2组成的固体混合物,为了除去其中的MgSO4和CaCl2 , 得到纯净的KCl,设计如下实验方案:
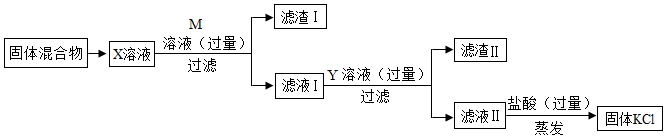 (1)、M溶液中的溶质是什么?(2)、请设计实验证明滤液Ⅱ中除KCl外的其他溶质。(写出实验步骤和现象)(3)、最后所得KCl的质量大于原固体中KCl的质量,写出一个可使KCl质量增加的化学方程式。
(1)、M溶液中的溶质是什么?(2)、请设计实验证明滤液Ⅱ中除KCl外的其他溶质。(写出实验步骤和现象)(3)、最后所得KCl的质量大于原固体中KCl的质量,写出一个可使KCl质量增加的化学方程式。
-
-