安徽省阜阳市临泉县2018-2019学年中考化学模拟考试试卷
试卷更新日期:2019-07-30 类型:中考模拟
一、单选题
-
1. 不列入目前我国城市空气质量监测项目的物质是( )A、可吸入颗粒物 B、二氧化碳 C、二氧化硫 D、二氧化氮2. 下列实验操作中,正确的是( )A、
 加热液体
B、
加热液体
B、 检查装置气密性
C、
检查装置气密性
C、 检验二氧化碳是否集满
D、
检验二氧化碳是否集满
D、 除去水中的泥沙
3. 2018年年初,我省各地普降暴雪,一些地方使用了融雪剂用于消除道路积雪、结冰。乙酸钾(CH3COOK)是一种环保融雪剂,下列关于乙酸钾的说法中正确的是( )A、是氧化物 B、C,H,O,K的质量比为2:3:2:1 C、由三种非金属和一种金属组成 D、组成中氢元素的质量分数最小4. 普通电动车使用的电池一般是铅蓄电池,铅蓄电池在放电时会不断生成PbSO4 , 已知在PbSO4 , 中硫元素的化合价为+6,则Pb的化合价是( )A、 B、 C、 D、5. 钪常用来制特种玻璃。该元素的相关信息如图所示,下列有关说法正确的是( )
除去水中的泥沙
3. 2018年年初,我省各地普降暴雪,一些地方使用了融雪剂用于消除道路积雪、结冰。乙酸钾(CH3COOK)是一种环保融雪剂,下列关于乙酸钾的说法中正确的是( )A、是氧化物 B、C,H,O,K的质量比为2:3:2:1 C、由三种非金属和一种金属组成 D、组成中氢元素的质量分数最小4. 普通电动车使用的电池一般是铅蓄电池,铅蓄电池在放电时会不断生成PbSO4 , 已知在PbSO4 , 中硫元素的化合价为+6,则Pb的化合价是( )A、 B、 C、 D、5. 钪常用来制特种玻璃。该元素的相关信息如图所示,下列有关说法正确的是( ) A、质子数为21 B、中子数为21 C、钪属于非金属元素 D、相对原子质量为6. 某物质燃烧的微观示意图如图,下列有关叙述正确的是( )
A、质子数为21 B、中子数为21 C、钪属于非金属元素 D、相对原子质量为6. 某物质燃烧的微观示意图如图,下列有关叙述正确的是( ) A、该反应为化合反应 B、反应前后原子的数目发生了改变 C、反应中甲、乙两物质的分子个数之比为1:1 D、反应物和生成物都是由分子构成的7. 推理是化学学习中常用的思维方法,以下推理正确的是( )A、离子是带电的微粒,所以带电的微粒都是离子 B、含碳元素的物质完全燃烧会生成 ,因此燃烧生成 的物质一定含碳元素 C、燃烧一般伴随有发光、放热现象,所以有发光、放热现象的变化就是燃烧 D、单质只含有一种元素,所以只含有一种元素的物质一定是单质8. 把一定质量的甲,乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量分数变化如图所示。下列说法中错误的是( )
A、该反应为化合反应 B、反应前后原子的数目发生了改变 C、反应中甲、乙两物质的分子个数之比为1:1 D、反应物和生成物都是由分子构成的7. 推理是化学学习中常用的思维方法,以下推理正确的是( )A、离子是带电的微粒,所以带电的微粒都是离子 B、含碳元素的物质完全燃烧会生成 ,因此燃烧生成 的物质一定含碳元素 C、燃烧一般伴随有发光、放热现象,所以有发光、放热现象的变化就是燃烧 D、单质只含有一种元素,所以只含有一种元素的物质一定是单质8. 把一定质量的甲,乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量分数变化如图所示。下列说法中错误的是( ) A、该反应为分解反应 B、乙可能是此反应的催化剂 C、参加反应的甲、丁的质量之比为9:1 D、丁一定是化合物,甲、丙可能是单质9. 依据下列20℃时的实验和数据回答。已知20℃时,NaCl和NaNO3的溶解度分别为36g和88g。
A、该反应为分解反应 B、乙可能是此反应的催化剂 C、参加反应的甲、丁的质量之比为9:1 D、丁一定是化合物,甲、丙可能是单质9. 依据下列20℃时的实验和数据回答。已知20℃时,NaCl和NaNO3的溶解度分别为36g和88g。
序号
①
②
③
④
⑤
固体种类
NaCl
NaCl
NaNO3
NaNO3
NaNO3
固体的质量/g
30
60
30
60
90
水的质量/g
100
100
100
100
100
下列关于①~⑤所得溶液的说法错误的是( )
A、溶质质量: B、溶液质量: C、溶质质量分数:①=③ D、⑤中溶质与溶剂的质量比为9:1010. 用相同质量的镁和铁分别与稀盐酸反应,横坐标表示加入盐酸的体积,则生成氢气的质量符合实际的是( )A、 B、
B、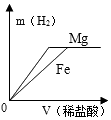 C、
C、 D、
D、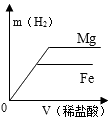
二、多选题
-
11. 现代社会对能量的需求越来越大,下列活动中通过化学反应提供能量的是( )A、
 蓄电池放电
B、
蓄电池放电
B、 水力力电
C、
水力力电
C、 太阳能供热
D、
太阳能供热
D、 火箭点火升空
火箭点火升空
三、填空题
-
12. 水是生命之源,也是人类最宝贵的资源。请回答下列问题:(1)、实验室电解水的方程式为:;说明水是由氢、氧两种元素组成的化合物。(2)、下列物质中属于纯净物的是(填字母序号)。
A海水 B冰水混合物 C自来水 D河水
(3)、区分硬水和软水可用;生活中,人们常采用的方法,既降低水的硬度,又杀菌消毒。(4)、如图是“国家节水标志”,请你列举一种生活中具体的节水措施:。
四、计算题
-
13. 为测定鸡蛋壳中CaCO3的质量分数,取9.0g干燥的碎鸡蛋壳放入烧杯中,向其中加入足量的稀盐酸40.0g(假设其他物质不与盐酸反应,且盐酸与水均不挥发,生成的气体全部逸出)。充分反应后烧杯中物质的总质量为46.8g。请计算:(1)、产生气体的质量是;(2)、鸡蛋壳中CaCO3的质量分数是(结果保留1位小数)。
五、实验题
-
14. 根据下列装置,结合所学化学知识回答下列问题。
 (1)、写出仪器a的名称。(2)、实验室用高锰酸钾制取氧气时发生反应的化学方程式为:;为制得较为干燥的氧气,应选择的制取与收集装置是(填字母序号),该套装置(填“能”或“不能”)用于实验室制取二氧化碳。(3)、某同学将制得的二氧化碳通入B装置中,观察到的现象是 , 反应的方程式为。
(1)、写出仪器a的名称。(2)、实验室用高锰酸钾制取氧气时发生反应的化学方程式为:;为制得较为干燥的氧气,应选择的制取与收集装置是(填字母序号),该套装置(填“能”或“不能”)用于实验室制取二氧化碳。(3)、某同学将制得的二氧化碳通入B装置中,观察到的现象是 , 反应的方程式为。六、科学探究题
-
15.(1)、实验室用过氧化氢与二氧化锰制取氧气的化学方程式为: , 加入二氧化锰是为了。(2)、如表是某研究小组探究影响化学反应速率的因素的相关实验数据:(每次实验取用含碳酸钙60%的大理石10 g.每次实验盐酸的用量为20mL,大理石中杂质不与盐酸反应)。
实验编号
温度/℃
大理石规格
盐酸的质量分数
完全反应的时间/s
a
20
粗颗粒
18.25%
130
b
粗颗粒
9.125%
205
c
30
粗颗粒
18.25%
63
d
20
细颗粒
18.25%
95
(实验目的)
①实验a和b探究大理石颗粒大小相同下盐酸的质量分数对该反应速率的影响,则实验b中的温度应该为。
②实验a和c探究对该反应速率的影响。
③实验a和探究大理石颗粒大小对该反应速率的影响。
④根据表格中的数据写出2个与实验目的相对应的实验结论:
16. 实验室保存有一瓶淡黄色固体药品,标签上的药品名称为“过氧化钠(Na2O2),但是已经过了保质期。某化学兴趣小组想知道这瓶固体究竟含有哪些物质。他们在老师的指导下进行了实验探究,请你完成兴趣小组的下列实验报告。(查阅资料)
Ⅰ.过氧化钠是一种淡黄色固体,常用在呼吸面具和潜艇中制造氧气。其原理是:2Na2O2+2CO2═2Na2CO3+O2 2Na2O2+2H2O═4NaOH+O2↑
Ⅱ.常温常压下,O2和CO2的密度分别为1.3g/L、1.8g/L。
(分析猜想)
(1)、该小组同学认为,不用做实验,仅由查得的资料和所学知识就可推断该固体一定含有Na2O2 . 理由是。(2)、进一步对固体成分提出以下猜想:Ⅰ.只有Na2O2;Ⅱ.含有Na2O2和Na2CO3两种物质;
Ⅲ.含有两种物质;Ⅳ.含有。
(3)、(实验操作)首先按如图连接好装置。用电子秤称取 1.00g 固体样品置于干燥的仪器 X 中,向分液漏斗中加入一定量的蒸馏水。

仪器X的名称是。打开分液漏斗活塞,将蒸馏水加入仪器X中。反应完全后(无固体剩余),注射器内收集到80.0mL气体,说明样品中含有g Na2O2(计算结果保留到小数点后两位)。
(4)、更换注射器后,再通过分液漏斗向仪器X 中加入足量稀盐酸,溶液中出现气泡,最终注射器内收集气体的质量为 0.11g。由此可知,样品中含有 , 该物质的质量为(计算结果保留到小数点后两位)。(5)、(得出结论)通过以上实验操作得出结论,猜想是正确的(填序号)。
-
-
-
-