湖南省益阳市2019年中考化学试卷
试卷更新日期:2019-07-22 类型:中考真卷
一、单选题
-
1. 下列变化属于化学变化的是()A、红磷的燃烧 B、胆矾的研碎 C、氮气的液化 D、酒精的挥发2. 空气中含量最多的物质是()A、O2 B、N2 C、稀有气体 D、H2O3. 下列物质属于盐的是()A、CH3COOH B、CaCO3 C、Ca(OH)2 D、MnO24. 下列物质直接排放到空气中,不会产生大气污染的是()A、NO2 B、CO2 C、SO2 D、可吸入颗粒物5. 下列四种金属中,能与稀H2SO4反应放出H2的是()A、Cu B、Ag C、Zn D、Hg6. 下列化学反应属于置换反应的是()A、2NaOH+CuSO4═Na2SO4+Cu(OH)2↓ B、CaCO3+CO2+H2O=Ca(HCO3)2 C、2NaNO3 2NaNO2+O2↑ D、CuO+H2 Cu+H2O7. 影响元素化学性质的最主要因素是()A、原子的质子数 B、原子的电子层数 C、原子的最外层电子数 D、组成某种物质的原子个数8. 为响应党的号召,益阳市采取了一系列落实“绿水青山,就是金山银山”这一理念的措施,以保护生态环境。下列措施中,益阳市不会采纳的是()A、拆除水上娱乐设施,恢复湿地生态 B、建立污水处理厂,处理城市生活污水 C、整改或关停排放物不达标的企业 D、大规模围湖造田,以发展经济9. 实验室中,药品的存放必须符合一定的规则。下列存放药品时所选择的仪器及存放方式正确的是()A、
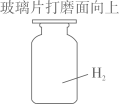 B、
B、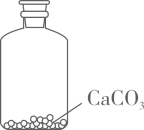 C、
C、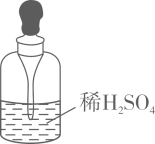 D、
D、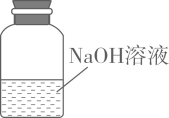 10. 我国古代某些画家、书法家用墨(用炭黑等制成)绘制或书写的字画能够保存至今而不变色的原因是()A、碳在常温下化学性质不活泼 B、炭黑具有很强的吸附能力 C、部分炭黑转变成了更稳定的物质 D、碳单质不溶于水11. 建立宏观和微观之间的联系对学习化学十分重要。下列宏观事实的微观解释错误的是()A、品红在水中扩散﹣﹣分子在不断运动 B、水蒸发由液态变成气态﹣﹣水分子发生改变 C、NO与NO2化学性质不同﹣﹣构成物质的分子不同 D、10mL H2O与10mL C2H5OH混合后体积小于20mL﹣﹣分子间有间隔12. “化学是在分子、原子层次上研究物质性质、组成、结构与变化规律的科学”,实验是研究化学的基本方法。下列有关化学实验与实验目的相符的是()A、闻灼烧织物产生的气味,可以区分某织物是羊毛织品还是合成纤维织品 B、电解H2O生成H2和O2 , 可以说明H2O是由H2和O2组成的 C、观察加入食盐振荡后生成泡沫的多少,可以区分某水样是软水还是硬水 D、用带火星的木条伸入集气瓶中,可以证明氧气是否集满13. 在一个密闭容器中放入X、Y、Z、M四种物质,使之在一定条件下发生化学反应。一段时间后,测得有关数据如下表:
10. 我国古代某些画家、书法家用墨(用炭黑等制成)绘制或书写的字画能够保存至今而不变色的原因是()A、碳在常温下化学性质不活泼 B、炭黑具有很强的吸附能力 C、部分炭黑转变成了更稳定的物质 D、碳单质不溶于水11. 建立宏观和微观之间的联系对学习化学十分重要。下列宏观事实的微观解释错误的是()A、品红在水中扩散﹣﹣分子在不断运动 B、水蒸发由液态变成气态﹣﹣水分子发生改变 C、NO与NO2化学性质不同﹣﹣构成物质的分子不同 D、10mL H2O与10mL C2H5OH混合后体积小于20mL﹣﹣分子间有间隔12. “化学是在分子、原子层次上研究物质性质、组成、结构与变化规律的科学”,实验是研究化学的基本方法。下列有关化学实验与实验目的相符的是()A、闻灼烧织物产生的气味,可以区分某织物是羊毛织品还是合成纤维织品 B、电解H2O生成H2和O2 , 可以说明H2O是由H2和O2组成的 C、观察加入食盐振荡后生成泡沫的多少,可以区分某水样是软水还是硬水 D、用带火星的木条伸入集气瓶中,可以证明氧气是否集满13. 在一个密闭容器中放入X、Y、Z、M四种物质,使之在一定条件下发生化学反应。一段时间后,测得有关数据如下表:物质
X
Y
Z
M
反应前的质量/g
20
5
3
28
反应后的质量/g
待测值
30
3
8
关于此反应的认识错误的是()
A、物质Z可能是该反应的催化剂 B、该反应一定是化合反应 C、参加反应的Y、M的质量比为5:4 D、待测值为1314. 下列说法正确的是()A、洗洁精能使餐具上的油污乳化 B、锡铅合金的熔点比锡和铅的熔点都高 C、溶液中的溶剂只能是水 D、NH4NO3溶于水放热使水的温度升高15. X、Y、Z三种物质的溶解度曲线如图所示。下列说法正确的是()
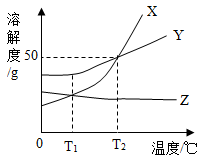 A、将T2℃时三种物质的饱和溶液降温到T1℃后,溶质质量分数大小关系为:Y>X>Z B、Y的溶解度为50g C、降低温度可使Z的不饱和溶液变成饱和溶液 D、T2℃时,50gH2O与50gX混合,可得到100gX的饱和溶液16. 粗盐中难溶性杂质的去除过程中,涉及到称量、溶解、过滤、蒸发等过程。下列说法错误的是()A、称量时粗盐放在天平左盘的称量纸上 B、粗盐溶解时,要用玻璃棒不断搅拌 C、蒸发时,在恰好蒸干时停止加热 D、过滤时漏斗下端尖嘴处紧靠烧杯内壁17. 欲除去下列物质中的少量杂质,所用试剂及方法错误的是()
A、将T2℃时三种物质的饱和溶液降温到T1℃后,溶质质量分数大小关系为:Y>X>Z B、Y的溶解度为50g C、降低温度可使Z的不饱和溶液变成饱和溶液 D、T2℃时,50gH2O与50gX混合,可得到100gX的饱和溶液16. 粗盐中难溶性杂质的去除过程中,涉及到称量、溶解、过滤、蒸发等过程。下列说法错误的是()A、称量时粗盐放在天平左盘的称量纸上 B、粗盐溶解时,要用玻璃棒不断搅拌 C、蒸发时,在恰好蒸干时停止加热 D、过滤时漏斗下端尖嘴处紧靠烧杯内壁17. 欲除去下列物质中的少量杂质,所用试剂及方法错误的是()物质
杂质(少量)
除杂试剂及方法
A
O2
CO2
依次通过NaOH溶液和浓硫酸
B
NaCl溶液
Na2CO3
先加过量稀盐酸,再滴加NaOH溶液调节pH=7
C
FcCl2溶液
CuCl2
加入过量铁粉,过滤
D
铜粉
铁粉
加入过量AgNO3溶液,过滤
A、A B、B C、C D、D18. 下列图示实验操作中,正确的是()A、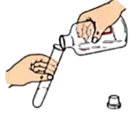 B、
B、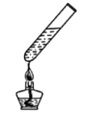 C、
C、 D、
D、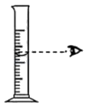
二、实验题
-
19. 实验室提供H2O2溶液、MnO2、KClO3和KMnO4四种药品及下列仪器。
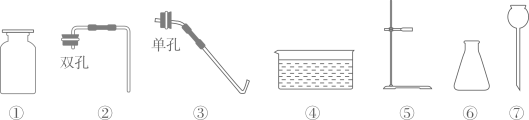 (1)、仪器⑤的名称为。(2)、利用上述药品及仪器可以制取O2 , 反应的化学方程式是 , 组装发生和收集O2的装置,需要选择的最佳仪器是(选择序号填空)。
(1)、仪器⑤的名称为。(2)、利用上述药品及仪器可以制取O2 , 反应的化学方程式是 , 组装发生和收集O2的装置,需要选择的最佳仪器是(选择序号填空)。三、填空题
-
20. 请用化学用语填空:(1)、铝合金中铝的元素符号是 , 生石灰的化学式是。(2)、酸有一些相似的化学性质,是因为不同的酸溶液中都含有。(3)、某种硫单质的一个分子中含有6个硫原子,这种硫单质的化学式是。21. 从NH3、CO、CH4和NH4H2PO4四种物质中,选择合适的物质填空(填化学式):(1)、属于复合肥料的是 , 属于有机物的是。(2)、其水溶液能使酚酞溶液变红的是 , 可用于冶金工业炼铁的是。22. 钙元素是构成人体的重要组成部分,钠、锌等元素对人体健康也有着重要作用。(1)、少儿患佝偻病和发育不良,老年人得骨质疏松症是因为体内缺(填元素符号)。(2)、上述三种元素中,属于微量元素的是(填元素符号);对维持人体内的水分和维持体液pH的恒定起重要作用的是(填离子符号)。23. 材料一:侯德榜是我国著名的化学家,发明了侯氏制碱法,为纯碱和氮肥工业技术的发展作出了杰出的贡献。下面是实验室模拟侯氏制碱法原理的生产过程:

①20℃时,将CO2通入含NH3的饱和NaCl溶液中,生成NaHCO3晶体和NH4Cl溶液。
②将①中的产物NaHCO3晶体充分加热分解,得到Na2CO3、H2O和CO2。
材料二:20℃时几种物质在水中的溶解度/g
NaCl
NH4Cl
NaHCO3
36.0
37.2
9.6
请回答下列问题:
(1)、在第①步反应中,有 NaHCO3晶体析出,而没有NH4Cl和NaCl晶体析出的原因是。(2)、该生产过程中部分生成物可作为原料循环使用的是 , 同时得到的副产品NH4Cl是一种氮肥。四、简答题
-
24. 某化学反应的微观示意图如图所示,其中相同的球代表同种原子。
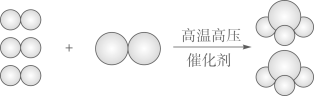 (1)、该化学反应中,发生变化的是(选填“分子”或“原子”),参加反应的两种分子的个数比为。(2)、该反应的生成物是_____(选择序号填空)。A、化合物 B、单质 C、混合物(3)、该反应的微观示意图说明,化学反应遵守质量守恒定律的原因是。25. 合理运用燃烧与灭火的原理,对保障生命财产安全至关重要。(1)、消防队员用高压水枪灭火的原理是 , 做实验时不慎碰倒酒精灯,酒精在桌面燃烧起来,可用的灭火方法是。(2)、着火时,可用湿毛巾捂住口鼻,低姿势跑离着火区域逃生,理由是_____(选择序号填空)。A、湿毛巾可防止吸入灼热的气体灼伤呼吸道 B、湿毛巾会吸收CO C、地面附近的有毒气体相对较少
(1)、该化学反应中,发生变化的是(选填“分子”或“原子”),参加反应的两种分子的个数比为。(2)、该反应的生成物是_____(选择序号填空)。A、化合物 B、单质 C、混合物(3)、该反应的微观示意图说明,化学反应遵守质量守恒定律的原因是。25. 合理运用燃烧与灭火的原理,对保障生命财产安全至关重要。(1)、消防队员用高压水枪灭火的原理是 , 做实验时不慎碰倒酒精灯,酒精在桌面燃烧起来,可用的灭火方法是。(2)、着火时,可用湿毛巾捂住口鼻,低姿势跑离着火区域逃生,理由是_____(选择序号填空)。A、湿毛巾可防止吸入灼热的气体灼伤呼吸道 B、湿毛巾会吸收CO C、地面附近的有毒气体相对较少五、流程题
-
26. 制作电脑芯片的材料为高纯硅,工业上制造高纯硅的基本流程如图1所示(某些反应过程中的部分物质没有在图中标出):
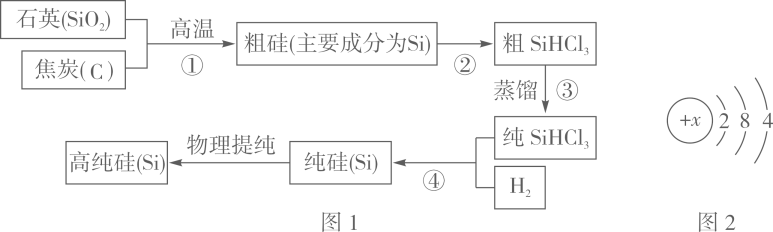 (1)、SiHCl3中Cl元素的化合价为﹣1价,则Si元素的化合价为。(2)、硅原子的结构示意图如图2所示,硅原子的核电荷数为。(3)、第①步至第④步的变化中,属于物理变化的是第步。(4)、第④步反应,除生成纯硅以外,还有HCl生成。写出第④步反应的化学方程式。
(1)、SiHCl3中Cl元素的化合价为﹣1价,则Si元素的化合价为。(2)、硅原子的结构示意图如图2所示,硅原子的核电荷数为。(3)、第①步至第④步的变化中,属于物理变化的是第步。(4)、第④步反应,除生成纯硅以外,还有HCl生成。写出第④步反应的化学方程式。六、科普阅读题
-
27. 材料一:人通过食物获得的蛋白质,在胃肠道里与水反应,生成氨基酸。氨基酸的种类很多,如:乙氨酸(C2H5O2N)、丙氨酸(X)、丁氨酸(C4H9O2N)、戊氨酸(C5H11O2N)等。
材料二:乙氨酸的化学式也可写成NH2CH2COOH.乙氨酸的某些性质与醋酸类似,如都能与NaOH溶液反应。已知醋酸与NaOH溶液反应的化学方程式为CH3COOH+NaOH=CH3COONa+H2O。
(1)、根据材料一,推测丙氨酸的化学式X为。(2)、根据材料二,写出乙氨酸与NaOH溶液反应的化学方程式。七、科学探究题
-
28. 向一定量的NaOH溶液中慢慢通入CO2气体,看不到明显现象。某实验小组的同学对所得溶液成分进行了如下探究。请你参与他们的探究活动,并完成以下问题:
(提出问题)所得溶液中溶质的成分是什么?
(査阅资料)资料一:将CO2气体慢慢地通入一定量的NaOH溶液中,可能发生以下两个化学反应:
先发生反应:2NaOH+CO2═Na2CO3+H2O
当NaOH反应完全后,继续发生反应:Na2CO3+CO2+H2O═2NaHCO3
資料二;Ca(HCO3)2易溶于水;CaCl2溶液与NaCl溶液均呈中性; NaHCO3溶液呈碱性,可使酚酞溶液变红色。
(猜想与假设)小组同学通过讨论,提出了以下四种猜想
猜想一:溶质为NaOH和Na2CO3
猜想二:溶质全为Na2CO3
⑴你认为猜想三:溶质为
猜想四:溶质全为 NaHCO3
(实验探究)小组同学设计并完成了如下实验:
实验步骤
实验过程
实验现象
实验结论
①
取适量反应后的溶液置于试管
中,加入过量CaCl2溶液
有白色沉淀生成
⑵猜想不成立
②
取适量步骤①反应后的上层清
液,滴加几滴酚酞溶液
⑶现象为
猜想二不成立
③
取适量步骤①反应后的上层清
液,加入适量稀HCl
有气泡产生
⑷猜想成立
(实验总结)针对上述实验,实验小组的同学总结并写出了上述探究过程中的各步反应方程式。
⑸你认为步骤①发生反应的化学方程式是。
八、计算题
-
29. 今年4月,多家媒体报道,中科院专家的研究成果中完整阐明了抗癌活性物质汉黄芩素(C16H12O5)的合成机制,成功解析了一种使用2000多年的药用植物中的珍贵化学物质合成途径。请计算:(1)、汉黄芩素的相对分子质量是。(2)、汉黄芩素中各元素质量的最简整数比m(C):m(H):m(O)=。30. 某市售某浓盐酸试剂瓶标签上的有关数据如图1所示。小张同学取5mL该浓盐酸加入锥形瓶中,加水稀释后,再逐滴滴加溶质质量分数为5%的NaOH溶液,反应过程中溶液的酸碱度变化如图2所示。
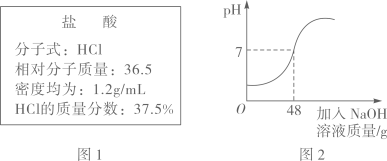 (1)、小张同学所取的5mL浓盐酸的质量为克。(2)、通过计算,判断该浓盐酸中HCl的质量分数是否与试剂瓶标签上的数据相符(需要计算过程,计算结果精确到0.1%)
(1)、小张同学所取的5mL浓盐酸的质量为克。(2)、通过计算,判断该浓盐酸中HCl的质量分数是否与试剂瓶标签上的数据相符(需要计算过程,计算结果精确到0.1%)
-
-
-
-