吉林省2019年中考化学试卷
试卷更新日期:2019-07-02 类型:中考真卷
一、单项选择握(每小题1分,共10分)
-
1. 2019年是“国际化学元素周期表年”,编制元素周期表的俄国科学家是( )A、侯德榜 B、屠呦呦 C、门捷列夫 D、拉瓦锡2. 通常情况下,空气中体积分数约占21%的气体是( )A、氮气 B、氧气 C、二氧化碳 D、稀有气体3. 下列有关分子、原子说法错误的是( )A、很小 B、不断运动 C、有间隔 D、不可分4. 下列实验操作正确的是( )A、连接仪器
 B、塞紧胶塞
B、塞紧胶塞  C、倾倒液体
C、倾倒液体 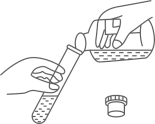 D、过滤
D、过滤 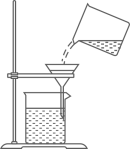 5. 下列说法错误的是( )A、NaHCO3俗称小苏打 B、CaCO3可用作补钙剂 C、Na2CO3俗称火碱 D、K2CO3属于钾肥6. 下列实验现象描述正确的是( )A、铁丝燃烧时发出耀眼白光 B、红磷燃烧时产生大量白雾 C、氢气燃烧时发出黄色火焰 D、硫在氧气中燃烧发出蓝紫色火焰7. 下列化学方程式书写正确的是( )A、2H2O 2H2+O2 B、2KMnO4=K2MnO4+MnO2+O2 C、BaCl2+Na2CO3=2Nal+BaCO3↓ D、Zn+H2SO4=ZnSO4+H28. 下列说法正确的是( )A、点燃可燃性气体前要验纯 B、稀释浓硫酸时将水倒入浓硫酸中 C、蒸发食盐水时出现固体就停止加热 D、配制溶液时用量筒溶解固体物质9. 向盛有一定成固体的烧杯中加入某溶液,固体质量变化与下图相符的是( )
5. 下列说法错误的是( )A、NaHCO3俗称小苏打 B、CaCO3可用作补钙剂 C、Na2CO3俗称火碱 D、K2CO3属于钾肥6. 下列实验现象描述正确的是( )A、铁丝燃烧时发出耀眼白光 B、红磷燃烧时产生大量白雾 C、氢气燃烧时发出黄色火焰 D、硫在氧气中燃烧发出蓝紫色火焰7. 下列化学方程式书写正确的是( )A、2H2O 2H2+O2 B、2KMnO4=K2MnO4+MnO2+O2 C、BaCl2+Na2CO3=2Nal+BaCO3↓ D、Zn+H2SO4=ZnSO4+H28. 下列说法正确的是( )A、点燃可燃性气体前要验纯 B、稀释浓硫酸时将水倒入浓硫酸中 C、蒸发食盐水时出现固体就停止加热 D、配制溶液时用量筒溶解固体物质9. 向盛有一定成固体的烧杯中加入某溶液,固体质量变化与下图相符的是( ) A、MnO2中加入H2O2溶液 B、Cu-Zn合金中加入稀HCl C、CuO中加入稀H2SO4 D、BaCO3中加入稀HNO310. 下列实验方案设计不能达到实验目的的是( )A、用Ba(OH)2溶液除去NaNO3溶液中的CuSO4 B、用Na2CO3溶液鉴别NaOH溶液和CaCl2溶液 C、用稀H2SO4 , Fe2O3 , 和NaOH溶液制备Fe(OH)3 D、用酚酞溶液检验CaO中是否含有Ca(OH)2
A、MnO2中加入H2O2溶液 B、Cu-Zn合金中加入稀HCl C、CuO中加入稀H2SO4 D、BaCO3中加入稀HNO310. 下列实验方案设计不能达到实验目的的是( )A、用Ba(OH)2溶液除去NaNO3溶液中的CuSO4 B、用Na2CO3溶液鉴别NaOH溶液和CaCl2溶液 C、用稀H2SO4 , Fe2O3 , 和NaOH溶液制备Fe(OH)3 D、用酚酞溶液检验CaO中是否含有Ca(OH)2二、填空题(每空1分,共10分)
-
11. 如图所示,用化学符号填空。
 (1)、(2)、(3)、12. 化学与我们的生活联系密切。(1)、生活中通过的方法可以降低水的硬度。(2)、大米中含量最多的营养素是。(3)、天然气有性,常用作燃料。(4)、炒菜时油锅着火,通常用的方法灭火。13. A,B两种固体物质的溶解度曲线如右图所示。
(1)、(2)、(3)、12. 化学与我们的生活联系密切。(1)、生活中通过的方法可以降低水的硬度。(2)、大米中含量最多的营养素是。(3)、天然气有性,常用作燃料。(4)、炒菜时油锅着火,通常用的方法灭火。13. A,B两种固体物质的溶解度曲线如右图所示。 (1)、t1℃时,A的溶解度是g。(2)、将t1℃时B的饱和溶液升高温度至t2℃,所得溶液为(填“饱和”或“不饱和”)溶液。(3)、将t2℃时A的饱和溶液冷却到t1℃,溶液的浓度会(填“变大”或“不变”或“变小”)。
(1)、t1℃时,A的溶解度是g。(2)、将t1℃时B的饱和溶液升高温度至t2℃,所得溶液为(填“饱和”或“不饱和”)溶液。(3)、将t2℃时A的饱和溶液冷却到t1℃,溶液的浓度会(填“变大”或“不变”或“变小”)。三、简答题(每空1分,化学方程式2分,共12分)
-
14. 回答下列问题。(1)、2Na+2H2O=2NaOH+R↑,其中R的化学式为。(2)、水与氧化钙反应的生成物属于(填“酸”或“碱”或“盐”)。15. 在宏观、微观与符号之间建立联系,是化学学科的特点。

按上图所示,回答下列问题。
(1)、指1中两种微粒属于不同种元素是因为不同。(2)、图2中反应的化学方程式为 , 其基本反应类型是。16.(1)、某同学在实验室中看到铁钉表面附着红色物质,分不出是铁锈还是铜,为证明红色物质的成分,将其“刮”下来,放入溶液中进行验证。
(2)、若固体溶解,则该物质为铁锈;铁锈是铁与反应生成的。(3)、若固体不溶,则该物质为铜;铜可能是铁与溶液反应生成的。17. 某同学在做中和反应实验时,用pH传感器测得溶液的pH变化如图所示,回答下列问题。 (1)、向A点溶液中滴加紫色石蕊溶液的现象是。(2)、曲线上点表示酸和碱恰好完全反应。(3)、C点溶液中含有种溶质。
(1)、向A点溶液中滴加紫色石蕊溶液的现象是。(2)、曲线上点表示酸和碱恰好完全反应。(3)、C点溶液中含有种溶质。四、实验与探究题(每空1分,化学方程式2分,共12分)
-
18. 根据下图回答问题。
 (1)、图中仪器a的名称是。(2)、实验室用加热方法制取氧气的发生和收集装置为(填字母序号)。(3)、某同学用自制的D装置在实验室制取二氧化碳气体,无纺布包内装的药品为 , 其反应的化学方程式为。19. 教育部从2018年开始,要求在学校普及垃圾分类回收处理的相关知识。某化学活动小组结合新学的知识对此进行一系列实践活动。(1)、I.活动探究
(1)、图中仪器a的名称是。(2)、实验室用加热方法制取氧气的发生和收集装置为(填字母序号)。(3)、某同学用自制的D装置在实验室制取二氧化碳气体,无纺布包内装的药品为 , 其反应的化学方程式为。19. 教育部从2018年开始,要求在学校普及垃圾分类回收处理的相关知识。某化学活动小组结合新学的知识对此进行一系列实践活动。(1)、I.活动探究学会识图分拣垃圾:下列垃圾应投入带有右图图标的垃圾箱内的是(填字母序号)。

A.塑料版 B.果皮 C.碎瓷片
(2)、学会检验有害气体:含氯塑料焚烧时会产生氯化氢等气体,若要检验焚烧后的气体中有氯化氢,可将其通入溶液中,有白色沉淀生成即可。(3)、Ⅱ.实验探究【提出问题】如何回收处理废旧电池中的镉?
【查阅资科】
①废旧电池中含有镉、汞等元素,这些元素会危害人类健康。
②镉(Cd)从溶液中析出时呈海绵状固体,在化合物中通常表现为+2价。
③碳酸镉(CdCO3)、氢氯化镉[Cd(OH)2]都是白色固体,难溶于水。
【设计实验】先将废旧电池进行处理以制得硫酸镉(CdSO4)溶液,用于以下实验。
实验设计
实验步骤
实验现象
实验结论
与金属反应
取少许溶液于试管中,加入足量的Zn粉,充分反应。
Zn可以置换出Cd。
与碱反应
取少许溶液于试管中,加入足量的NaOH溶液,充分反应。
产生白色沉淀
用化学反应方程式表示为
取少许溶液于试管中,加入足量的溶液,充分反应。
产生白色沉淀
可用该试剂除去CdSO4.。
(4)、【回收处理】实验结束后,将反应后的混合物通过过滤、洗涤、加热,进而再制得镉。
【交流反思】
请同学们基于化学视角说明垃圾分类回收处理的重要意义(答一点即可)。
五、计算题(6分)
-
20. 现有5.6gKOH固体与100g稀HCl恰好完全反应,求该稀HCl中溶质的质量分数。