山东省德州市2019年中考化学试卷
试卷更新日期:2019-06-27 类型:中考真卷
一、单选题
-
1. 2019年世界地球日的主题是“珍爱美丽地球 守护自然资源”。下列做法不符合这一主题的是( )A、合理施用化肥和农药,减少负面作用 B、工业废水达标后排放,防治水体污染 C、露天焚烧废旧塑料,减少白色污染 D、垃圾分类回收,节约资源、减少污染2. 下面是实验室常见的玻璃仪器,其中能够在酒精灯上直接加热的是( )A、
 B、
B、 C、
C、 D、
D、 3. 空气是一种宝贵的自然资源。下列对空气的相关叙述正确的是( )A、空气是由空气分子构成的 B、空气中的氧气可以作燃料 C、稀有气体化学性质很不活泼 D、化石燃料的使用不会污染空气4. 中国诗词、成语和谚语中有些蕴含着化学知识。下列说法正确的是( )A、“遥知不是雪,为有暗香来”说明分子在不断地运动 B、“只要功夫深,铁杵磨成针”描述的是化学变化 C、“真金不怕火炼"说明金具有熔点高的物理性质 D、“釜底抽薪”体现的灭火原理是隔绝氧气(或空气)5. 下列化学用语书写正确的是( )A、2个氮原子-N2 B、钙离子-Ca+2 C、氯化铁-FeCl2 D、氦气-He6. 碳酸氢铵(NH4HCO3)可用作食品添加剂,有关它的说法正确的是( )A、碳酸氢铵是有机物 B、氮、氢元素质量比为1: 5 C、碳酸氢铵由10个原子构成 D、碳酸氢铵由四种元素组成7. 下面是某同学在制取二氧化碳时选用的实验装置或操作方法,正确的是( )A、
3. 空气是一种宝贵的自然资源。下列对空气的相关叙述正确的是( )A、空气是由空气分子构成的 B、空气中的氧气可以作燃料 C、稀有气体化学性质很不活泼 D、化石燃料的使用不会污染空气4. 中国诗词、成语和谚语中有些蕴含着化学知识。下列说法正确的是( )A、“遥知不是雪,为有暗香来”说明分子在不断地运动 B、“只要功夫深,铁杵磨成针”描述的是化学变化 C、“真金不怕火炼"说明金具有熔点高的物理性质 D、“釜底抽薪”体现的灭火原理是隔绝氧气(或空气)5. 下列化学用语书写正确的是( )A、2个氮原子-N2 B、钙离子-Ca+2 C、氯化铁-FeCl2 D、氦气-He6. 碳酸氢铵(NH4HCO3)可用作食品添加剂,有关它的说法正确的是( )A、碳酸氢铵是有机物 B、氮、氢元素质量比为1: 5 C、碳酸氢铵由10个原子构成 D、碳酸氢铵由四种元素组成7. 下面是某同学在制取二氧化碳时选用的实验装置或操作方法,正确的是( )A、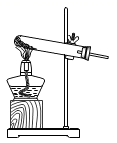 发生装置
B、
发生装置
B、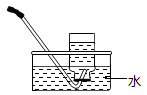 收集
C、
收集
C、 干燥
D、
干燥
D、 验满
8. 石墨烯是一种非常优良的纳米材料,由碳元素组成,化学性质和石墨相似,还具有超强导电、导热的性能。关于石墨烯的认识错误的是( )A、可作散热材料 B、是一种新型化合物 C、常温下化学性质稳定 D、可作新型电池的电极9. 化学反应不仅有新物质生成,而且还伴随能量变化。以下能量变化不是由化学变化引起的是( )A、鞭炮爆炸发声 B、蜡烛燃烧发光 C、煤燃烧火力发电 D、电水壶通电放热10. 根据如图所示的实验现象分析,下列说法错误的是( )
验满
8. 石墨烯是一种非常优良的纳米材料,由碳元素组成,化学性质和石墨相似,还具有超强导电、导热的性能。关于石墨烯的认识错误的是( )A、可作散热材料 B、是一种新型化合物 C、常温下化学性质稳定 D、可作新型电池的电极9. 化学反应不仅有新物质生成,而且还伴随能量变化。以下能量变化不是由化学变化引起的是( )A、鞭炮爆炸发声 B、蜡烛燃烧发光 C、煤燃烧火力发电 D、电水壶通电放热10. 根据如图所示的实验现象分析,下列说法错误的是( )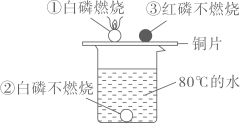 A、①②对比说明物质燃烧需要与空气接触 B、①中使温度达到白磷着火点是利用了铜的导热性 C、烧杯中的热水只起提高温度的作用 D、①③对比说明红磷着火点高于白磷11. 下面是人体内一些液体的正常pH范围,其中显酸性的是( )A、血浆 7.35-7.45 B、胃液 0.9-1.5 C、胆汁 7.1-7.3 D、胰液 7.5-8.012. 分类是一种重要的研究方法。以下对常见物质的分类正确的是( )A、氧化物:水、生石灰、五氧化二磷 B、碱:火碱、熟石灰、纯碱 C、混合物:煤、食盐水、冰水混合物 D、合成材料:羊毛、塑料、合成橡胶13. 两瓶标签损毁的溶液分别是稀盐酸、稀硫酸,下列试剂中能够用来区分两种溶液的是. ( )A、锌粒 B、氯化钡溶液 C、紫色石蕊溶液 D、氢氧化钠溶液14. 推理是一种重要的思维方法。下列推理正确的是( )A、分子是构成物质的微粒,所以物质都是由分子构成 B、氧气由氧元素组成,所以制取氧气的反应物一定含有氧元素 C、溶液是均一、稳定的混合物,所以均一、稳定的物质就是溶液 D、化合物由多种元素组成,所以由多种元素组成的物质就是化合物15. 下列实验方案不能达到实验目的的是( )
A、①②对比说明物质燃烧需要与空气接触 B、①中使温度达到白磷着火点是利用了铜的导热性 C、烧杯中的热水只起提高温度的作用 D、①③对比说明红磷着火点高于白磷11. 下面是人体内一些液体的正常pH范围,其中显酸性的是( )A、血浆 7.35-7.45 B、胃液 0.9-1.5 C、胆汁 7.1-7.3 D、胰液 7.5-8.012. 分类是一种重要的研究方法。以下对常见物质的分类正确的是( )A、氧化物:水、生石灰、五氧化二磷 B、碱:火碱、熟石灰、纯碱 C、混合物:煤、食盐水、冰水混合物 D、合成材料:羊毛、塑料、合成橡胶13. 两瓶标签损毁的溶液分别是稀盐酸、稀硫酸,下列试剂中能够用来区分两种溶液的是. ( )A、锌粒 B、氯化钡溶液 C、紫色石蕊溶液 D、氢氧化钠溶液14. 推理是一种重要的思维方法。下列推理正确的是( )A、分子是构成物质的微粒,所以物质都是由分子构成 B、氧气由氧元素组成,所以制取氧气的反应物一定含有氧元素 C、溶液是均一、稳定的混合物,所以均一、稳定的物质就是溶液 D、化合物由多种元素组成,所以由多种元素组成的物质就是化合物15. 下列实验方案不能达到实验目的的是( )实验目的
实验方案
A
鉴别木炭粉和铁粉
分别加入到足量稀硫酸中
B
鉴别棉线和合成纤维
点燃,闻气味、看灰烬
C
除去氯化亚铁溶液中少量的氯化铜
加人足量锌粉
D
除去氧气中的二氧化碳
将气体通入足量的氢氧化钠溶液
A、A B、B C、C D、D16. 下图是X、Y两种固体物质的溶解度曲线。下列叙述正确的是( )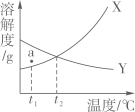 A、温度低于t2℃时,物质Y的溶解度小于X B、X、Y的溶解度都随温度升高而增大 C、a点表示t1℃时X、Y的溶液都、不饱和 D、Y的饱和溶液降低温度后,溶质质量分数不变
A、温度低于t2℃时,物质Y的溶解度小于X B、X、Y的溶解度都随温度升高而增大 C、a点表示t1℃时X、Y的溶液都、不饱和 D、Y的饱和溶液降低温度后,溶质质量分数不变二、填空题
-
17. 化学与生活息息相关。请回答下列问题:(1)、大枣含有蛋白质、糖类及维生素等营养素,其中能起到调节人体新陈代谢,预防疾病作用的是。(2)、净化水时放入活性炭除去色素、异味,这是利用了活性炭的性。(3)、家庭中常用洁厕灵(有效成分为盐酸)去除尿垢(其中含有碳酸钙)。写出盐酸与碳酸钙反应的化学方程式。18. “化学是在分子、原子层次上研究物质的性质、组成,结构与变化规律的科学”。请根据你对“化学”这门科学的认识解答以下问题:(1)、通过电解水的实验,可以推断水是由(填元素符号)元素组成。(2)、金刚石和石墨组成元素相同,而它们的物理性质却有很大差异,其微观解释是。(3)、以下物质用途主要是由其物理性质决定的是(填序号)。
①氢气填充探空气球 ②氢氧化钠干燥气体 ③天然气作燃料 ④用铜制作导线
(4)、以下符合化学方程式书写原则的是(填序号)。①C+O2=CO2 ②Al+HCl=AICl3+H2↑ ③Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
19. 含氮元素的物质与人类生产,生活关系密切。请你回答有关问题:(1)、N2、NH3、HNO3等都是常见的含氮物质,其中氮元素化合价最低的物质是。(2)、氮气具有广泛的用途.如超导材料在液氮的低温环境下能显示超导性能。从微观角度分析:制取液氮时,在氮气液化过程中发生变化的是(填序号).①分子的大小 ②分子的质量 ③分子间的间隔 ④分子的数目
(3)、将空气中的氮气转化为含氮化合物的过程称为固氮(“氮"指氮元素)。某些生物(如大豆根系中的根瘤菌)就具有固氮作用。经田间试验测定,一亩大豆可固氮8kg,相当于施用kg(保留整数)尿素[化学式为CO(NH2)2]。(4)、下面是在汽车尾气治理过程中有关化学反应的微观示意图。图中所示反应的化学方程式为。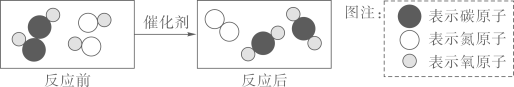 20. 依据对初中所学四种反应类型(化合反应、分解反应、置换反应、复分解反应)概念的理解,结合下列化学方程式,比较反应前后元素化合价的变化情况:(1)、一定有变化的是(填反应类型.下同)
20. 依据对初中所学四种反应类型(化合反应、分解反应、置换反应、复分解反应)概念的理解,结合下列化学方程式,比较反应前后元素化合价的变化情况:(1)、一定有变化的是(填反应类型.下同)
(2)、不一定有变化的是;(3)、一定没有变化的是。①CO2+H2O=H2CO3 ②Cu+2AgNO3=Cu(NO3)2+2Ag
③ ④
⑤NaOH+HCl=NaCl+H2O ⑥
21. 将NaOH、NaCl、NH4NO3固体各10g分别放入盛有100mL水的烧杯中充分溶解。在不同时间测量溶液的温度,绘制成如下图像:
分析图像,回答问题:
(1)、在NaOH、NaCl、NH4NO3三种物质中,溶解时出现吸热现象的是(写名称);(2)、对NaOH而言,a点右侧曲线表示:在一定时间段内,溶液温度随时间推移面(填“升高”或“降低”),其原因是。三、实验题
-
22. 化学是一门以实验为基础的科学。请结合图示回答以下问题:
 (1)、图1是某同学稀释浓硫酸的操作,请指出该操作可能出现的现象。(2)、在实验室中选用图2装置制取氧气.请用化学方程式表示其制取原理:。(3)、图3是一氧化碳还原氧化铁的实验装置图。实验过程中玻璃管内出现的现象是;试管内发生反应的化学方程式为。23.(1)、我们通过学习知道:钠原子结构示意图如下,钠原子在化学反应中易电子,成为(填名称)。
(1)、图1是某同学稀释浓硫酸的操作,请指出该操作可能出现的现象。(2)、在实验室中选用图2装置制取氧气.请用化学方程式表示其制取原理:。(3)、图3是一氧化碳还原氧化铁的实验装置图。实验过程中玻璃管内出现的现象是;试管内发生反应的化学方程式为。23.(1)、我们通过学习知道:钠原子结构示意图如下,钠原子在化学反应中易电子,成为(填名称)。 (2)、(I)“在金属活动顺序里,位于前面的金属能把位于后面的金属从其盐溶液里置换出来”,金属钠排在的前面。有的同学据此推测:钠能从蓝色硫酸铜溶液中把铜置换出来。教师按照下列图示顺序进行演示实验,并记录实验现象:
(2)、(I)“在金属活动顺序里,位于前面的金属能把位于后面的金属从其盐溶液里置换出来”,金属钠排在的前面。有的同学据此推测:钠能从蓝色硫酸铜溶液中把铜置换出来。教师按照下列图示顺序进行演示实验,并记录实验现象:
①由以上实验现象得出结论:因为反应中没有色的物质生成,所以金属钠(填:"能"或“不能")把铜从硫酸铜溶液中置换出来
②对实验涉及的物质进行分析:硫酸铜溶液中溶剂为水.溶质为(填化学式),钠与硫酸铜溶液反应后培养中所含元素有:Na、Cu、H、O、(填元素符号)五种元素。查阅资料得知:“蓝色絮状难溶物”是一种学过的碱,该物质的名称是。
(3)、有的同学又产生新的疑问:钠能否与水发生反应?生成物是什么?教师为解答学生的疑惑,又设计并进行如下实验.同时记录有关现象:
请结合上图所示信息,回答下列问题:
①用手触摸图3中烧杯外壁,感觉烫手,说明钠与水发生的是(填:"吸热"或"放热")反应。
②从“图3”中可以断定:液体中出现红色说明反应后液体显性,结合液体中所含元素,继而推断有(填化学式)生成。另外,钠与水反应还生成一种可燃性气体单质。请写出钠与水反应的化学方程式:。
四、计算题