安徽省宣城市2016-2017学年高二下学期化学期末考试试卷
试卷更新日期:2019-06-19 类型:期末考试
一、单选题
-
1. 中国汉字听写大会后,某校掀起了汉字书写考查热,下列有关化学名称正确的是()A、坩锅 B、蒸馏烧瓶 C、萃取 D、苯乙稀2. 化学是“五颜六色”的,下列颜色变化不包含化学变化的是()A、刚切开的钠为银白色,迅速变暗 B、浓硫酸滴在胆矾晶体表面,蓝色变白 C、小龙虾出锅“着红袍” D、CCl4加入碘水中,振荡后碘水褪色3. 用NA 表示阿伏加德罗常数的值,下列说法正确的是()A、44.8LH2完全燃烧消耗氧气分子数为NA B、28g乙烯(C2H4)和丙烯(C3H6)的混合物含碳原子数为2.5NA C、2mol·L-1NaOH溶液中的钠离子数为2NA D、1molD2O和H218O混合物中子数为10NA4. 下列化学用语使用正确的是( )A、14C原子结构示意图:
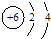 B、硝基苯的结构简式:
B、硝基苯的结构简式: 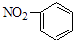 C、CO2的电子式:
C、CO2的电子式:  D、CH4分子的球棍模型:
D、CH4分子的球棍模型:  5. 25℃,对于1L1mol·L-1CuSO4溶液和1L1mol·L-1FeCl3溶液,下列说法正确的是()A、前者溶液为黄色,后者为蓝色 B、加入1L1mol·L-1Na2CO3溶液后都能大量共存 C、加入28g还原铁粉,都发生氧化还原反应 D、都可以催化H2O2的分解,且催化效果相同6. 下列关于新型净水剂高铁酸钾(K2FeO4)有关说法错误的是()A、Fe位于元素周期表第四周期,VⅢA族 B、K在同周期中,原子半径最大,金属性最强 C、高铁酸钾具有强氧化性 D、高铁酸钾中Fe的化合价为+67. 下列关于基本营养物质说法错误的是()A、家庭做菜用的菜籽油、花生油和猪油都属于酯类 B、蔗糖水解得到葡糖糖和果糖,麦芽糖水解只得到葡萄糖,蔗糖和麦芽糖是同分异构体 C、疫苗需冷冻保藏,是防止蛋白质变性 D、糖类和蛋白质都是人体必需的营养物质,都属于高分子化合物8. 如下图烧杯内盛有0.5mol·L-1的稀硫酸200mL,工作一段时间后,测得电路中通过0.02mol电子,若忽略溶液体积的变化,下列叙述正确的是()
5. 25℃,对于1L1mol·L-1CuSO4溶液和1L1mol·L-1FeCl3溶液,下列说法正确的是()A、前者溶液为黄色,后者为蓝色 B、加入1L1mol·L-1Na2CO3溶液后都能大量共存 C、加入28g还原铁粉,都发生氧化还原反应 D、都可以催化H2O2的分解,且催化效果相同6. 下列关于新型净水剂高铁酸钾(K2FeO4)有关说法错误的是()A、Fe位于元素周期表第四周期,VⅢA族 B、K在同周期中,原子半径最大,金属性最强 C、高铁酸钾具有强氧化性 D、高铁酸钾中Fe的化合价为+67. 下列关于基本营养物质说法错误的是()A、家庭做菜用的菜籽油、花生油和猪油都属于酯类 B、蔗糖水解得到葡糖糖和果糖,麦芽糖水解只得到葡萄糖,蔗糖和麦芽糖是同分异构体 C、疫苗需冷冻保藏,是防止蛋白质变性 D、糖类和蛋白质都是人体必需的营养物质,都属于高分子化合物8. 如下图烧杯内盛有0.5mol·L-1的稀硫酸200mL,工作一段时间后,测得电路中通过0.02mol电子,若忽略溶液体积的变化,下列叙述正确的是() A、Zn表面产生224mLH2(标况) B、因气体逸出,溶液的质量减轻 C、正极电极反应式:2H+ +2e-=H2↑ D、0.02mol电子经溶液由Cu极转移到Zn极9. 对于工业合成氨反应 N2(g)+3H2(g)
A、Zn表面产生224mLH2(标况) B、因气体逸出,溶液的质量减轻 C、正极电极反应式:2H+ +2e-=H2↑ D、0.02mol电子经溶液由Cu极转移到Zn极9. 对于工业合成氨反应 N2(g)+3H2(g) 2NH3(g),以下分析错误的是() A、在5L固定容积的密闭容器内,前2分钟消耗2molN2 , 则v(N2)=0.2mol·L-1·min-1 B、改变条件可使H2的转化率达100% C、每消耗3molH2 , 必然生成2molNH3 D、合成氨是人类科学史上的一项重大突破,缓解了粮食不足问题10. 用下列装置制取NH3 , 并用AlCl3溶液吸收多余NH3制Al(OH)3 , 最后回收NH4Cl,能达到实验目的的是()A、用装置甲制取NH3
2NH3(g),以下分析错误的是() A、在5L固定容积的密闭容器内,前2分钟消耗2molN2 , 则v(N2)=0.2mol·L-1·min-1 B、改变条件可使H2的转化率达100% C、每消耗3molH2 , 必然生成2molNH3 D、合成氨是人类科学史上的一项重大突破,缓解了粮食不足问题10. 用下列装置制取NH3 , 并用AlCl3溶液吸收多余NH3制Al(OH)3 , 最后回收NH4Cl,能达到实验目的的是()A、用装置甲制取NH3 B、用装置乙吸收NH3制取Al(OH)3
B、用装置乙吸收NH3制取Al(OH)3  C、用装置丙分离Al(OH)3和NH4Cl溶液时,用玻璃棒不停的在漏斗内搅拌
C、用装置丙分离Al(OH)3和NH4Cl溶液时,用玻璃棒不停的在漏斗内搅拌  D、用装置丁蒸干NH4Cl溶液并灼烧制NH4Cl
D、用装置丁蒸干NH4Cl溶液并灼烧制NH4Cl  11.
11. 分子被称为“福禄双全宝宝”。苯环上连一个氟原子、一个氯原子、两个邻位醛基的其他“福禄双全宝宝”还有几种() A、3种 B、4种 C、5种 D、6种12. 下列实验设计、操作或实验现象合理的是()A、实验室制取乙炔时:用饱和食盐水代替蒸馏水,以得到平稳的气流 B、除去苯中的少量苯酚:加入适量溴水溶液,过滤 C、检验甲酸中是否混有乙醛:可向样品中加入足量NaOH溶液以中和甲酸,再做银镜反应或与新制Cu(OH)2共热的实验 D、检验氯乙烷存在的氯元素:向氯乙烷中加入稀NaOH溶液共煮几分钟,再加入AgNO3溶液,观察是否生成白色沉淀13. 下列说法正确的是( )A、乙烯和聚乙烯都可以与溴水发生加成反应 B、在浓硫酸作催化剂条件下,加热乙醇不一定得到乙烯 C、苯酚在空气中显淡红色,并未变质 D、甲苯最多有15个原子在同一个平面14. 元素W、X、Y、Z的原子序数依次增加。p、q、r是由这些元素组成的二元化合物。m、n分别是元素Y、Z的单质,m是生产、生活中运用最广泛的金属单质,n通常为深红棕色液体,r是一种强酸,p是来自于煤的一种常见有机物,s是难溶于水、比水重的油状液体。上述物质的转化关系如图所示。下列说法正确的是()
分子被称为“福禄双全宝宝”。苯环上连一个氟原子、一个氯原子、两个邻位醛基的其他“福禄双全宝宝”还有几种() A、3种 B、4种 C、5种 D、6种12. 下列实验设计、操作或实验现象合理的是()A、实验室制取乙炔时:用饱和食盐水代替蒸馏水,以得到平稳的气流 B、除去苯中的少量苯酚:加入适量溴水溶液,过滤 C、检验甲酸中是否混有乙醛:可向样品中加入足量NaOH溶液以中和甲酸,再做银镜反应或与新制Cu(OH)2共热的实验 D、检验氯乙烷存在的氯元素:向氯乙烷中加入稀NaOH溶液共煮几分钟,再加入AgNO3溶液,观察是否生成白色沉淀13. 下列说法正确的是( )A、乙烯和聚乙烯都可以与溴水发生加成反应 B、在浓硫酸作催化剂条件下,加热乙醇不一定得到乙烯 C、苯酚在空气中显淡红色,并未变质 D、甲苯最多有15个原子在同一个平面14. 元素W、X、Y、Z的原子序数依次增加。p、q、r是由这些元素组成的二元化合物。m、n分别是元素Y、Z的单质,m是生产、生活中运用最广泛的金属单质,n通常为深红棕色液体,r是一种强酸,p是来自于煤的一种常见有机物,s是难溶于水、比水重的油状液体。上述物质的转化关系如图所示。下列说法正确的是() A、四种元素中存在第三周期元素 B、W的氧化物常温常压下为液态 C、常温下将m投入浓硫酸中不发生任何反应 D、p的最简式是CH2
A、四种元素中存在第三周期元素 B、W的氧化物常温常压下为液态 C、常温下将m投入浓硫酸中不发生任何反应 D、p的最简式是CH2二、填空题
-
15. X、Y、Z、W、R是前三周期常见元素,T位于第四周期,其相关信息如下表:
元素
相关信息
X
宇宙中最丰富的元素
Y
其单质是空气中最主要的成分
Z
地壳中含量最高的元素
W
其原子质量数为23,中子数为12
R
其最高价氧化物对应的水化物既能与强酸反应,也能与强碱反应
T
其单质在空气中放置表面会变绿,其常见氧化物有两种,为黑色和砖红色
(1)、Y、Z、W、R四种元素的原子半径从大到小的顺序是(用元素符号表示)。(2)、YX3的电子式为;X与Z形成一种18e-的分子,其结构式为。(3)、A是人体必需的常量元素,与W同主族,位于第四周期,其原子序数为(4)、R在元素周期表中的位置为。(5)、T单质可与Y最高价氧化物对应水化物的稀溶液发生反应,该反应的离子方程式为。三、解答题
-
16. 实验室利用马矿的矿渣(成分Fe2O3、FeO、Al2O3、SiO2)制备明矾[KAl(SO4)2·12H2O]和绿矾FeSO4·7H2O。流程如下:
 (1)、操作I得到的滤渣主要成分是。(2)、加入H2O2的离子反应方程式为。(3)、若X是一种固体单质,且溶液Ⅲ的溶质只有一种,则X化学式为。(4)、向明矾水溶液中加过量的NaOH溶液,其离子方程式为。(5)、绿矾放置在空气中,可能被氧气氧化,请设计实验判断绿矾是否被氧化(简述实验过程、现象和结论) 。(6)、若实验室取用1kg矿渣(含铁元素5.6%)进行实验,操作Ⅱ中消耗铁红80g,假设每个过程反应都恰好完全进行,且忽略损失,则理论上得到绿矾g
(1)、操作I得到的滤渣主要成分是。(2)、加入H2O2的离子反应方程式为。(3)、若X是一种固体单质,且溶液Ⅲ的溶质只有一种,则X化学式为。(4)、向明矾水溶液中加过量的NaOH溶液,其离子方程式为。(5)、绿矾放置在空气中,可能被氧气氧化,请设计实验判断绿矾是否被氧化(简述实验过程、现象和结论) 。(6)、若实验室取用1kg矿渣(含铁元素5.6%)进行实验,操作Ⅱ中消耗铁红80g,假设每个过程反应都恰好完全进行,且忽略损失,则理论上得到绿矾g四、实验题
-
17. 亚硫酸钠是工业中重要的原料。某亚硫酸钠样品因在空气中放置而被部分氧化为硫酸钠。某化学实验小组设计实验测定样品中亚硫酸钠的含量。
甲方案
①准确称取5.0g样品放入烧杯中,加足量稀盐酸,充分搅拌溶解。
②边搅拌边滴加1mol·L-1BaCl2溶液至过量
③过滤,洗涤,干燥,称得固体质量为m1g
乙方案
准确称取5.0g样品置于右图锥形瓶中,并通一段时间N2。打开分液漏斗活塞,逐滴加入70%硫酸至不再产生气体。再通入一段时间N2 , 最终称得C装置反应前后增重m2g

回答下列问题
(1)、甲方案步骤①中发生了离子反应,其离子方程式为。(2)、如何判断步骤②中滴加BaCl2溶液已过量。(3)、甲方案测得的样品中亚硫酸钠的含量为(用含带m1的代数式表示)(4)、乙方案中第一次通入氮气的目的是。(5)、乙方案中B装置的作用是 , 若C、D置中药品相同,则是(填药品名称),若无D装置,测定结果(填“偏大”、“偏小”、“无影响”)(6)、有同学设计实验通过测量产生的SO2气体体积来测定样品中的亚硫酸钠含量,下列实验装置最准确、最恰当的是。
五、推断题
-
18. 阿司匹林是一种历史悠久的解热镇痛药,对预防血栓和脑梗有很好的作用,M是一种防晒剂,它们的结构简式分别为
 ,它们的合成路线如下:
,它们的合成路线如下: 
已知:Ⅰ. E的俗称水杨酸,学名2-羟基苯甲酸。

根据以上信息回答下列问题
(1)、M中无氧官能团的名称。(2)、A→B过程的反应类型为。C的结构简式。(3)、由E→阿司匹林的过程中,另一种产物是一种常见的酸,该过程化学方程式。(4)、下列关于阿司匹林和防晒剂M说法正确的是_________(双选)。A、M的分子式是C15H19O3 B、两者都可发生氧化反应 C、1mol阿司匹林完全水解,需消耗3molNaOH D、1molM与足量氢气发生加成反应,最多消耗1molH2(5)、阿司匹林有多种同分异构体,请写出同时满足下列条件的任意一种同分异构体的结构简式。ⅰ苯环上有3个取代基;
ⅱ能发生水解反应,能发生银镜反应,还能与NaHCO3产生CO2
(6)、写出由I到M的合成路线(第一步已给出):合成路线示例如下:
-
-
-