四川省遂宁市2017-2018学年高一下学期化学期末考试试卷
试卷更新日期:2019-05-28 类型:期末考试
一、单选题
-
1. “绿水青山就是金山银山”,十九大再次强调环境保护的重要性。“绿色化学”的核心是实现污染物“零排放”。下列符合 “绿色化学”理念的是( )A、甲烷与氯气制备一氯甲烷 B、用稀硝酸和铜反应制取Cu(NO3)2 C、由反应2SO2+02 2SO3制SO3 D、向铜和稀硫酸的溶液中加入H2O2制备硫酸铜2. 下列说法正确的是( )A、石油的分馏、煤的干馏都是化学变化 B、PCl3分子中各原子属于8电子结构 C、海水含溴元素,向海水中加入苯可以提取单质溴 D、用电解氯化钠饱和溶液制取钠3. 下列各组化合物的性质比较,正确的是( )A、熔点:Li<Na<K B、稳定性:HF<HCl<HBr<HI C、酸性:HClO4<H2SO4<H3PO4 D、氧化性:K+< Na+< Li+4. NA表示阿伏加德罗常数的值,下列说法正确的是( )A、常温下,1mol—OH所含的电子数目为9NA B、常温下,在16g 18O2中含有NA个氧原子 C、1 mol乙烷中含有C—H的键数为7NA D、标准状况下,11.2LSO2与足量O2反应生成SO3分子数 0.5NA5. 下列说法写正确的是( )A、 Rn+ 的质子数为 Z ,中子数为A B、乙烯的结构简式:CH2CH2 C、氯化镁的电子式:
 D、HClO的结构式:H-Cl-O
6. 下列各组物质中一定属于同系物的是( )A、C2H4和C4H8 B、烷烃和环烷烃 C、C3H7Cl与C5H11Cl D、正丁烷和异丁烷7. 下列各组物质中所含化学键类型完全相同的是( )A、NaF、HCl B、NaOH、NaHS C、MgCl2、Na2O2 D、CaO、Mg(OH)28. 下列叙述正确的是( )A、乙烷中含乙烯杂质可以加入氢气反应除去 B、C4H9Br的同分异构体有4种 C、淀粉溶液中加入KI溶液,液体变蓝色 D、蔗糖溶液加入3滴稀硫酸,水浴加热后,加入新制Cu(OH)2 , 加热产生砖红色沉淀9. 下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )
D、HClO的结构式:H-Cl-O
6. 下列各组物质中一定属于同系物的是( )A、C2H4和C4H8 B、烷烃和环烷烃 C、C3H7Cl与C5H11Cl D、正丁烷和异丁烷7. 下列各组物质中所含化学键类型完全相同的是( )A、NaF、HCl B、NaOH、NaHS C、MgCl2、Na2O2 D、CaO、Mg(OH)28. 下列叙述正确的是( )A、乙烷中含乙烯杂质可以加入氢气反应除去 B、C4H9Br的同分异构体有4种 C、淀粉溶液中加入KI溶液,液体变蓝色 D、蔗糖溶液加入3滴稀硫酸,水浴加热后,加入新制Cu(OH)2 , 加热产生砖红色沉淀9. 下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )元素代号
L
M
Q
R
T
原子半径/nm
0.160
0.143
0.086
0.102
0.074
主要化合价
+2
+3
+2
+6、-2
-2
A、L、R形成的简单离子核外电子数相等 B、单质与浓度相等的稀盐酸反应的速率为Q>L C、氢化物的还原性为H2T>H2R D、M与T形成的化合物既能与强酸反应又能与强碱反应10. 实验室用海带提取碘的操作过程中,所选仪器错误的是( )选项
操作
所选仪器
A
称取3.0 g的干海带
托盘天平
B
灼烧干海带至完全变成灰烬
蒸发皿
C
过滤煮沸后的海带灰与水的混合液
漏斗
D
用四氯化碳从氧化后的海带灰浸取液中提取碘
分液漏斗
A、A B、B C、C D、D11. 金刚石和石墨是碳元素的两种单质(同素异形体)。在100 kPa时,1 mol金刚石和1 mol石墨在氧气中完全燃烧放出的热量分别为395.4 kJ和393.5 kJ,下列说法正确的是( )A、1 mol石墨转化为1 mol金刚石时要放出1.9 kJ的热能 B、1 mol石墨比1 mol金刚石的能量高 C、1 mol石墨的总键能比1 mol金刚石的总键能大1.9 kJ D、金刚石比石墨稳定12. 砹是原子序数最大的卤族元素,推测砹或砹的化合物最不可能具有的性质是( )①砹化氢很稳定
②砹单质与水反应,使砹全部转化成氢砹酸和次砹酸
③砹是黑色固体
④砹化银难溶于水
⑤砹易溶于某些有机溶剂.
A、只有①② B、只有①②⑤ C、只有③⑤ D、只有②⑤13. 下列说法错误的是( )①共价化合物含共价键,也可能含离子键
②H2CO3酸性<H2SO3酸性,故非金属性C<S
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤熔融状态能导电的物质是离子化合物
⑥由分子组成的化合物中一定存在共价键
A、①③⑤ B、②④⑥ C、①②④⑥ D、①③⑤⑥14. 将一定量纯净的氨基甲酸铵(NH2COONH4)置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)。下列可以判断该分解反应已经达到化学平衡状态的是( )A、2v (NH3)=v (CO2) B、密闭容器中气体密度不变 C、密闭容器中混合气体的平均摩尔质量不变 D、密闭容器中氨气的体积分数不变15. 近两年流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品。苹果酸(α-羟基丁二酸)是这种饮料的主要酸性物质,苹果酸的结构简式为 ,下列说法错误的是( ) A、苹果酸在一定条件下能发生酯化反应 B、苹果酸在一定条件下能发生催化氧化反应 C、苹果酸在一定条件下能发生取代反应 D、1 mol苹果酸与Na2CO3溶液反应最多消耗1 mol Na2CO316. 将等物质的量的A、B混合于2L的密闭容器中,发生下列反应:3A(g)+B(g)⇌xC(g)+2D(g),经2min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.25mol•L﹣1•min﹣1 , 下列说法正确的是( )A、该反应方程式中,x=1 B、2min时,A的转化率为50% C、2min时,A的物质的量为0.75mol D、反应速率v(B)=0.25 mol•L﹣1•min﹣117. 已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性,下列说法正确的是( )A、X、Y、Z、W的原子半径依次减小 B、W与X形成的化合物中只含离子键 C、W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 D、若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W318. 如图所示的是常见四种有机物的比例模型。下列说法正确的是( )A、
,下列说法错误的是( ) A、苹果酸在一定条件下能发生酯化反应 B、苹果酸在一定条件下能发生催化氧化反应 C、苹果酸在一定条件下能发生取代反应 D、1 mol苹果酸与Na2CO3溶液反应最多消耗1 mol Na2CO316. 将等物质的量的A、B混合于2L的密闭容器中,发生下列反应:3A(g)+B(g)⇌xC(g)+2D(g),经2min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.25mol•L﹣1•min﹣1 , 下列说法正确的是( )A、该反应方程式中,x=1 B、2min时,A的转化率为50% C、2min时,A的物质的量为0.75mol D、反应速率v(B)=0.25 mol•L﹣1•min﹣117. 已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性,下列说法正确的是( )A、X、Y、Z、W的原子半径依次减小 B、W与X形成的化合物中只含离子键 C、W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 D、若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W318. 如图所示的是常见四种有机物的比例模型。下列说法正确的是( )A、 能使酸性高锰酸钾溶液褪色
B、
能使酸性高锰酸钾溶液褪色
B、 可与溴水发生取代反应使溴水褪色
C、
可与溴水发生取代反应使溴水褪色
C、 在铁作催化剂时能与溴水发生取代反应
D、
在铁作催化剂时能与溴水发生取代反应
D、 在浓硫酸的存在并加热的条件下可与乙酸发生取代反应
19. 目前世界上60%的镁是从海水中提取的.主要步骤如下:
在浓硫酸的存在并加热的条件下可与乙酸发生取代反应
19. 目前世界上60%的镁是从海水中提取的.主要步骤如下:
下列说法错误的是( )
A、为使海水中的MgSO4转化成Mg(OH)2 , 试剂①可选择石灰乳 B、加入试剂①后,分离得到Mg(OH)2沉淀的方法是过滤 C、加入试剂②反应的离子方程式为:OH﹣+H+=H2O D、通过电解熔融的无水MgCl2得到48gMg,共转移4mol电子20. 某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是( ) A、正极反应为AgCl+e-=Ag+Cl- B、负极反应为Ag-e-=Ag+ C、放电时,交换膜右侧溶液中有大量白色沉淀生成 D、当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
A、正极反应为AgCl+e-=Ag+Cl- B、负极反应为Ag-e-=Ag+ C、放电时,交换膜右侧溶液中有大量白色沉淀生成 D、当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子二、综合题
-
21. 下表是元素周期表的前四周期,请回答有关问题:(相关均用具体化学用语回答)
1
①
2
②
③
④
3
⑤
⑥
⑦
⑧
4
⑨
⑩
(1)、元素⑤⑥⑦的简单离子半径大小顺序;②在元素周期表位置;③的简单氢化物和⑧的氢化物混合形成的化合物电子式。(2)、⑤其最高价氧化物水合物和⑥的最高价氧化物反应的离子方程式(3)、用电子式表示元素①和⑧形成的化合物的形成过程。(4)、④、⑧、⑩的氢化物沸点最高的是 , 原因是。(5)、由②和①组成最简单物质与O2和⑨的最高价氧化物对应的水化物的水溶液组成燃料电池,写出电池的负极反应式。22.(1)、Ⅰ.过量铁片与100mL 0.01mol/L的稀盐酸反应,能量变化趋势,如图所示:
该反应为反应(填“吸热”或“放热”)。
(2)、为了加快产生H2的速率而不改变H2的产量,可以使用如下方法中的______①加H2O ②加入几滴1mol/LHNO3溶液 ③滴入几滴浓盐酸
④加入一定量铁粉 ⑤加NaCl溶液 ⑥滴入几滴硫酸铜溶液
⑦适当升高温度(不考虑盐酸挥发) ⑧改用10mL0.1mol/L盐酸
A、②③⑥⑦⑧ B、③④7⑧ C、③⑥⑦⑧ D、③⑥⑦(3)、若将上述反应设计成原电池,铜为原电池某一极材料,则铜电极上发生的电极反应为。(4)、Ⅱ.某温度时,在5 L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题: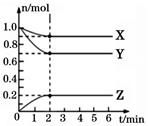
分析有关数据,写出X、Y、Z的反应方程式。
(5)、该反应在3 种不同条件下进行,其中Y起始浓度相同,Z起始浓度为0,反应物X的浓度随反应时间的变化情况如下表:
①实验1中,在10~20 min内,以物质Y表示的平均反应速率为mol/(L·min) ,50min时,实验3中Z的浓度。
②0~20min内,其它条件一样实验2 和实验1的反应速率不同,其原因可能是;实验3 和实验1的反应速率不同,其原因是。
三、推断题
-
23. A,B,C,D,E均为有机物,其中A是化学实验中最常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平,有关物质的转化关系如图①所示:
 (1)、写出B的结构简式 , A中官能团的名称为。(2)、反应②和④的反应类型分别是、。(3)、写出下列反应的化学方程式:反应① , 反应④。(4)、实验室利用反应③制取C,常用上图②装置:
(1)、写出B的结构简式 , A中官能团的名称为。(2)、反应②和④的反应类型分别是、。(3)、写出下列反应的化学方程式:反应① , 反应④。(4)、实验室利用反应③制取C,常用上图②装置:①a试管中的主要化学反应的方程式为。
②在实验中球形干燥管除起冷凝作用外,另一个重要作用是。
③试管b中液体作用是。
四、实验题
-
24. 工业生产需要大量原料,消耗大量能源,在得到所需产品同时产生了大量废气、废水、废渣。某工厂排放的废水中含有Cu2+、Fe2+、Hg2+、H+等离子,某化学小组为了充分利用资源和保护环境,准备回收废水中的铜和汞,同时得到绿矾。他们设计了如下实验方案:
 (1)、现有仪器:酒精灯、玻璃棒、坩埚、蒸发皿、蒸馏烧瓶、烧杯、铁架台等,完成步骤Ⅳ的实验操作还需要选择的玻璃仪器是设计简单实验检验绿矾是否变质,简述你的操作:。(2)、步骤Ⅰ中加入过量铁粉的目的是 , 步骤Ⅱ中(填“能”或“不能”)用盐酸代替硫酸。(3)、步骤V利用氧化铜制取铜有如下四种方案:
(1)、现有仪器:酒精灯、玻璃棒、坩埚、蒸发皿、蒸馏烧瓶、烧杯、铁架台等,完成步骤Ⅳ的实验操作还需要选择的玻璃仪器是设计简单实验检验绿矾是否变质,简述你的操作:。(2)、步骤Ⅰ中加入过量铁粉的目的是 , 步骤Ⅱ中(填“能”或“不能”)用盐酸代替硫酸。(3)、步骤V利用氧化铜制取铜有如下四种方案:方案甲:利用氢气还原氧化铜;
方案乙:利用一氧化碳还原氧化铜;
方案丙:利用炭粉还原氧化铜;
方案丁:先将氧化铜溶于稀硫酸,然后加入过量的铁粉、过滤,再将滤渣溶于过量的稀硫酸,再过滤、洗涤、烘干。
从安全角度考虑,方案不好;从产品纯度考虑,方案不好。
(4)、写出步骤Ⅱ中涉及反应的离子方程式:;步骤Ⅳ得到绿矾的操作蒸发浓缩、。
-